在中国🇨🇳,PD-1的第一大适应症是EGFR(-)ALK(-)非小细胞肺癌(NSCLC),中国每年新增肿瘤病例450万,其中31万新增病例是EGFR(-)ALK(-)NSCLC。
在美国🇺🇸,默沙东K药营收来源中,65%来源于EGFR(-)ALK(-)NSCLC,10%来源于黑色素瘤,5%来源于尿路上皮癌。
但是,这不是真相的全部。
美国🇺🇸每年新增肿瘤病例180万,其中22.2万例是肺癌,8.1万例是尿路上皮癌。
也就是说,PD-1的尿路上皮癌适应症并没有被充分开发。
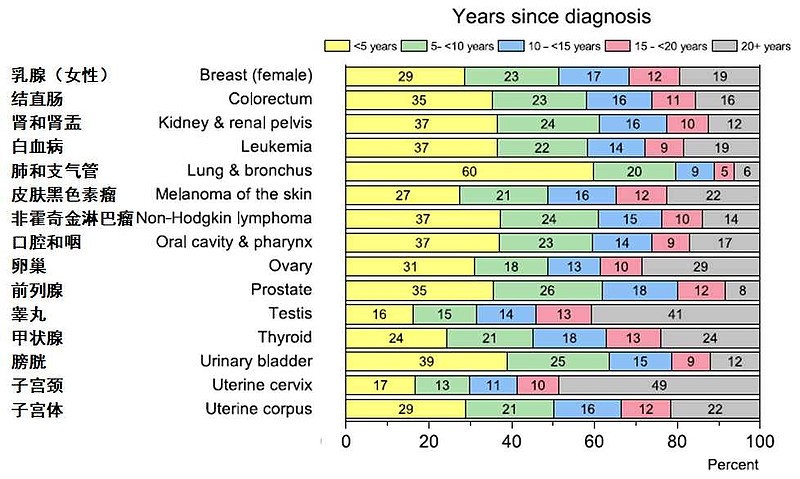
2019年美国,肺癌患者生存期较短,OS<5年的比例是60%。尿路上皮癌(膀胱癌)患者生存期也较短,OS<5年的比例是39%。
所以,尿路上皮癌急需更好疗效的药物上市。
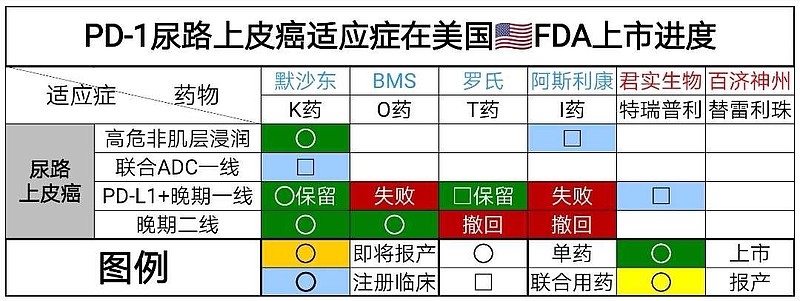
美国🇺🇸PD-L1+尿路上皮癌一线适应症对应的是,
①阿斯利康PD-L1联合CTLA-4的3期临床失败。
②罗氏PD-L1联合化疗的3期临床错过OS终点,FDA投票保留适应症。
③默沙东PD-1单药的3期临床OS对比化疗组没有显著差异,FDA投票保留适应症。
美国🇺🇸尿路上皮癌二线适应症,
①阿斯利康PD-L1单药二线治疗适应症被FDA撤回。
②罗氏PD-L1单药二线治疗适应症被FDA撤回。
所以,美国🇺🇸PD-1尿路上皮癌适应症,差一点沦为#无药可用# 的境地。
然后,可以看见一个奇怪的现象。
(1)$荣昌生物-B(09995)$ RC48(HER2-ADC),≥2线治疗HER2+尿路上皮癌,确证客观缓解率(cORR)达到51.2%。获得美国🇺🇸FDA‘‘突破性疗法认定’’。总计才43例2期临床证据。(RC48已经被Seagen西雅图基因26亿美元买走欧美曰发达国家的商业开发权益)
(2)$Seagen(SGEN)$ 西雅图基因Padcev+默沙东K药无铂联合用药,一线治疗尿路上皮癌,确认的客观缓解率(cORR)高达73.3% 。获得美国🇺🇸FDA‘‘突破性疗法认定’’。总计才45例1b/2期临床证据。
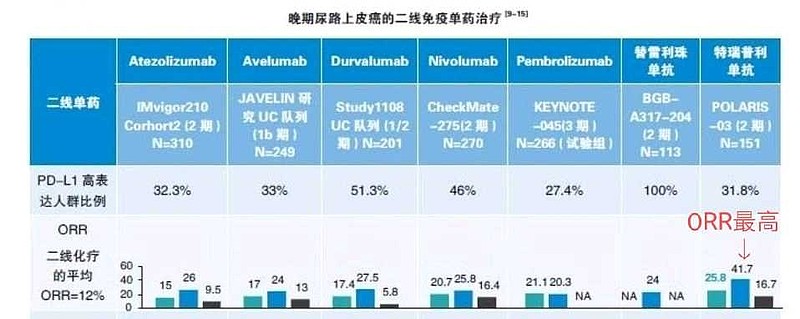
其实,其他PD-1/PD-L1的ORR很低,君实生物特瑞普利单抗单药≥2线治疗PD-L1+尿路上皮癌,cORR=41.70%,也应该算‘‘突破性疗法’’(2期临床,PD-L1+病例总计48例)。
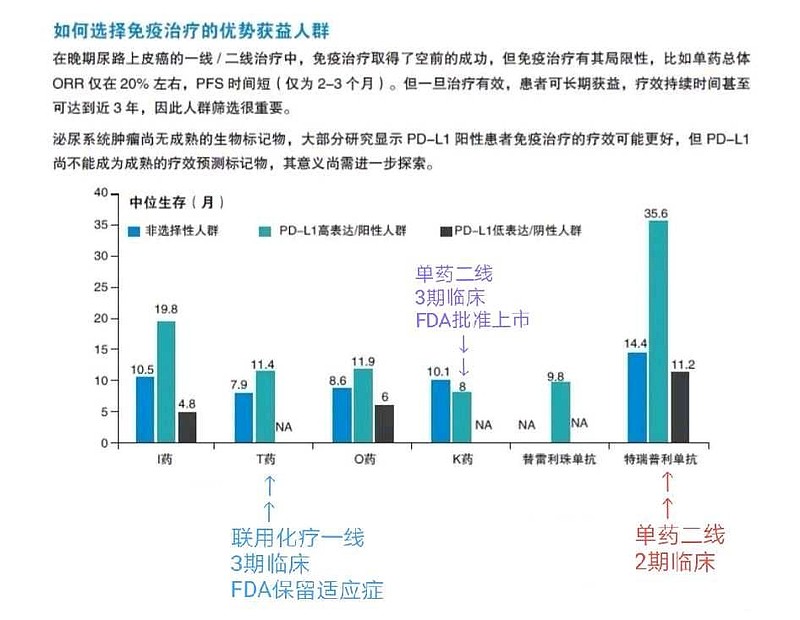
更夸张的是,PD-L1+尿路上皮癌的关键注册证据OS,$君实生物-U(SH688180)$ 特瑞普利单抗≥2线治疗mOS(中位生存期)=35.6个月,数据漂亮得令人震惊。
所以,君实生物在海外选择PD-1注册临床试验的策略是,
特瑞普利单抗+化疗,一线治疗PD-L1+尿路上皮癌,启动了#国际多中心3期临床# ,就是在欧美国家树立#独家适应症# 优势。