有观点,有态度
这是医业观察的第2152-4期文章
来源:CACLP体外诊断资讯
阿尔茨海默病(AD)是一种神经系统退行性疾病,临床前阶段可长达10-20年。随着人口老龄化进程的加快,以阿尔茨海默病为主的老年痴呆疾病发病人数持续增加,严重威胁老年人健康和生命质量。
《2022年中国阿尔茨海默病报告》显示,2019年我国约有1314万阿尔茨海默病(AD)患者;预计到2050年,这一数字将超过2800万,治疗总费用将超1.8万亿美元,成为一笔废大的医疗费用支出。据WHO预计,2050年全球AD患者将增至0.83-1.11亿。
阿尔兹海默症多发于60岁以上高龄人群,患者群体正在扩大,并且患者年龄越来越年轻。中国老龄人口迅速增长,在2011-2022年的10年时间里,60岁以上人口从1.85亿增长到2.8亿,预计到2035年左右,60岁及以上的老年人将超4亿【3】。老龄化背景下,阿尔兹海默症已成为全球范围内一大公共健康挑战,存在着巨大的未被满足的需求,针对阿尔兹海默症的相关药物与检测在未来具有广阔的应用前景。
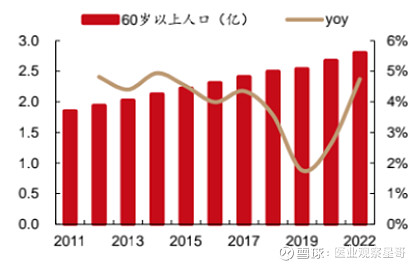
中国历年60岁以上老人数量图片来源:西部证券
AD发病人数不断增加,带来巨大的社会负担,随着阿尔兹海默症药物研发的不断突破,检测端的潜在需求有望持续增加。早期发现、早期诊断、早期治疗已成为防治阿尔茨海默病的重要策略。
目前阿尔兹海默症检测的金标准是PET-CT,但其大范围筛查成本昂贵。外周血检测具有检测效果好、侵入性低、价格相对低廉等优势。随着血标志物检测技术不断成熟,有望与影像学诊断形成有力互补。
多文件出台 推动AD早筛

2024 年 1 月 15 日国务院办公厅发布《关于发展银发经济增进老年人福祉的意见》,提到开发老年病早期筛查产品和服务,对阿尔兹海默病等老年病的诊断设备和试剂市场具有促进作用。
2023年国家卫生健康委办公厅发布《关于开展老年痴呆防治促进行动(2023-2025年)的通知》提出:开展老年人认知功能筛查及早期干预,指导有条件的地区结合实际为辖区内65岁及以上常住居民每年提供1次认知功能初筛。
《阿尔茨海默病的诊疗规范(2020版)》明确提出尽早诊断、及时治疗、终身管理的治疗原则。
AD生物标志物

《阿尔茨海默病源性轻度认知障碍诊疗中国专家共识2021》指出,阿尔茨海默病体液检查包括:
1、血浆Aβ42/Aβ40、P⁃tau217、P⁃tau181和NfL可用于AD源性MCI的早期诊断和疾病进展的评估(I级推荐,A级证据)。
2、脑脊液Aβ42、Aβ42/Aβ40、P⁃tau181、P⁃tau217、T⁃tau、NfL可用于AD源性MCI的早期诊断及疾病进展的评估(I级推荐,A级证据)。
3、ApoE基因型检测可用于MCI患者危险分层,预测其向AD转化的风险,并可应用于临床研究中的疗效分析(IIa级推荐,B级证据)。
2023年7月新修订的阿尔茨海默病诊断指南草案(NIA-AA Revised Clinical Guidelines for Alzheimer’s)发布,将血液和脑脊液合并为体液,推荐了用于诊断阿尔茨海默病的核心生物标志物:
1)AD 核心生物标志物:包括反映 Aβ 积聚的生物标志物(A)(CSF/血浆 Aβ42/40;amyloid-PET)和 tau 病理生物标志物(T)(CSF/血浆 p-Tau181;CSF/血浆 p-Tau217;tau-PET);
2)在 AD 发病机制中很重要,但也涉及其他神经退行性疾病的非特异性生物标志物:包括神经元变性或损伤的生物标志物(N)(CSF/血浆 NfL;结构磁共振脑区萎缩;FDG-PET)和炎症/免疫生物标志物(I)(CSF/血浆 GFAP);
根据NIA-AA联合发布的《Revised Criteria for Diagnosis and Staging of Alzheimers Disease》,3)可用于AD诊断及病情监测的血液标志物及指标包括:p-tau217、p-tau217/np-tau217、pT205、NfL、GFAP等。
总体而言,目前已确立的核心标志物包括脑脊液中的Aβ42(Aβ42/Aβ40比例)、T-tau以及P-tau,其经过数百个实验室重复验证得到了一致认可。
国内外部分检测试剂生产企业

2023年6月,日本富士(Fujirebio)获得了其自动化Aβ42/40脑脊液分析仪的FDA批准,同期罗氏(Roche)则获得了其自动化Aβ42/p-tau181和Aβ42/t-tau脑脊液测试的批准。由于这些测试已经通过淀粉样蛋白PET进行了验证,因此,相关开发者可能只需要做很少的工作来使它们完全符合FDA新标准。Quest诊断公司一度直接向消费者推销了一项AD血液测试,引发了该领域的强烈反对。 越来越多的AD实验室检测诊断方法进入市场。对于痴呆症的血液生物标志物来说,目前还不具备这些条件,因此FDA的这一决定应该会激励那些开发此类测试的人加快步伐。
目前,国内获批血液标志物检测试剂企业快速增多,预计未来潜在市场广阔。根据NMPA显示,国产企业中目前国内已获批AB生物标志物检测试剂的包括11个企业的20个注册证。已获批p-tau生物标志物检测试剂的包括11个企业的21个注册证,均为二类注册证,涉及的方法学包括酶联免疫法荧光免疫层析法磁微粒化学发光法等。
部分企业及产品:
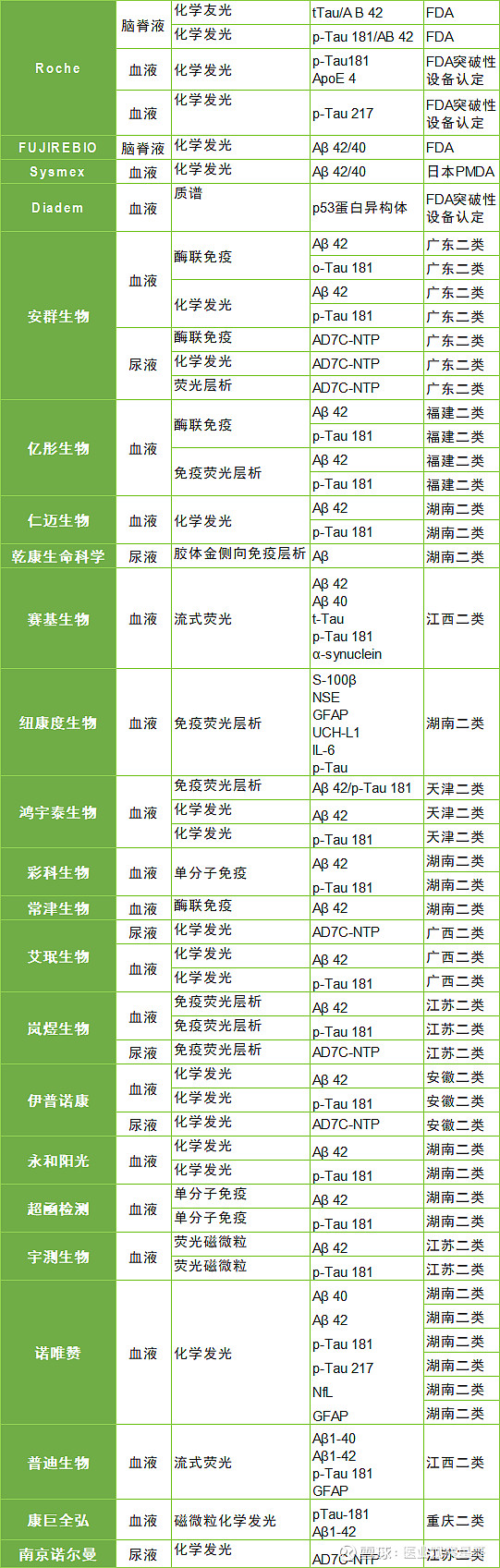
---The End---
欢迎扫码添加编辑微信号,加入行业交流群
欢迎点击关注
喜欢就一键三连,点赞,在看,分享!