有观点,有态度
这是医业观察的第2133-2期文章
来源:安必平、企业公告等
整理:医业观察
编辑:小K
5月8号,广州安必平医药科技股份有限公司发布关于自愿披露取得医疗器械注册证的公告。
广州安必平医药科技股份有限公司(以下简称“公司”)于近日收到由国家 药品监督管理局颁发的《医疗器械注册证(体外诊断试剂)》
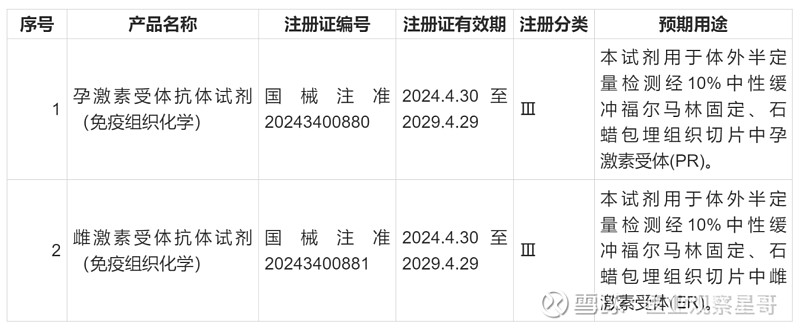
在2024年的4月19日,广州安必平医药科技股份有限公司研制的HER2抗体试剂(免疫组织化学)取得了国家药品监督管理局颁发的医疗器械注册证(国械注准20243400697)。
据悉,安必平新获证的这两款试剂与公司现有的 HER2 抗体试剂(免疫组织化学)、HER2 基因检测 试剂盒(荧光原位杂交法)联合使用可提供更加完善的乳腺癌检测套餐,有利 于扩充公司在肿瘤筛查与精准诊断领域的产品布局,加深各技术平台的联动, 围绕临床需求,从单一技术检测到提供多技术、多靶点联合检测,进一步增强公司的核心竞争力。至此,安必平HER2/ER/PR乳腺癌三证齐了!
安必平一直聚焦肿瘤筛查和精准诊断的产品和服务,主要面向医院病理科。在宫颈癌筛查领域,安必平可提供细胞学、HPV基因检测、p16/Ki-67双染检测等多技术联合筛查和检测。继宫颈癌之后,针对威胁女性的另一大癌种乳腺癌,安必平再次实现了突破性进展。
乳腺癌治疗任重道远
最新的国际癌症研究显示,全球新发癌症病例数量在2022年达到了1996万例,其中乳腺癌的发病率位居第二。特别是对于女性而言,乳腺癌已成为最常见的癌症类型。据2024年4月16日发表在国际医学期刊《柳叶刀》上的一份详尽报告指出,虽然过去三十年的癌症研究与治疗已经取得显著进展,使得多数高收入国家的乳腺癌死亡率下降了超过40%,但在2020年,仍有约68.5万名女性死于此病。该报告预计,到2040年,全球的乳腺癌病例将从2020年的230万例增至超过300万例,死亡人数可能达到100万。
在当今医学技术不断进步的背景下,我们有充分的理由期待乳腺癌在早期发现和治疗的助力下,继宫颈癌之后,成为人类彻底攻克的又一癌症。安必平将继续以临床诊断需求为核心,利用其在细胞学、免疫组化、荧光原位杂交及PCR技术领域的专业积累。安必平通过推动数字化和智能化的创新,以及加强与药企的合作和伴随诊断,致力于提高临床诊疗的精准性。这不仅能够提供更精确的预后检测和用药指导,还将极大优化患者的治疗成果。
安必平业务结构明显优化
根据2023年年度报告显示,由于医院病理科检测业务恢复比较缓慢,公司实现营业收入4.97亿元,实现归属于母公司所有者的净利润4005.72万元,与上一年基本持平。
综合公司年报可以看出,上市以后,安必平一直在加大研发投入,2023年度公司研发投入达7738.71万元,同比增长12.39%,占公司营业收入15.56%,为近年最高。
随着研发投入项目逐步落地,公司认为现有病理检测技术平台液基细胞学、PCR、免疫组织化学和荧光原位杂交已经明确各自优势,未来将加强具有独占技术优势、靶点的市场占有率,同时加深各技术平台的联动,从单一技术检测到提供某一癌种筛查、诊断的多技术、多靶点联合检测方案;继续通过数字化、智能化产品增加现有客户黏性、刺激增量需求,拓展新增大客户。随着病理共建、药企服务和伴随诊断、海外市场等战略逐步落地,加强了各个业务模块的协同作用。
从肿瘤检测临床需求来看,往往需要多个技术联合诊断,才能相互验证,明确诊断结果。据公司透露,目前公司在检测技术布局上已经可以在多个癌种上实现联动,比如宫颈癌癌前病变、乳腺癌、肺癌、淋巴瘤等靶点交叉检测诊断。以宫颈癌筛查为例,在细胞学与HPV联检的基础上,进一步拓展免疫细胞技术 p16/Ki-67双染检测对宫颈病变的分流检查;针对非小细胞肺癌,可以联合使用公司的荧光原位杂交、免疫组织化学两种方法学,进一步明确MET扩增检测。
---The End---
欢迎扫码添加编辑微信号,加入行业交流群
欢迎点击关注
喜欢就一键三连,点赞,在看,分享!