
频繁吸引MNC的中国Biotech
一直关注着这个行业内真正有实力和技术的一批人的走向,也代表着这个时代转变的标志:掌握核心技能的人将主导行业的发展脉络。双抗领域,从信达生物出走的研发巨擘刘晓林创建的普米斯生物正在积蓄新力量;ADC领域,科伦博泰因Trop2 ADC牵手MSD,从科伦出走的研发团队创建的宜联生物也频繁获得国外药企合作。一众新生力量开始依托于资本的青睐,会在风向已经明确的赛道,如双抗、ADC领域,异军突起 ,攫取new money,成为聚光灯下的闪亮新星。


宜联生物丨快讯
2024年5月27日,ADC赛道新贵苏州宜联生物宣布与不缺钱却亟需转型的BioNTech达成新的的战略合作:
BioNTech将获得一项利用宜联生物TMALIN® ADC技术平台开发针对限定的某几个前沿创新靶点的ADC产品的独家选择权及相应全球独家许可。根据新协议条款,宜联生物将获得2500万美元的首付款,并有资格获得最高可达18亿美元的开发、监管和商业化里程碑付款,以及未来基于全球年度销售净额的梯度特许权使用费。

这是两家企业的第二次合作,早在2023年10月12日,达成战略合作和全球许可协议,BioNTech正在开创针对癌症和其他重症疾病的新疗法。双方将合作开发新一代的HER3 ADC。
根据协议条款,宜联生物将授予BioNTech其所拥有的一款ADC产品在全球范围内(不包括中国内地、香港和澳门)开发、制造和商业化的独家权利。BioNTech将向宜联生物支付7000万美元首付款,以及额外开发、监管和商业化里程碑付款,潜在总金额超过10亿美元。该协议的完成将受制于常规交易达成条件,包括根据哈特-斯科特-罗丁诺(“HSR”)反垄断改进法案的批准。
BioNTech,先后合作国内的一众企业,包括映恩生物、普米斯、昂科免疫,包括今天要谈的宜联生物。
(具体详情见:网页链接{BioNtech合作宜联生物HER3 ADC,预测成药性如何}、诺奖得主加盟的BioNTech掀起国内Biotech合作狂潮)
对于MNC来说,投资要未雨绸缪进行差异化管线布局,以小成本的预付款和里程碑限定,四处扫货,是大厂的投资逻辑。先后获得BioNTech两次合作的宜联生物究竟吸引力在哪里,本文就核心管理团队和管线进行介绍。
起底宜联生物
宜联生物成立于2020年7月8日,是一家专注于抗体药物结合物(ADC)和相关技术的创新药物开发公司。宜联生物由来自小分子和大分子药物开发领域的经验丰富的科学家组成。主要创始人简历如下:



ADC平台技术—TMALIN
传统ADC药物仍有许多缺点。
抗体需要被细胞吸收到溶酶体中,因此ADC药物的抗体选择是有限的。
有效载荷需要通过多个环节释放,如肿瘤细胞内吞和溶酶体溶解,其中许多环节可能导致耐药性或ADC无治疗效果。
当分子量较大时,肿瘤富集速度慢,通透性低,靶抗原表达低,很难发挥良好的治疗效果。
TMALIN(Tumor_Microenvironment_Activable_LINker)技术平台可以解决现有ADC技术的缺陷。
独特的酶消化特性,具有在肿瘤微环境中细胞外溶解的能力,无论抗体是否具有内吞能力,所形成的ADC仍具有较高的抗肿瘤活性,大大拓宽了抗体的选择范围;
这种特殊的结构使ADC能够丰富肿瘤微环境,增加肿瘤中有效载荷的比例和血液浓度,并具有较高的治疗指数;
酶消化特性和肿瘤富集特性使有效载荷在肿瘤组织中大大富集,产生较强的旁观者效应,在抗原表达低甚至无抗原表达的肿瘤中产生良好的抗肿瘤作用。
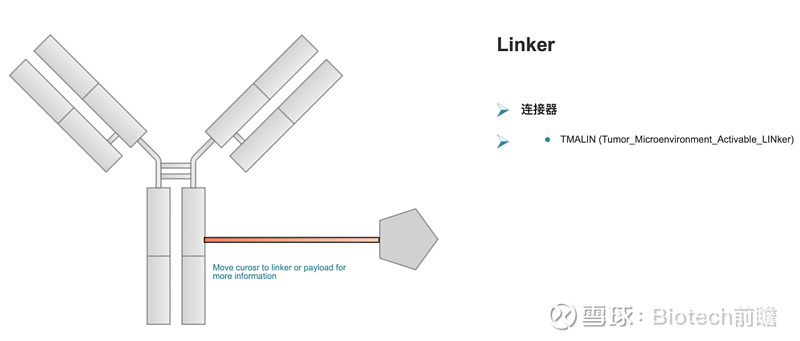
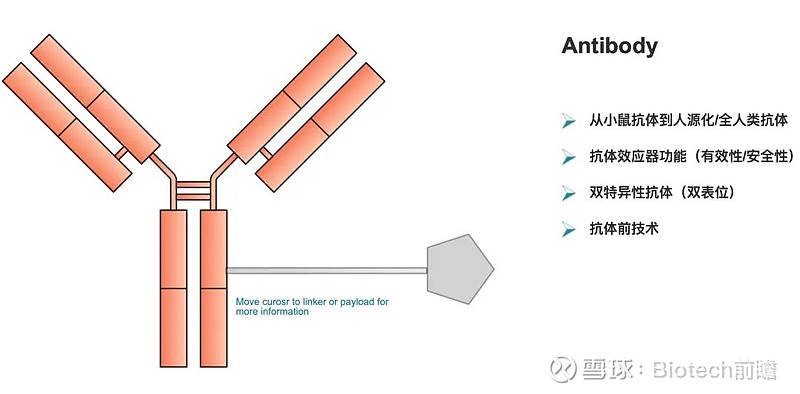
此外,TMALIN技术形成的ADC具有许多优点。
它具有极高的全身循环稳定性,可减少有效载荷在非靶组织中的脱落以及有效载荷在无靶组织中脱落所引起的“偏离靶”毒性。
它具有优异的溶解性和优异的化学稳定性,不存在传统ADC中马来酰亚胺连接方式引起的可逆Michael加成反应,可以获得高均匀度的ADC(DAR=8.0),并实现定点定量耦合。
耦合效率高(≥90%)。
目前,宜联生物通过TMALIN技术搭建了多条管线,靶点尚未公布。
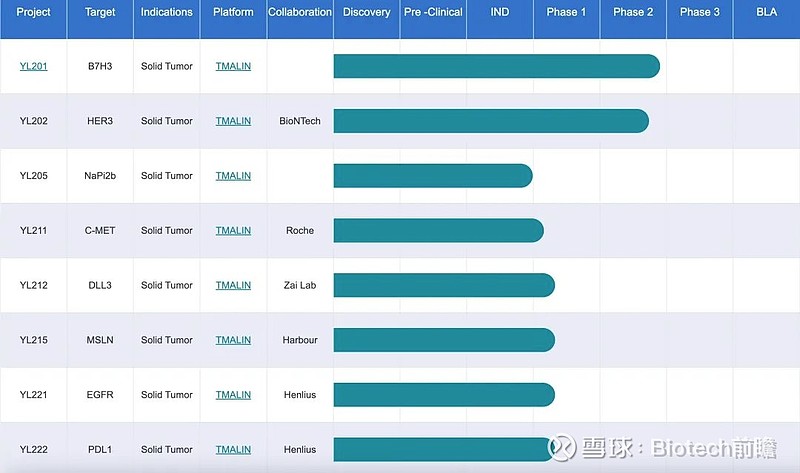
宜联生物 pipeline
(Cited by:宜联生物官方网站)
随着肿瘤药物研发领域竞争的日益白热化,基于已成药靶点的各种药物形式的探索,是相对风险性较低的研发选择。但已经商业化运作成功的可成药靶点,原本竞争就非常激烈,肿瘤免疫治疗领域的明星靶点PD-1,就是典型的例子。所以,为了尽可能避免可预见的红海市场竞争,选择明星靶点同类,且功能近似的靶点,应该是不少药企的不二选择。正如当下各大药企在LAG3、OX40等免疫检查点的探索,可惜的是,鲜有成功者。此时,不妨将注意力放到靶向药物领域成熟靶点的再开发。衷心期望不断获得MNC关注的中国Biotech企业能够在全球靶点竞争中处于第一梯队。
参考文献
Mishra, Rosalin, et al. "HER3signaling and targeted therapy in cancer." Oncology reviews 12.1 (2018).
Mujoo, Kalpana, et al. "Regulationof ERBB3/HER3 signaling in cancer." Oncotarget 5.21 (2014): 10222.
Geuijen et al. Cancer Cell. 2018;33(5):922-36.