——快 讯——
近期,被Genmab 18亿美金全现金收购普方生物引起行业关注,普方生物是一家临床阶段的生物技术公司,致力于为治疗包括卵巢癌和其他FRα表达实体瘤在内的特定癌症研发下一代抗体偶联药物(ADC)和ADC技术,研发管线包含多种针对实体瘤和血液恶性肿瘤的在研ADC药物。
普方生物丨FRα ADC
普方生物中最核心的ADC药物为rinatabart sesutecan(Rina-S),以叶酸受体α(FRα)为靶点的ADC药物,目前推进至针对于卵巢癌和子宫内膜癌患者的临床二期研究,预计于今年晚些时候开展卵巢癌的关键临床研究。FRα是一种位于细胞膜上的叶酸结合蛋白,参与调控肿瘤细胞的浸润、增殖和转移。该受体在多种肿瘤组织中广泛高表达,如卵巢癌(76%-89%)、三阴乳腺癌(35%-68%)、非小细胞肺癌(14%-74%),而在正常组织中几乎不表达,因此FRα是开发抗肿瘤药物的理想靶点。
Immunomedics丨索米妥昔单抗
2022年11月14日,FDA加速批准由美国Immunomedics公司研发和生产的索米妥昔单抗(Elahere/HDM-2002)上市,适用于治疗既往接受过1-3种系统治疗的叶酸受体α(FRα)阳性的铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌成年患者,索米妥昔单抗由此成为全球首款FRα ADC,也标志着PROC治疗由此进入了ADC时代。索米妥昔单抗自上市后放量迅速,超出预期,2023年一季度的销售额为2950万美元,二季度为7740万美元,根据11月2号ImmunoGen发布的财报,第三季度美国净销售额为1.052亿美元,前九个月销售额达到2.12亿美元。如此亮眼的数据,聚焦的适应症是卵巢癌,也获得了国内企业的关注和引进,相信也能够造福国内的卵巢癌患者。
2023年8 月 28 日,ImmunoGen 宣布就 FRα ADC 新药索米妥昔单抗(Elahere/HDM-2002)与武田达成合作。根据协议,武田制药将获得索米妥昔单抗在日本的开发与商业化权益。ImmunoGen 则将收到武田支付的 3400 万美元预付款及近期里程碑金额,并有资格获得潜在的监管和商业里程碑付款以及两位数的销售分成。
早前在 2020 年 10 月,ImmunoGen 已将索米妥昔单抗大中华区的权益授权给华东医药,获得 4000 万美元的首付款以及最高可能达 2.65 亿美元的里程碑付款。
目前,该产品主要适应症还是聚焦在卵巢癌领域。在患者数量更大的宫颈癌领域,也迎来了免疫治疗及ADC治疗时代。
普方生物丨EGFR/c-Met ADC
2024年AACR年会(美国癌症研究协会)于4月5日-4月10日在美国圣地亚哥盛大召开。目前,AACR官网已公布部分摘要,普方生物在研的新型EGFR/cMET双特异性抗体ADCPRO1286也中了一项摘要:在临床前模型中表现出广泛的抗肿瘤活性和良好的耐受性。

本人也一直关注EGFR/c-Met双抗及EGFR/c-Met双抗ADC的研发进度。
——EGFR/c-Met 双抗——
强生丨埃万妥单抗
EGFR/c-Met双抗首个NSCLC 3期成功
2024年3月1日,强生宣布,FDA已批准埃万妥单抗(Rybrevant)联合化疗一线治疗EGFR外显子20插入突变的局部晚期或转移性非小细胞肺癌患者。FDA本次行动也将Rybrevant在2021年5月的加速批准转换为基于确认性III期PAPILLON研究的完全批准。
2023年7月20日,强生宣布,其EGFR/MET双特异性抗体疗法Rybrevant联合化疗在新诊断EGFR外显子20插入突变的晚期或转移性非小细胞肺癌患者中开展的3期PAPILLON研究取得积极结果,患者无进展生存期(PFS)出现具有统计学显著性和临床意义的改善。
除了在一线NSCLC领域有布局以外,埃万妥单抗二线治疗NSCLC也有布局。
EGFR/c-MET双抗组合疗法二线治疗NSCLC III期研究成功
2023年9月6日,强生宣布,Rybrevant(amivantamab,埃万妥单抗)联合第三代EGFR抑制剂lazertinib及化疗治疗奥希替尼耐药后的非小细胞肺癌患者的III期MARIPOSA-2研究获得积极顶线数据。
国内企业中,岸迈生物、贝达药业、嘉和生物、和翰森制药这4家企业有临床布局,高BD频出,为何5年前就坚定看好普米斯,管线细究谈原因一文中提到了普米斯。
普米斯丨PM1080
2024年3月14日,一直追踪的普米斯获得新的利好消息,翰森制药全资附属公司已经与普米斯生物签订协议,获得普米斯在研EGFR/cMet双特异性抗体PM1080的独家许可,在全球范围内将PM1080/HS-20117用于ADC产品的开发、生产、商业化。普米斯将获得翰森制药支付的首付款和基于ADC产品的开发、注册及基于销售的商业化里程碑潜在付款,合计不超过50亿元人民币,以及基于全球净销售额的分级特许权使用费。
国外企业中,对于同时拥有一代和三代EGFR TKI的阿斯利康,自然不会错过此赛道。但阿斯利康另辟蹊径,选择布局双抗EGFR/c-Met双抗 ADC(AZD9592)。
——EGFR/c-Met 双靶点 ADC——
阿斯利康丨AZD9592
2023年3月9日,据 CDE 官网显示,阿斯利康 EGFR/c-Met 双靶点 ADC 国内申报临床(受理号:JXSL2300048)。

AZD9592 为阿斯利康基于自有 ADC 平台开发的一款 EGFR/c-Met 双靶点 ADC 药物 ,而非外部合作,采用新型拓扑异构酶1载荷,旨在解决奥希替尼耐药问题。该药在临床验证的 DuetMab 单价双特异性 IgG 平台的基础上构建,并通过专有的拓扑异构酶 1 抑制剂(TOP1i)载荷 AZ14170132 与可裂解 linker 结合。相较于 EGFR,AZD9592 对 c-MET 具有更高的亲和力(>15 倍),这样设计的目的是降低由 EGFR 驱动的正常组织毒性。据 Insight 数据库显示,该药当前已经处于 I 期临床研究中。
正如网页链接{百利天恒双抗 ADC丨施贵宝首付款8亿美元已到账,加速创新},网页链接{施贵宝布局双抗ADC,首付款8亿美元合作百利EGFR/HER3 ADC} 中所提及的,MNC正在全球扫货,百利药业的潜力重磅EGFR/HER3 ADC引起了施贵宝的关注,而普方生物的FRα ADC的销售峰值可以预估,但潜力产品EGFR/c-Met 双特异性ADC如果顺利经过II期,将进一步拉升市值,在早期阶段进行布局投资,未来收益一定更大。下述汇总的全球和国内已上市的ADC潜力产品,EGFR/c-Met ADC毫无疑问都是潜力重磅产品,让我们期待EGFR/c-Met ADC能够解决EGFR/c-Met 双抗的高输液反应和不良反应高的弊端。
全球及国内上市ADC产品汇总
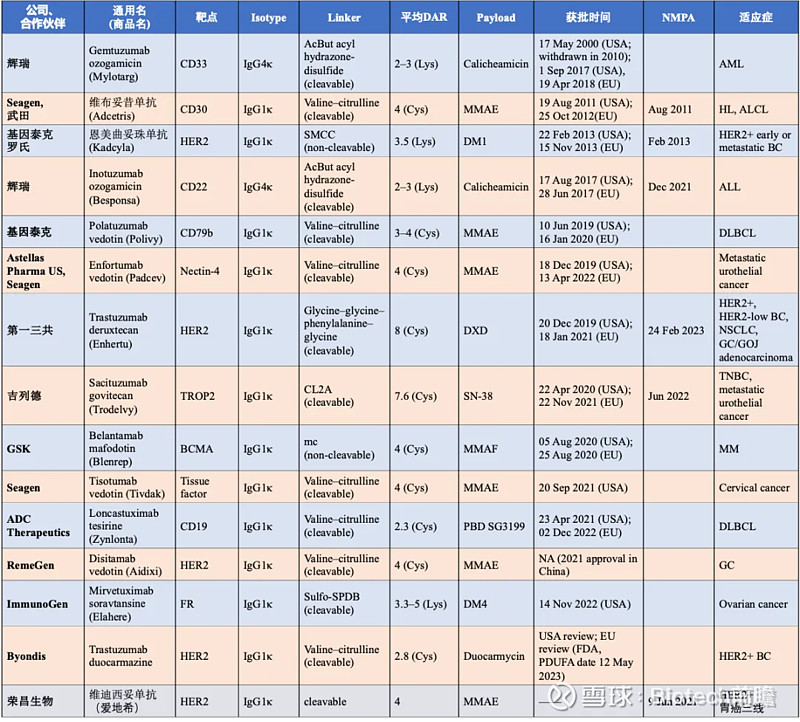
全球已获批ADC
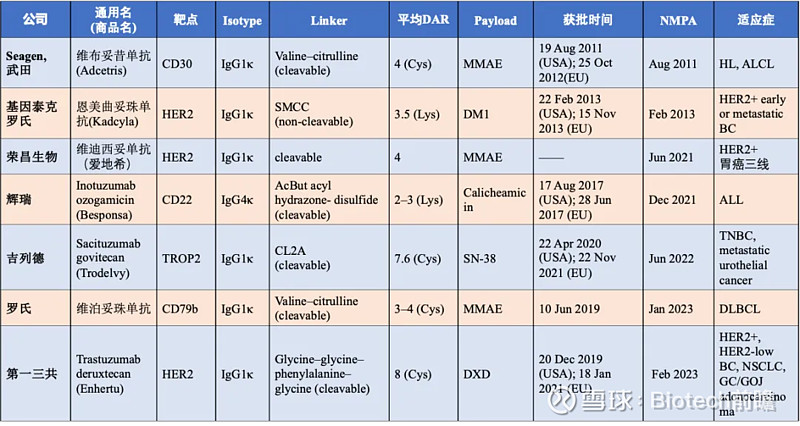
国内已获批ADC
临床试验阶段的ADC
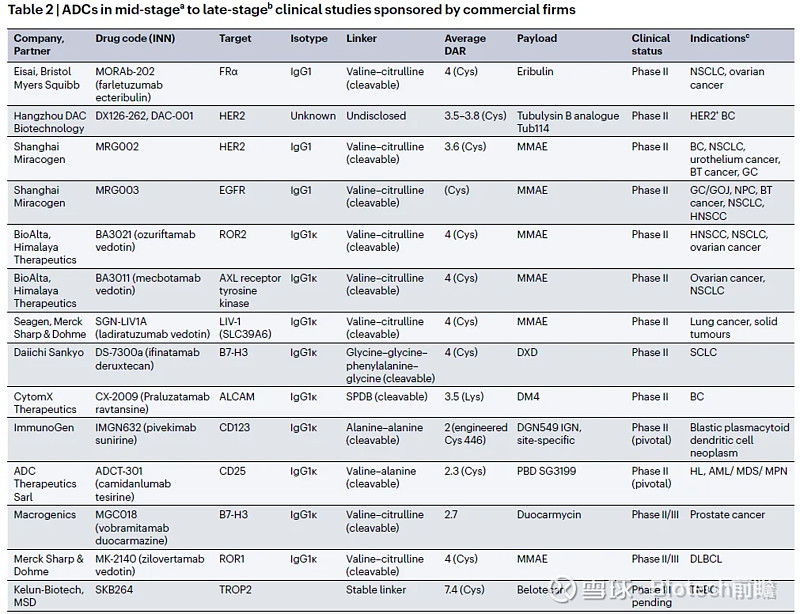
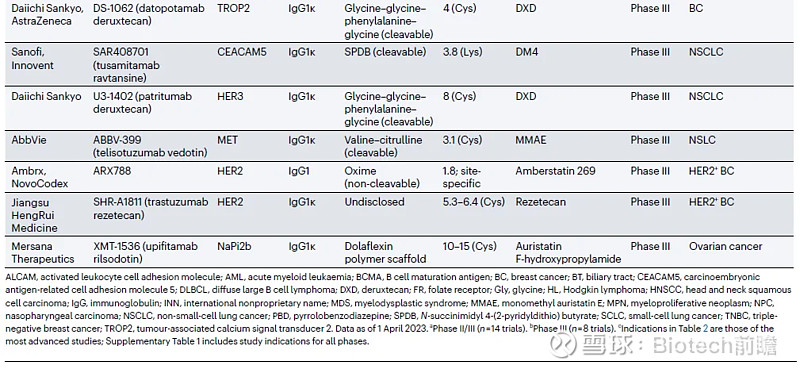
企业赞助的中期至后期ADC临床研究汇总