ALG-000184 是由 Aligos Therapeutics 开发用于慢性乙型肝炎治疗的一款泛基因型 II 型衣壳组装调节剂(CAM),是ALG-001075的前药。
目前 ALG-000184 正处在 Phase 1期(ALG-000184-201研究)期临床试验阶段,研究是一项多部分、双盲、随机、安慰剂对照研究,旨在评估健康志愿者和慢乙肝患者中单次和多次递增剂量 ALG-000184 的安全性、药代动力学和抗病毒活性。
在第 1 部分和第 2 部分中,健康志愿者对单剂和多剂 ALG-000184 (7天用药)的耐受性良好。
第3部分是在未经治的 HBeAg阳性 (10, 100, 300 mg) 和阴性 (10, 50, 100 mg)慢性乙型肝炎患者中评估每日口服ALG-000184或安慰剂28天的安全性、药代动力学和抗病毒活性。结果发现其耐受性良好,PK良好。对降低HBV DNA, HBV RNA病毒指标该药是目前同类药物中最好的药物。在降低乙肝表面抗原(HBsAg)表现上该药也是目前同类药物中最好的药物,在5名患者中观察到最高达 0.8 log10 IU/mL 的降低。
ALG-000184-201研究的第四部分以及更多的研究(用药小于等于48周,联用或不联用恩替卡韦)正在进行中。
第4部分评估了未经治HBeAg阳性慢性HBV感染或慢性乙型肝炎患者(N≤15/队列,12名用药患者:3名安慰剂)每日服用ALG-000184或安慰剂联合恩替卡韦12-48周的安全性、耐受性和抗病毒活性。
第四部分的队列1纳入了11名受试者,目前该研究已经完成,采用两种用药方案:1)ALG-000184 100 mg + ETV x 24周,随访8周;2)安慰剂+恩替卡韦(12周)随后 ALG-000184 100mg + ETV x 12周,随访8周。
队列1 (100 mg ALG-00184 + ETV x 24 周):N=4 ,100 mg ALG-000184 + ETV x ~24 周: HBV DNA 降低大于 6 log10 IU/mL;100 mg ALG-000184 + ETV 相较于恩替卡韦单药导致额外约 2 log10 IU/mL HBV DNA 降低。
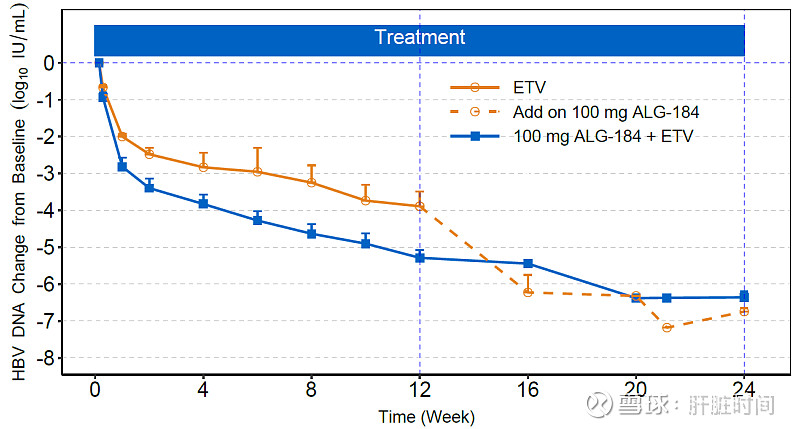
N=4,100 mg ALG-000184 + ETV x ~24周; 3/4 名患者 HBsAg 降低大于 0.4 log10 IU/mL,最高降低~0.7 log10 IU/mL 。2 名安慰剂患者转换到 100 mg ALG-000184 + ETV 方案后观察到 HBsAg 降低趋势。
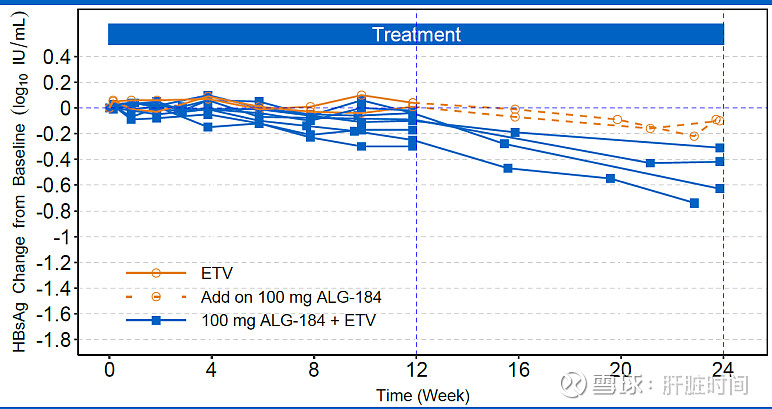
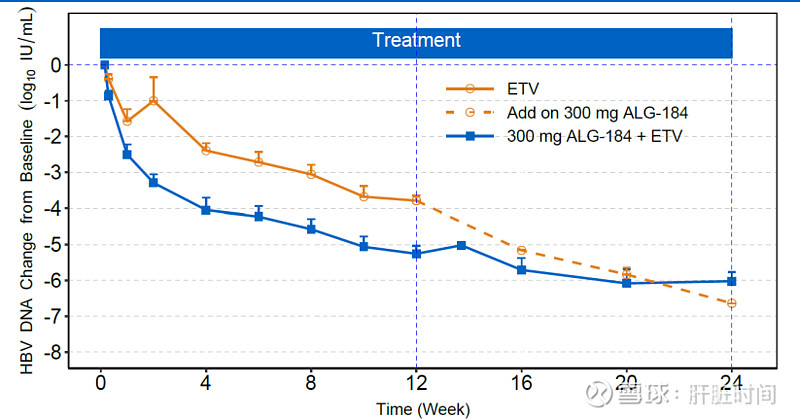
第四部分队列2纳入了15名受试者,招募已经完成,用药工作尚未全部完成。采用两种用药方案:1)ALG-000184 300 mg + ETV x 48周,随访8周;2)安慰剂+恩替卡韦(12周)随后 ALG-000184 300mg + ETV x 48周,随访8周。
队列2(300 mg ALG-00184 + ETV x 48 周)(接受ALG-00184用药大于等于12周):N=7,300 mg ALG-000184 + ETV x ≥12 周,在第 24周: 受试者有大于等于 6 log10 IU/mL 的 HBV DNA 降低,2 名受试者已经处在检测下限。
300 mg ALG-000184 + ETV 用药时间 ≥12 周(N=7): 6 /7 名受试者HBsAg 至少降低~0.4 log10 IU/mL;用药时间≥24 周 (N=5): 4/7 名受试者 HBsAg 降低≥1 log10 IU/mL;在第28周观察到的最大降幅为 1.65 log10 IU/mL。
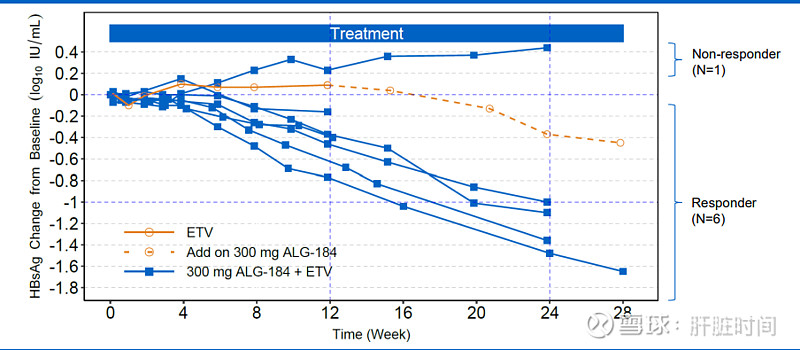
HBsAg变化情况 VS 药代动力学(第24周)
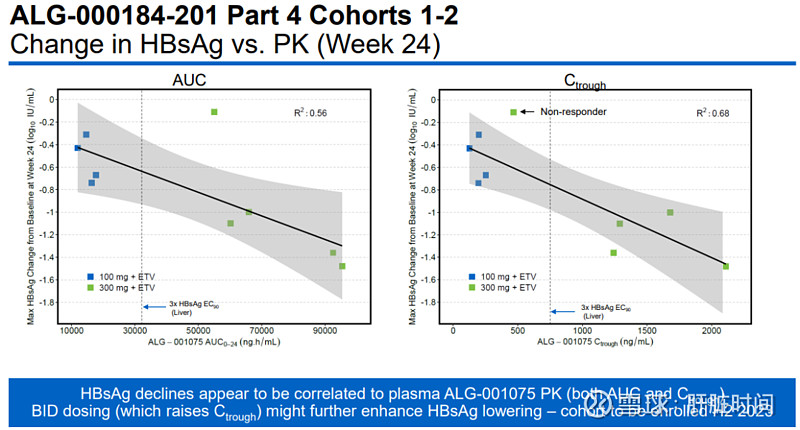
ALG-000184-201研究第四部分中期数据归纳:ALG-000184的安全性和耐受性良好。联合恩替卡韦具有显著的抗病毒活性,其中ALG-000184 + ETV抗病毒活性显著强于恩替卡韦单药,4/5名患者用药时间长于或等于24周后拥有大于等于 1.0 log10 IU/mL的 HBsAg 降低,截止目前观察到最高的 HBsAg 降低是来自300 mg ALG-000184 + ETV x 28周用药方案的一名患者,降幅为1.65 log10 IU/mL。
更长时间的用药方案和其他队列(每日两次)将会更进一步的定义 ALG-000184 联合或不联合 ETV 的安全性、耐受性、药代动力学和抗病毒活性。
貌似 ALG-000184 目前拥有着同类药物最佳的临床表现,与其他抗病毒药物和免疫调节药物如PD-L1抑制剂联合应用或具备增强慢乙肝功能性治愈的潜能。