▎医药观澜/报道
近日,再鼎医药宣布,一款名为Optune的肿瘤电场治疗产品获得中国国家药监局(NMPA)创新医疗器械资格认定。若进展顺利,中国将有望迎来首款肿瘤电场疗法!肿瘤电场治疗的技术源自于Novocure公司,其原理是用调整到特定频率的交替电场靶向肿瘤细胞,来破坏肿瘤细胞分裂,抑制肿瘤生长并导致肿瘤细胞死亡。2018年9月,再鼎医药从Novocure公司获得在大中华区推广Optune的独家许可。
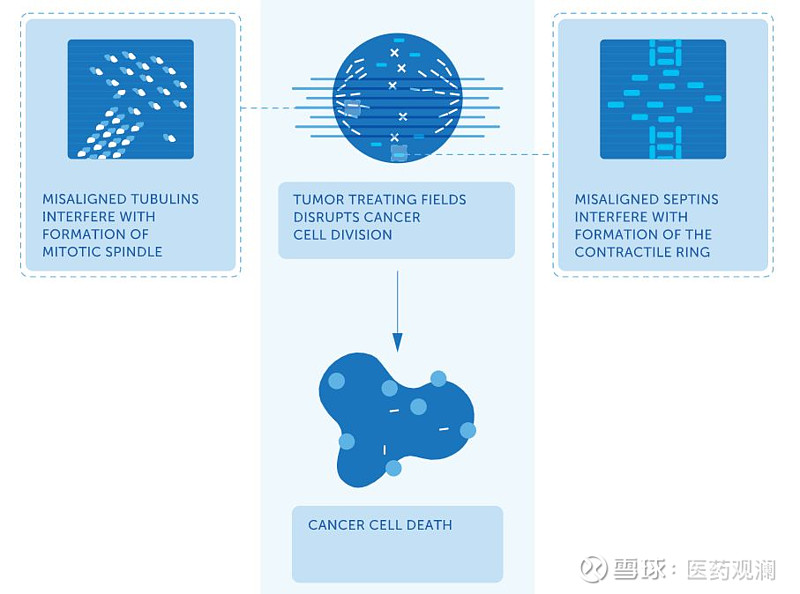
▲肿瘤电场治疗作用机理(图片来源:Novocure公司官网)
目前,这款肿瘤电场治疗产品已在美国、欧盟、日本、中国香港等国家和地区上市,获批适应症有胶质母细胞瘤(GBM)和恶性胸膜间皮瘤(MPM)。此外,该疗法针对四种实体肿瘤适应症的研究已进入晚期临床开发阶段,包括非小细胞肺癌(NSCLC)、脑转移、胰腺癌和卵巢癌。
1.胶质母细胞瘤
Novocure公司此前进行的临床3期关键性试验结果表明:相比单独使用替莫唑胺治疗,肿瘤电场治疗Optune与替莫唑胺联合使用治疗新发胶质母细胞瘤,患者的五年总生存率(OS)由5%提升至13%,提高超过两倍,患者的中位总生存期由16个月延长至20.9个月。此外,在这一试验中,Optune表现出的效果与依从性密切相关,高依从性的患者中位生存期显著延长。当患者每天穿戴超过22小时,五年生存率可提升至29.3%。
2.恶性胸膜间皮瘤
在一项名为STELLAR的临床试验中,80名MPM患者接受了肿瘤电场治疗产品NovoTTF-100L与化疗构成的组合疗法的一线治疗。试验结果表明,接受组合疗法治疗的患者中位总生存期为18.2个月,62%的患者在接受组合疗法后1年时仍然活着。在至少接受过一次CT扫描随访检查的患者中,疾病控制率达到97%,其中部分缓解率为40%。
基于这项结果,美国FDA于今年5月批准了NovoTTF-100L系统上市,与培美曲塞和铂基化疗联用,一线治疗无法切除的局部晚期,或转移性恶性胸膜间皮瘤。这是15年来FDA批准的第一款治疗MPM的新疗法。此前,培美曲塞与顺铂构成的组合疗法是治疗无法切除的MPM的唯一获批疗法。
3.胰腺癌
一项针对晚期胰腺癌的2期临床试验,招募了20位没有化疗或者放疗过的晚期胰腺癌患者,采用肿瘤电场治疗联合紫杉醇和吉西他滨进行治疗。结果显示,这20位患者的中位无进展生存期达到12.7个月,而紫杉醇和吉西他滨联合吉西他滨的历史数据是5.5个月,表明肿瘤电场治疗可能会让患者受益。

去年8月,Novocure公司与US Oncology Research公司联合宣布将合作推进名为PANOVA-3的关键性临床3期试验的进展。PANOVA-3将检测肿瘤电场治疗与蛋白结合型紫杉醇和吉西他滨这两种药物构成的组合疗法,在治疗无法切除的局部晚期胰腺癌患者时的疗效。
4.卵巢癌
在2018年ASCO年会上,一项肿瘤电场治疗与标准化疗组合治疗复发性卵巢癌患者的临床2期试验结果亮相。试验中,30名复发性卵巢癌患者接受了肿瘤电场治疗与紫杉醇构成的组合疗法的治疗。结果显示,接受组合疗法治疗的患者的平均PFS为8.9个月,而历史性对照的紫杉醇单一疗法组的PFS为3.9个月。截止到公布结果时,患者群的平均1年存活率为61%。而安全性结果表明这一组合疗法有良好的耐受性和安全性,能够作为一线疗法治疗复发性卵巢癌患者。
5.非小细胞肺癌
在Clinicaltrials网站上,登记了一项肿瘤电场治疗用于非小细胞肺癌患者的关键性3期临床试验。此前,一项发表在2010年欧洲医学肿瘤协会(ESMO)上的2期临床数据显示,对于先前化疗失败的患有局部晚期和转移性的NSCLC(IIIb-IV期)患者,接受电场疗法联合培美曲塞治疗组相比单独培美曲塞治疗平均存活时间为13.8vs8.3个月;联合治疗一年生存率为57%(vs30%),且无进展的存活时间增加了一倍多,达到了22-28周(vs12周)。唯一报告的不良反应是在治疗位轻微到中度的皮肤刺激。
此外,该网站还登记了一项研究电场疗法治疗NSCLC脑转移的3期临床试验,以及多项该疗法针对肝癌的早期试验。根据Novocure公司官网,肿瘤电场治疗可以在18种不同的实体肿瘤中具有抗有丝分裂作用,包括一些极具侵袭性的癌症。
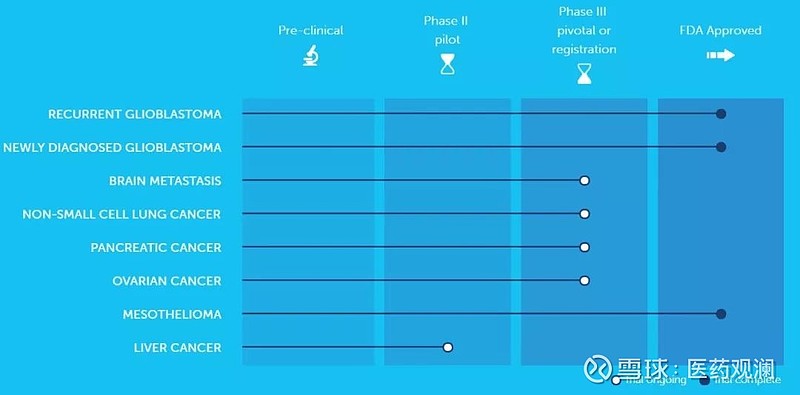
▲Novocure公司电场治疗在研管线(图片来源:Novocure公司官网)
肿瘤电场治疗在中国
去年9月,再鼎医药从Novocure公司获得在大中华区推广Optune的独家许可。除胶质母细胞瘤(GBM)外,双方还将合作开展肿瘤电场治疗用于多种实体肿瘤适应症的研发项目。包括正在进行的针对非小细胞肺癌和胰腺癌的3期临床,及即将启动的卵巢癌的3期临床试验。除此之外,再鼎医药还将在中国开展针对胃癌的2期临床试验。

在再鼎医药的推动下,Optune在去年底正式登陆中国香港,用于多形性胶质母细胞瘤。香港成为继美国,欧洲和日本之后第四个上市该治疗方案的市场。目前,Optune尚未获准进入中国大陆市场,但该技术已在2015年被纳入《中国中枢神经系统胶质瘤诊断与治疗指南》。2018年12月,肿瘤电场治疗又被《脑胶质瘤诊疗规范(2018版)》推荐用于新发和复发GBM的治疗。
创新医疗器械特别审查程序是中国国家药监局为加速医疗器械创新发展而制定的特别审查通道。此次Optune获得创新医疗器械资格,无疑将缩短审批时间和加快审批流程,进而加速进入患者手中。根据再鼎医药公告,替莫唑胺(TMZ)是目前中国唯一批准用于治疗新发GBM的药物,Optune有望成为第二个获批用于这一疾病的疗法。此外,一些中国国产化的电场治疗设备正在加紧研发,据悉已有同类产品获得多家医院及神外专家的支持。
欢迎扫码关注“医药观澜”微信公众号,了解更多中国医药创新动态。
参考资料:
[1]FDA Approves the NovoTTF-100LTM System in Combination with Chemotherapy for the Treatment of Malignant Pleural Mesothelioma. Retrieved May 23, 2019, from 网页链接
[2]Novocure and US Oncology Research Announce Collaboration on PANOVA-3 Trial for Patients with Advanced Pancreatic Cancer. Retrieved Aug 15, 2018, from 网页链接
[3]Novocure 公司和再鼎医药就肿瘤电场治疗(TTF)在大中华区独家商业许可及全球战略开发合作达成协议. Retrieved Sep 12, 2018, from 网页链接
[4]国家药品监督管理局授予Optune创新医疗器械资格认定. Retrieved Aug 12, 2019, from 网页链接
[5]肿瘤电场治疗在港上市,胶质母细胞瘤迎十年来首个突破性疗法2019年2月28日网页链接