日前,Acumen Pharmaceuticals公布了靶向毒性可溶性β淀粉样蛋白寡聚体(AβOs)的单克隆抗体ACU193的首个人体临床试验结果。结果显示,试验达到主要和次要目标,证明了ACU193的作用机制和安全性。在早期阿尔茨海默病(AD)患者中,ACU193剂量依赖性迅速降低患者的淀粉样蛋白斑块水平。

阿尔茨海默病是老年人中最常见的神经退行性疾病。在患者症状开始前20年,其脑部便出现复杂的变化,最终造成脑细胞死亡或连接丧失。淀粉样蛋白沉积是患者大脑的标志性特征,靶向淀粉样蛋白是阿尔茨海默病新药开发的重要方向之一。随着近年来两款抗淀粉样蛋白抗体疗法获得FDA的批准,这一研发策略也受到广泛关注。
ACU193是一种针对可溶性AβOs开发的选择性人源化单克隆抗体。Acumen认为,相比于Aβ淀粉样蛋白单体和淀粉样蛋白斑块,AβOs是毒性和致病性最强的一种形式。可溶性的AβOs已被观察到能与神经元结合,抑制突触功能并诱导神经变性,是一种强效的神经毒素。ACU193能够结合AβOs,由于其独特的结合特性,ACU193有可能在产生淀粉样蛋白相关成像异常(ARIA,一种抗体疗法产生的常见主要副作用)风险较低的情况下提供治疗益处,因为ACU193可以在不直接靶向淀粉样斑块的情况下阻断AβOs的毒性作用。
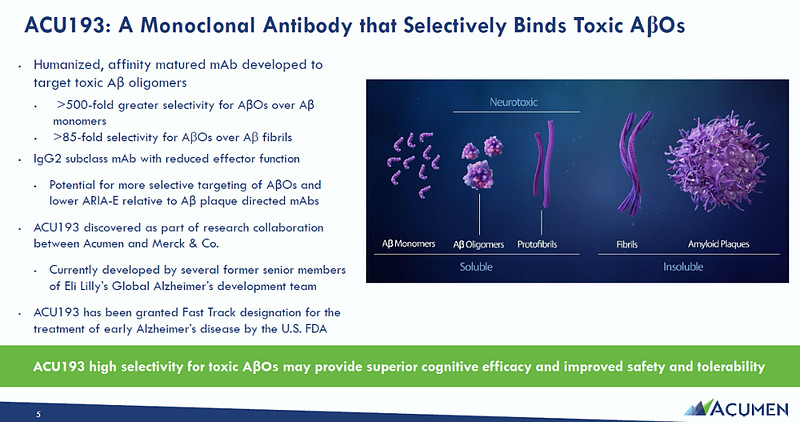
▲ACU193的作用机理(图片来源:Acumen公司官网)
在这项随机双盲,含安慰剂对照的1期临床试验中,早期AD患者接受不同剂量的ACU193或安慰剂的治疗。试验的主要目标为安全性,其它探索性目标包括药代动力学,与靶点的相互作用,以及大脑淀粉样蛋白沉积检测等等。
试验结果显示,ACU193表现出良好的耐受性和安全性特征,达到试验的主要目标。最常见的治疗后出现不良事件为ARIA,总体来说10.4%的患者出现ARIA-E(意味着大脑某个或多个区域因为ARIA出现暂时性肿胀)。出现症状的AIRA-E比例为2.1%。
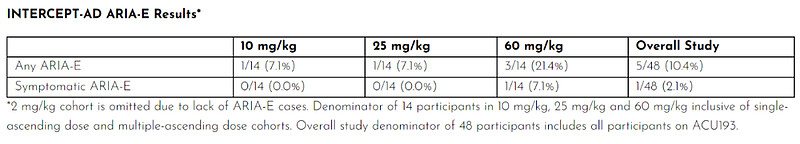
▲ACU193的ARIA-E数据(图片来源:Acumen公司官网)
此外,接受治疗6-12周后,大脑淀粉样蛋白PET扫描结果显示,接受较高剂量ACU193治疗的患者淀粉样蛋白斑块水平显著降低。这一降低幅度与已经获得FDA完全批准的抗淀粉样蛋白抗体相似。
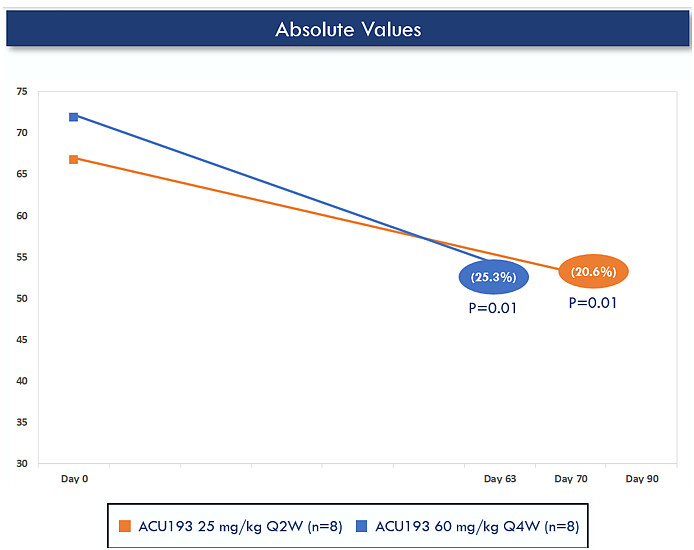
▲ACU193显著降低大脑淀粉样蛋白斑块水平(图片来源:参考资料[3])
试验结果同时显示,ACU193的药代动力学特征支持每月一次给药的用药方案。
基于这些积极结果,Acumen今日宣布将募集1.3亿美元资金,并将与监管机构进行讨论,决定启动2/3期临床研究的时间线。
@药明康德 内容团队编辑
本文来自药明康德内容团队,欢迎转发,谢绝转载到其他平台。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
⤵️喜欢我们的内容,欢迎关注@药明在线 ,或者点赞、分享给其他读者吧!