3月21日,BioNTech和OncoC4公司联合宣布,双方达成研发合作和许可协议,共同开发和商业化OncoC4公司的新一代抗CTLA-4单克隆抗体候选疗法ONC-392,作为单药疗法或组合疗法的一员,治疗多种实体瘤适应症。

CTLA-4通过多种不同机制抑制免疫细胞的活性。OncoC4公司的ONC-392的目标是清除肿瘤微环境中的免疫抑制性调节性T细胞(Tregs),同时不影响健康组织中的Tregs。它的潜在差异化安全性特征可能导致在临床试验中完成更为有效的给药方案,从而产生更好的肿瘤杀伤效果。去年,它已经获得美国FDA授予的快速通道资格,作为单药治疗先前接受过抗PD-1/L1疗法后疾病进展的转移性非小细胞肺癌(NSCLC)患者。昂科免疫拥有该药的大中华区权益。
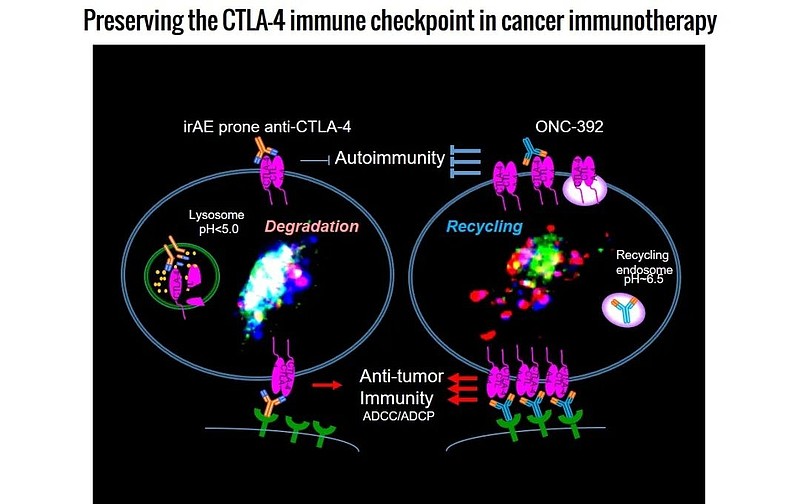
▲ONC-392的作用机制(图片来源:OncoC4官网)
根据协议,OncoC4将获得2亿美元前期付款,并且有资格获得开发、监管和商业化里程碑付款。BioNTech和OncoC4将联合开发ONC-392作为单药,或与抗PD-1/PD-L1抗体联用,治疗一系列包括NSCLC在内的实体瘤适应症。BioNTech将独自负责开发ONC-392与抗PD-1药物以外疗法构成的组合疗法。
“虽然已经成为靶点十多年,我们认为靶向CTLA-4仍未在抗癌免疫疗法中发挥全部的潜力。”BioNTech首席执行官Ugur Sahin博士说,“OncoC4的数据显示ONC-392在多种不同肿瘤类型中具有差异化的安全性特征和可喜的临床活性。我们相信不论作为单药,或与我们的个体化免疫疗法联用,这款抗体都是我们免疫肿瘤学管线有价值的补充。”
“由于其独特的作用机制,我们认为ONC-392有可能拓宽CTLA-4靶向免疫疗法的触达群体。”OncoC4的联合创始人、首席执行官兼首席科学官刘阳博士说,“我们非常期待与BioNTech携手合作,开发ONC-392用于医疗需求未得到满足的癌症适应症。”
参考资料:
[1] BioNTech and OncoC4 Announce Strategic Collaboration to Co-Develop and Commercialize Novel Checkpoint Antibody in Multiple Solid Tumor Indications. Retrieved March 20, 2023, from 网页链接
@药明康德 内容团队报道
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发,谢绝媒体或机构未经授权以任何形式转载至其他平台。