
撰文丨不器
编辑丨于靖
经历了长时间的等待,吉利德开发的长效HIV新药试验终于迎来重启。
根据公告,5月16日,FDA解除了Lenacapavir的相关临床搁置。这意味着,吉利德可以继续推进Lenacapavir用于HIV治疗和HIV暴露前预防(PrEP)的研究。
去年12月,吉利德获悉,因担心药物溶液与硼硅酸盐玻璃小瓶之间的相容性问题,Lenacapavir多达10项临床试验被FDA叫停。FDA声称,药物与容器有可能发生相互作用,进而产生亚可见的玻璃微粒。
受此影响,当时所有Lenacapavir研究均不允许对研究参与者进行筛选和入组,也不允许注射Lenacapavir。从范围来看,这次暂停涵盖开发早期到后期临床,包括2项III期试验。不过,监测参与者和对照组参与者的给药的研究,包括Lenacapavir的口服剂型,得以继续开展。
更早前的2021年6月,吉利德向FDA递交Lenacapavir的上市申请,用于治疗接受过多种疗法且对多种药物产生耐药的HIV-1感染者。
这次NDA基于一项II/III期临床(CAPELLA)的积极数据。结果显示,在14天的功能性单药治疗结束时,Lenacapavir组有88%(n=21/24)的患者HIV-1病毒载量至少降低了0.5log10拷贝/ml,远超对照组中达到相同水平的17%这一患者占比(n=2/12)。另外,Lenacapavir组病毒载量下降幅度相较对照组更为显著。
在正式递交NDA前,吉利德对CAPELLA进行一次更新,发现自第一次皮下注射Lenacapavir后的第26周,73%的患者(n=19/26)达到无法检测的病毒载量(<50拷贝/mL)。
但今年3月,FDA还是对Lenacapavir的上市申请发出CRL。FDA的担忧与叫停相关临床时如出一辙。尽管Lenacapavir在申请上市后获得了优先审查,监管机构也并未放松对CMC等问题的要求。
事实上,CMC一直犹如悬在药企头顶的达摩克里斯之剑。2021年,FDA共批准60款新药,仅次于2018年的65项批准,可是CRL的数量也在急剧增长——从2018年的9份,增长至2021年的21份。2022年尚未过半,在FDA处理的新药申请中,已有47.1%收到CRL,其中一半与CMC有关。
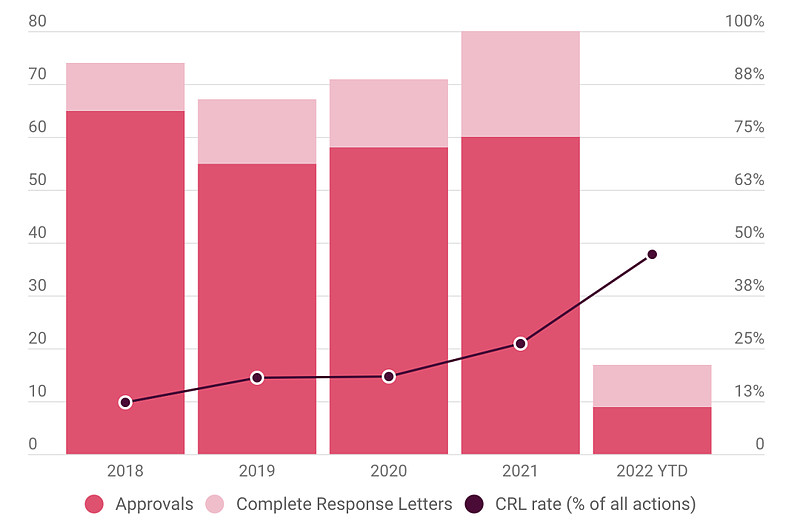
FDA发言人曾表示,CRL的增长并非由于对CMC流程的审核更严格,而是与应用程序类型和复杂性有关。
5月上旬,FDA专门发布了新的指导草案,详细说明如何评估质量风险、不确定性来源和可能的缓解策略。除了一些罕见情况,比如药品的收益大于剩余风险,此时可能会被容许批准后进行质量提交;否则,在大多数情况下,假设药品具有未解决的质量问题,FDA不会批准上市申请。
既往资料指示了,CRL会将产品进入市场的时间平均推迟14个月。Lenacapavir的NDA被拒绝后,Baird的分析师预测,这可能造成吉利德推出该产品的时间点延迟一年。
值得注意的是,吉利德向FDA提交的Lenacapavir包括注射和口服两种剂型。吉利德发言人Brian Plummer回应媒体时说,虽然容器问题针对注射溶液,但口服药片是作为治疗开始的一部分。因此,Lenacapavir口服剂的批准也要取决于Lenacapavir注射剂的批准。
这对于吉利德而言确实是个挫折。Lenacapavir一度是吉利德最为重要的项目之一,作为一种衣壳抑制剂,该药主要通过干扰病毒生命周期的多个重要步骤来抑制HIV-1复制,涉及衣壳介导的HIV-1前病毒DNA的摄取、病毒组装和释放以及衣壳核心的形成。
换言之,靶向衣壳的特点,让Lenacapavir不会与目前已批准的任何抗逆转录病毒疗法(ART)产生重叠耐药性。为此,2019年5月,FDA授予Lenacapavir与其他抗逆转录病毒药物联合治疗经治后产生多重耐药患者的HIV-1感染突破性疗法认定。
如果Lenacapavir获批,它将成为首个衣壳抑制剂,也是一年只需要给两次的HIV-1疗法,远比市面可能用的药物频率低得多。
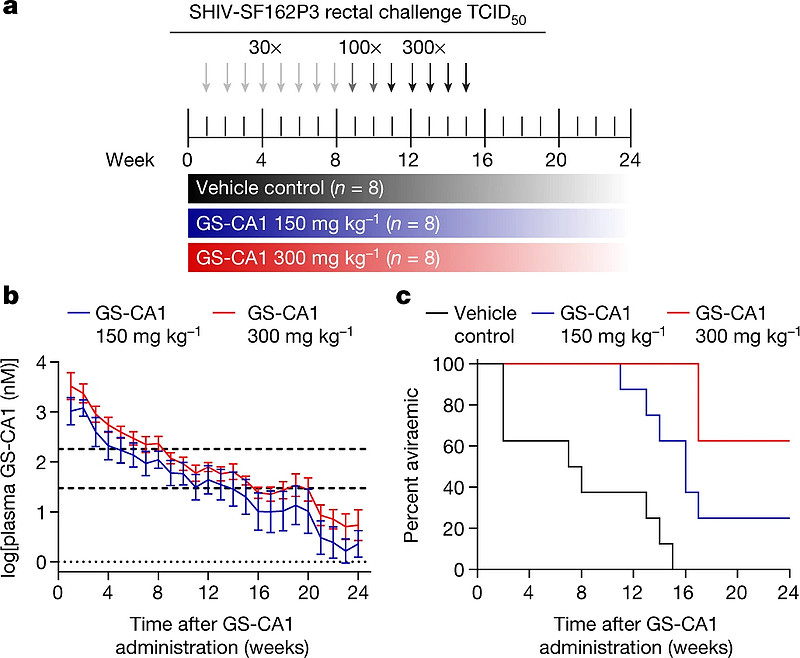
目前,至少业界在理论上看到了这样的新可能。吉利德还对衣壳做了其他探索。援引去年底哈佛大学医学院和吉利德的研究人员在Nature发表的一篇成果,针对HIV病毒衣壳的抑制剂GS-CA1,能够实现一次注射提供长期保护,避免恒河猴感染与HIV相关的猴免疫缺陷病毒(SHIV)。
研究人员指出,GS-CA1在非人灵长动物中的治疗潜力,有助于指导针对HIV衣壳抑制剂的进一步研究,以确定单次剂量能提供多久的保护力。
RBC Capital Markets的分析师也对吉利德的尝试表示看好。虽然Lenacapavir面临CMC问题,但由于每六个月进行一次给药的优势,吉利德有机会快速纠正其容器的问题,从而避免给许多患者提供替代治疗。
收到CRL后,吉利德向FDA提供使用不同类型小瓶(铝硅酸盐玻璃)的计划和数据。经过审查,FDA最终取消了Lenacapavir近半年的临床暂停。吉利德透露,其将与研究现场的调查人员合作,尽快全面恢复Lenacapavir开发项目。
3月递交Lenacapavir上市申请针对接受过大量预处理的HIV患者,但在此之外,吉利德还开展了Lenacapavir与其他疗法联合用于感染已经被抑制的患者的试验,以及评估Lenacapavir作为PrEP用途的研究——该数据预计在2024年发布。
顺利的话,Lenacapavir更多适应症的获批,使RBC Capital Markets的分析师相信,该药的最高年销售额可能超过40亿美元。
更重要的地方在于,吉利德需要早日摆脱长期依赖单品背后的专利悬崖,以及并购“消化不良”的窘境。2021年财报中,HIV药物Biktarvy以86.24亿美元位列创收单品第一,紧随其后的是卖出55.65亿美元的COVID-19药物Veklury。
即使吉利德在4月重申了进军抗肿瘤领域的愿景,现实来看,这份蓝图并不能把它从燃眉之急中解救出来。吉利德希望,到2030年,它将有三分之一的收入来自抗肿瘤管线,而在最新的年度财报中,这一板块才首次突破10亿美元大关。
焦头烂额的吉利德还有“买买买”后的一地鸡毛需要处理。3月,根据提交给新泽西州Worker Adjustment and Retraining Notification (WARN)的一份文件,吉利德计划在4月、9月和12月,分三批解雇所收购Immunomedics的前总部Morris Plains的114名员工。
可以预期,在华丽转身之前,HIV药物仍是吉利德的创收支柱之一。而能否最终将Lenacapavir推向市场,或许关系着吉利德有无机会在与GSK、强生、默沙东等同行的较量中稳住HIV基本盘。
主要参考资料:
1. FDA Lifts Clinical Hold on Investigational Lenacapavir for the Treatment and Prevention of HIV;Gilead
2. Gilead, having resolved manufacturing issues, forges ahead with HIV drug;BioPharma Dive
3. Biotech更易收到FDA的“死亡回函”?CMC问题凸显关键性;同写意
4. Gilead’s Investigational Lenacapavir Demonstrates Sustained Long-Acting Efficacy Through Week 26 in Data Presented at CROI;Gilead
5. Long-acting capsid inhibitor protects macaques from repeat SHIV challenges;Nature
6. 2030年之前成为抗肿瘤巨头,吉利德的“野望”如何照亮现实?;同写意
7. 一“裁”了之:吉利德、渤健等药企是如何深陷业绩风波的?;同写意