3月7日,国家知识产权局针对诺和诺德的一篇关于利拉鲁肽的制备方法专利ZL2015105721241发出无效宣告请求审查决定书,宣告专利权全部无效。无效宣告请求人为杭州中美华东制药有限公司。
2023年度中国医药专利无效报告(附详细清单)网页链接
利拉鲁肽注射液药品信息网页链接

利拉鲁肽为人胰高血糖素样肽-1(GLP-1)受体激动剂,与人GLP-1具有97%的序列同源性,其糖尿病适应症最早于2009年6月29日获EMA批准,2010年1月25日获FDA批准,商品名Victoza。2011年1月17日,在中国获批上市,商品名为“诺和力”,2017年8月,利拉鲁肽进入国家医保目录,奠定了其在中国的市场基础。
2017年8月,FDA批准Victoza增加“用于降低伴有心血管疾病的2型糖尿病患者重大心血管不良事件发病风险”的适应证,使利拉鲁肽成为首个在降血糖的同时还能降低心血管风险的已上市GLP-1受体激动剂。2014年12月,FDA批准利拉鲁肽注射液用于减肥,商品名Saxenda,目前该适应症尚未在国内获批。
根据医药魔方PharmaGO数据库显示,利拉鲁肽在中国的化合物专利CN100569798C已于2017年8月22日到期,目前国内市场开始了一波利拉鲁肽仿制药的研发热潮,进度最快的是华东医药和通化东宝,其利拉鲁肽类似物都已于2023年获批上市,此外,双鹭药业、圣诺生物、联邦制药、正大天晴等公司的利拉鲁肽类似物也在申请上市过程中。

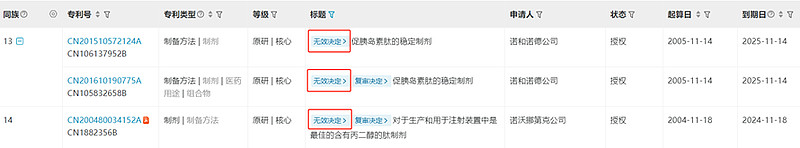
本次无效宣告请求人华东医药是国内首家利拉鲁肽在降糖和减肥两大适应症上都获批的企业,其对利拉鲁肽的专利围猎由来已久,本次无效涉及的专利为利拉鲁肽的制备方法专利,最终以不具备创造性为由被宣告专利权全部无效;其同族专利ZL2016101907759在2022年9月也同样以不具备创造性为由被宣告专利权全部无效;
华东医药的关联公司杭州九源基因曾在2015年对利拉鲁肽的制剂专利ZL2004800341528发起专利无效宣告请求,该专利被宣告专利权全部无效,专利权人不服无效决定提出行政诉讼,北京知产法院一审判决驳回了原告诺和诺德公司的诉讼请求,诺和诺德公司针对该判决继续提出上诉,终审判决维持原判。
虽然本次无效决定得到了仍不利于专利权人的结果,但是最终结果可能还会发生变化。
$诺和诺德(NVO)$ $礼来(LLY)$ $华东医药(SZ000963)$
更多相关报告和医药资讯持续更新,请持续医药魔方ByDrug 网页链接