6月28日,药监局官网显示,齐鲁制药1类创新药伊鲁阿克片获批上市,用于治疗既往接受过克唑替尼治疗后疾病进展或对克唑替尼不耐受的ALK突变阳性局部晚期或转移性非小细胞肺癌(NSCLC)患者。伊鲁阿克是齐鲁制药首个获批上市的创新药。

伊鲁阿克(研发代号为WX-0593)是一款由齐鲁自主研发的新型ALK/ROS1抑制剂,可以抑制不同融合类型的野生型以及ALK抑制剂耐药突变的ALK激酶活性,同时可有效抑制不同融合类型ROS1激酶的活性。研究显示,WX-0593在ALK阳性或ROS1阳性NSCLC中具有抗肿瘤活性,安全性可接受,180mg之内的剂量方案都有非常好的药代动力学参数和安全性。
此次获批上市是基于一项单臂、多中心的II期临床研究,旨在评估伊鲁阿克用于既往接受过克唑替尼治疗的ALK突变阳性晚期非小细胞肺癌的疗效与安全性。该试验共纳入146例患者,中位随访时间为9.3个月;90例患者有脑转移,其中41例有可测量的颅内病灶,20例患者既往接受过脑部放疗;56例患者既往接受过化疗。
该试验的主要终点是独立评审委员会(IRC)根据RECIST v1.1评估的客观缓解率(ORR);次要终点包括疾病控制率(DCR)、缓解持续时间(DOR)、无进展生存期(PFS)、疾病进展时间(TTP)和安全性。
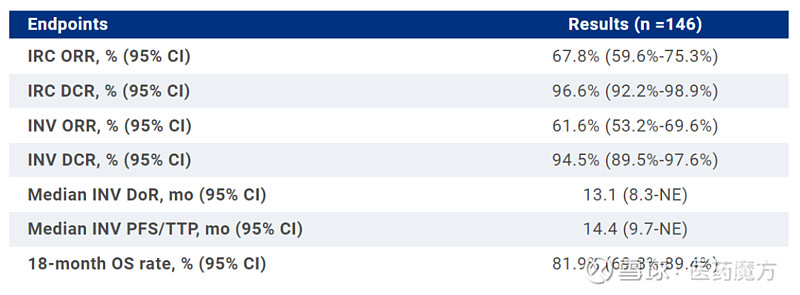
结果显示,由IRC评估的伊鲁阿克治疗组的ORR为67.8%,DCR为96.6%。由研究者评估的伊鲁阿克治疗组的ORR为61.6%,DCR为94.5%,中位DoR为13.1个月,中位PFS/TTP为14.4个月,18个月总生存率为81.9%。
亚组分析发现,IRC评估的无脑转移(79% vs 61%)以及既往接受过脑放疗(66% vs 45%)患者的ORR略微高;既往接受过化疗或未化疗的患者也略高(71% vs 66%);可测量的颅内病变患者的iORR(颅内客观缓解率)为63%;OS数据尚不成熟。
入组患者中有134例(91.8%)发生了治疗相关的不良事件,最常见的是天冬氨酸转氨酶、丙氨酸转氨酶以及血肌酸磷酸激酶升高。
值得一提的是,今年4月初,伊鲁阿克片用于ROS1阳性NSCLC的新适应症上市申请也获药监局受理。此前针对该适应症公布的研究结果显示,在50例既往未使用过克唑替尼的患者中,伊鲁阿克的ORR为74%(37/50),DCR为96%(48/50)。中位缓解持续时间为14.51个月。伊鲁阿克在克唑替尼耐药的患者中也显示出疗效信号,9例患者中2例达到部分缓解,6个月的缓解率为100%。
据医药魔方数据库,截至目前,国内已上市8款ALK抑制剂类药物获批,除了伊鲁阿克片外,辉瑞的克唑替尼、诺华/阿斯利康的塞瑞替尼、武田的布格替尼、罗氏的恩曲替尼、贝达药业的恩莎替尼、辉瑞/基石的洛拉替尼以及Chugai的阿来替尼均已获批上市。
据官方新闻稿,齐鲁制药共有129个产品通过一致性评价,其中51个为国内首家,妥妥的首仿大户。现如今,创新产品也陆续开花结果。除了率先出线的伊鲁阿克,齐鲁产品管线中还有50余款创新药,其中EGFR单抗QL1203、PD-1/CTLA-4组合抗体QL1706、莫奥珠单抗以及PD1单抗均进入III期临床阶段,另有多款处于I~II期。