2023年5月3日,GSK如期迎来了FDA对其RSV疫苗Arexvy的审批决定,FDA批准该款疫苗用于预防60岁及以上老年人因呼吸道合胞病毒(RSV)引起的下呼吸道疾病(LRTD)。这是世界上首款获得批准的针对老年人的RSV疫苗。GSK表示将于2023/24 RSV流感季节到来之前将这款疫苗推向市场。

2022年,辉瑞和GSK几乎同时宣布两家公司研发的RSV疫苗III期临床研究成功。2022年12月,RSV疫苗因取得重大进展入选SCIENCE年度《十大科学突破》。随着GSK的Arexvy获得批准,辉瑞的RSV疫苗也将于本月在美国迎来全球首批,这两款疫苗的上市也为人类这68年来为RSV艰辛探索的征途画上圆满句号。
60年沉浮,RSV新药的漫漫研发路
呼吸道合胞病毒(Respiratory syncytial virus,RSV)是一种副黏液病毒科肺炎病毒属的负单链RNA病毒,于1955年首次从患有呼吸道疾病的黑猩猩中分离出来[1]。1957年,科学家首次在患有严重下呼吸道疾病的婴儿体内也分离出了这种病毒[2,3]。从那时起,RSV已被证明是一种普遍存在的病原体,几乎所有2岁以下的儿童都会感染,并且有一半在此期间经历了两次感染[4]。
在全球范围内,RSV每年导致约300万名5岁以下儿童住院,约6万人在院内死亡[5]。而在美国,RSV是导致1岁以下婴儿住院的主要原因[6],且每年17.7万因RSV住院的老年人中,有1.4万人死亡[8]。
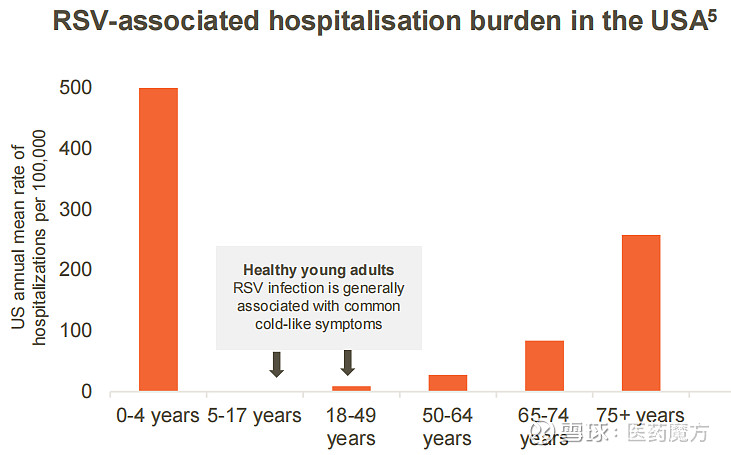
RSV导致的美国住院负担(来源:参考资料[8])
RSV造成的医疗负担不言而喻。事实上,自从这种病毒首次在人体内被发现开始,科学家就已经着手于疫苗的研发。在20世纪60年代,科学家基于F蛋白开发了一种FI-RSV疫苗[9],这款疫苗病毒由细胞培养产生,用福尔马林灭活,并与明矾混合作为佐剂[10]。但当他们在婴儿身上进行临床试验时,却以悲剧告终:两名婴儿死亡。德克萨斯大学奥斯汀分校的结构生物学家Jason McLellan说,起初,婴儿对疫苗的耐受性很好。但在接下来的感冒和流感季节,80%注射过疫苗的儿童随后感染了RSV,病情恶化者需住院治疗。相比之下,接种安慰剂后感染RSV的儿童中只有5%最终住院[11]。
这一失败一度使开发RSV疫苗的努力中断,后来经过科学家们的努力,试验失败背后的原因逐渐浮出了水面。RSV表面发现的F蛋白有助于将病毒和宿主细胞的细胞膜结合在一起,从而使病毒感染宿主细胞。F蛋白以两种形式存在:一种是高度稳定的融合后(postfusion)形式,另一种是不稳定的融合前(prefusion)形式。在感染期间,当病毒和宿主细胞聚集在一起时,这种蛋白质呈现prefusion形式,一旦感染发生,这种蛋白质就转变为更加稳定的postfusion形式[11]。
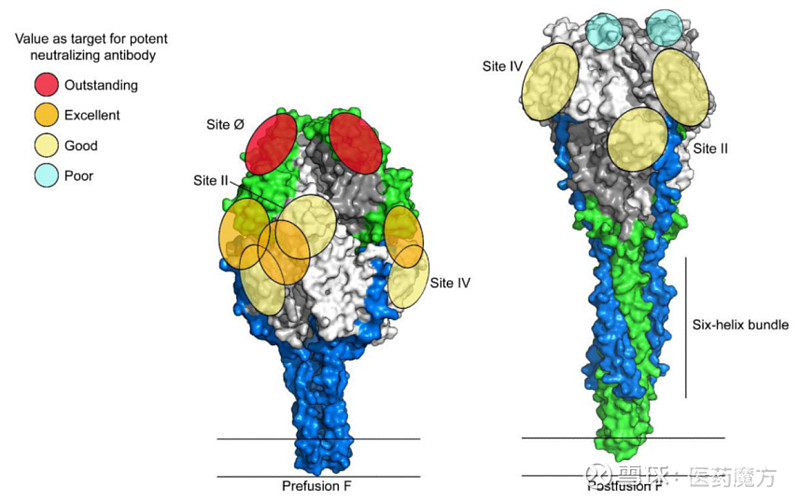
RSV F糖蛋白prefusion状态拥有更多的中和位点[12]
而FI-RSV疫苗主要产生F蛋白postfusion构象,而非prefusion构象。因此,该疫苗不仅不能保护血清阴性年轻婴儿免受RSV的感染,而且还会导致严重的加重性呼吸道疾病(ERD)[10]。而引起ERD的原因则是福尔马林介导的疫苗制备过程破坏了其中和表位[13]。
病毒颗粒通过福尔马林灭活处理成为FI-RSV时,传染性和F蛋白抗原性同时消失
(来源:参考资料[10])
相反地,prefusion F蛋白构象虽不稳定,但它是一种活跃的蛋白质,能诱导最强大的免疫反应,因此是制造有效疫苗所需要的[11]。
因FI-RSV引起的相关不良事件将RSV疫苗的开发推迟了几十年[14]。不过,经过探索,McLellan和一些合作者最终确定了prefusion F蛋白的结构,并研究出了使其变稳定的方法。这使得成功研发疫苗成为可能,也为潜在的基于抗体的疗法打开了大门[11]。
RSV疫苗三足鼎立之势即将形成
目前,全球在研RSV疫苗达60余款,GSK的重组蛋白疫苗已率先撞线,辉瑞的重组蛋白疫苗也呼之欲出;Moderna的RSV mRNA疫苗III期临床已达到主要终点,将在今年递交上市申请。GSK疫苗虽具有先发优势,不过谁能占据更大的市场份额仍然是个未知数。
GSK3844766A:更优的疗效
GSK是最先获得RSV疫苗振奋人心III期临床积极结果的企业。其开发的GSK3844766A由prefusion F糖蛋白(RSVPreF3)与GSK专有的佐剂组合而成。2022年6月10日,GSK宣布GSK3844766A用于预防60岁及以上人群RSV感染的关键III期试验(AReSVi 006)获得积极结果。这也是首个在60岁及以上人群中疗效显示出显著统计学和临床意义的RSV疫苗。
具体而言,GSK3844766A对RSV相关下呼吸道疾病(RSV-LRTD)总体保护效力为82.6%(96.95% CI, 57.9–94.1) ,对严重RSV相关下呼吸道疾病(至少有2种下呼吸道症状或体征)的保护效力为94.1%(95% CI, 62.4–99.9)。此外,在至少有一种基础病(如某些心肺和内分泌代谢疾病)的老年人中,GSK3844766A的保护效力为94.6% (95% CI, 65.9-99.9)。
安全性方面,GSK3844766A具有良好的耐受性和安全性。研究中报告的不良事件(AE)通常是轻度至中度且短暂的,最常见的AE是注射部位疼痛(60.9%)、疲劳(33.6%)、肌痛(28.9%)和头痛(27.2%)。
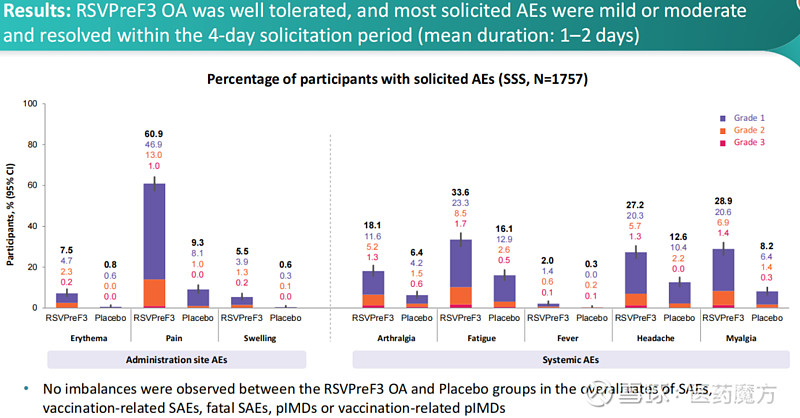
该临床数据已于今年2月在NEJM上发表[15]。在今年进行的FDA专家咨询委员会会议上,委员会成员以10:2投票结果认可RSVpre的安全性,以12:0投票结果认可其有效性,支持这款疫苗的批准。如今GSK已率先一步摘得疫苗研发领域这颗皇冠上的明珠。
GSK表示,另一项针对50-59岁成人(包括有潜在合并症)的临床试验结果预计将于2023年公布,而另外两项与流感疫苗联合接种试验的结果预计也将在2023年6月的免疫实践咨询委员会(ACIP)会议之前公布。
GSK同时开发了3款RSV疫苗,仅GSK3844766A获得了成功。GSK3389245A是一款腺病毒疫苗,适用于婴幼儿和成人,但GSK于2021年自愿停止了临床研究。GSK3888550A主要用于母体免疫,不过,2022年2月基于独立数据监测委员会(IDMC)常规安全评估观察结果,GSK宣布自愿暂停其用于母体免疫的III期GRACE试验入组和接种,同时暂停了另外两项在孕妇群体开展的临床试验。
PF-06928316:老年人、新生儿均有效
2022年8月25日,辉瑞宣布二价RSV候选疫苗RSVpreF疫苗(PF-06928316)用于预防60岁及以上人群RSV感染的III期RENOIR试验获得积极关键结果。
在中期分析(数据截止日期2022年7月14日)中,34284名受试者接种了RSVpreF疫苗(N=17215)或安慰剂(N=17069)。结果显示,该款疫苗对2种以上症状保护率为66.7%,对至少3种以上症状保护率为85.7%,对急性呼吸道疾病的保护率为62.1%。
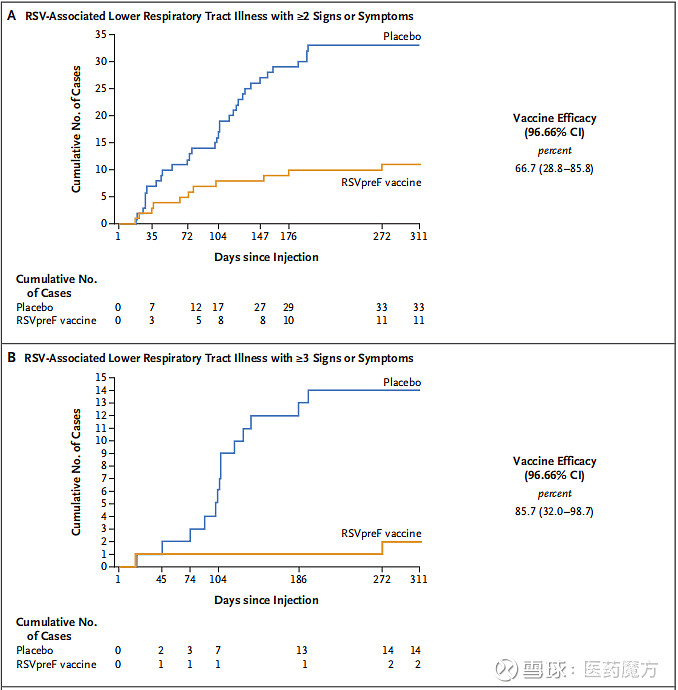
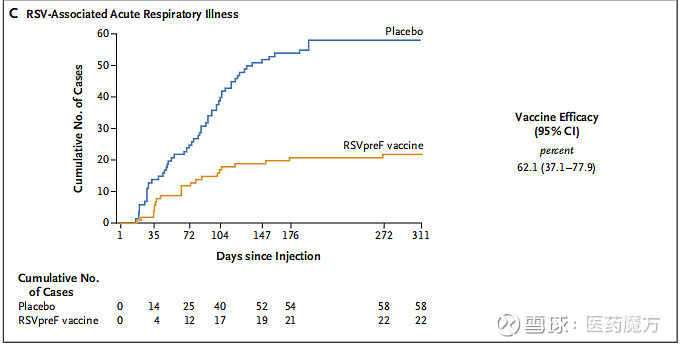
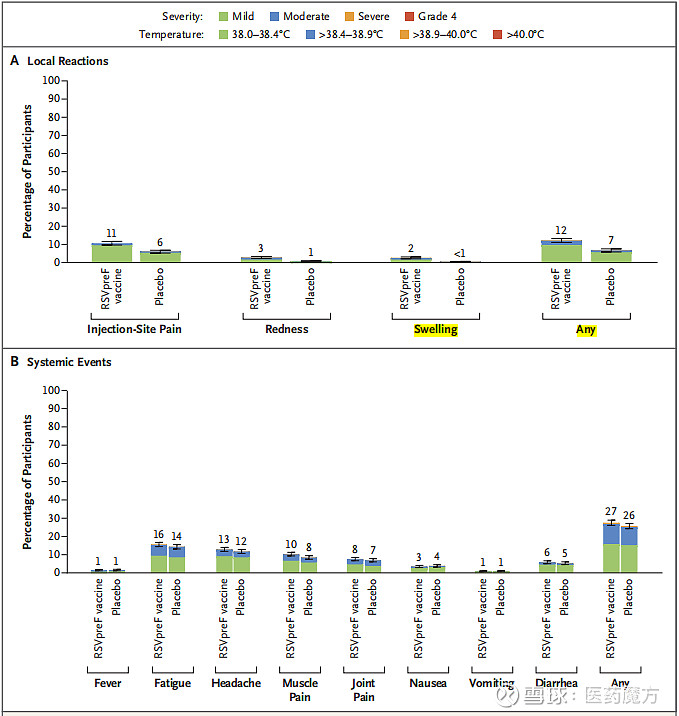
RSVpreF疫苗耐受性良好,最常见的不良反应包括注射部位疼痛(11%),疲劳(16%)和头痛(13%),较GSK3844766A更好。
同年11月1日,辉瑞又宣布RSVpreF疫苗在孕妇中开展的III期MATISSE研究达到两个主要终点中的其中一个,提前终止试验。婴儿出生后的前90天疫苗对RSV引起的严重下呼吸道疾病的保护效力达81.8%,6个月随访期的效力达69.4%。疫苗耐受性良好,在接种疫苗的孕妇及其新生儿中均未见安全性问题。
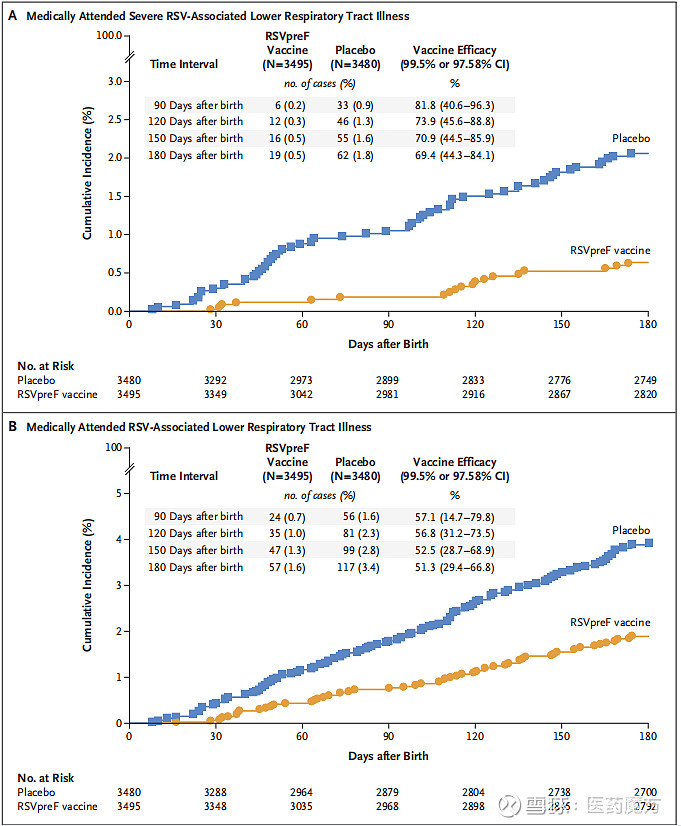
这两项研究结果已于今年4月5日同日发表在NEJM上[16,17]。
2023年2月28日,FDA专家委员会以7:4投票结果认可RSVpreF的安全性,以7:4投票结果认可RSVpreF的有效性。
辉瑞布局RSV决心不止于此,2022年4月,辉瑞以高达5.25亿美元价格收购了ReViral公司。据悉,ReViral拥有两款极具前景的RSV在研疗法,其中,sisunatovir是一款口服疗法,旨在阻断RSV病毒与宿主细胞融合,该候选药物已被FDA授予了快速通道资格。该公司第二个研发项目聚焦于通过靶向病毒N蛋白抑制RSV复制。该项目中的先导候选药物目前处于I期临床开发阶段。
mRNA-1345:RSV赛道的黑马
mRNA疫苗巧借新冠东风,迅速崛起,凭更快的开发速度和生产制造在抗击疫情中大放异彩。Moderna迅速将这一技术运用于RSV疫苗的开发。其开发的mRNA-1345为表达preF蛋白的单价mRNA疫苗,仅需单次免疫,从2020年9月启动I期临床到获得III期数据仅用了2年多时间。
2023年1月7日,Moderna宣布mRNA-1345预防老年人RSV感染的III期临床达到主要终点,对伴有两种及以上RSV-LRTD症状的保护率为83.7%,对伴有3个或更多症状的保护效力为82.4%。该试验正在进行中,并计划随着病例的增加(包括严重呼吸道合胞病毒)进行更多的疗效分析。基于该数据,Moderna计划于2023年上半年递交mRNA-1345的上市申请。
受试者大多数不良反应为轻度或中度,mRNA-1345组中最常见的不良反应为注射部位疼痛、疲劳、头痛、肌痛和关节痛。mRNA-1345组出现严重(3级或以上)系统性不良反应的总体发生率为4.0%,安慰剂组为2.8%。mRNA-1345组3级及以上局部不良反应的总体发生率为3.2%,安慰剂组为1.7%。
RSV疫苗的成功意味着在新冠之外,mRNA在常规疫苗领域也终于走通了成药之路,并且几乎与研发了60多年的重组蛋白疫苗在RSV预防领域同时撞线,不得不让人们对这类疫苗的前景产生无限遐想,未来mRNA疫苗将与传统疫苗同台竞技。
基于mRNA平台开发RSV疫苗的不止Moderna。2021年8月3日,赛诺菲宣布以32亿美元的价格收购了mRNA企业TranslationBio,将利用安全性可以媲美蛋白疫苗的新一代mRNA疫苗技术平台开发流感疫苗和RSV疫苗。
总结
每一个疾病领域获得突破的背后几乎都有着曲折的研发过程,在RSV疫苗研发追逐赛中,也有很多制药企业投入了大量的精力、物力、财力,比如Novavax,曾花费了十多年的时间开发该公司研发的RSV F蛋白重组纳米颗粒疫苗ResVax。遗憾的是,该款疫苗在老年人群、孕妇群体中进行的III期临床先后败北。
在GSK、辉瑞、Moderna进度领先的情况下,强生于今年3月29日宣布,在对其投资组合进行审查以确定产品开发优先级以及对RSV疫苗的前景进行评估后,决定退出RSV成人疫苗项目并终止正在开展的III期EVERGREEN研究。
在国外已经迎来首款获批的同时,国内RSV疫苗的开发也已经在路上,其中,艾棣维欣的ADV110已进展至II期临床,优锐医药从Bavarian Nordic引进的MVA-BN RSV疫苗已在国内获批临床,而爱科百发、歌礼制药、联拓生物等公司则专注于开发RSV治疗性药物。今年3月,GSK已在中国递交GSK3844766A的临床试验申请。相信,在不远的将来,中国也将迎来预防/治疗RSV的药物。
参考资料:
[1]. Blount, R. E. Jr, Morris, J. A. & Savage, R. E. Recovery of cytopathogenic agent from chimpanzees with coryza. Proc. Soc. Exp. Biol. Med. 92, 544–549 (1956).
[2]. Chanock, R., Roizman, B. & Myers, R. Recovery from infants with respiratory illness of a virus related to chimpanzee coryza agent (CCA). I. Isolation, properties and characterization. Am. J. Hyg. 66, 281–290 (1957).
This study reports the first isolation of RSV from infants.
[3]. Chanock, R. & Finberg, L. Recovery from infants with respiratory illness of a virus related to chimpanzee coryza agent (CCA). II. Epidemiologic aspects of infection in infants and young children. Am. J. Hyg.66, 291–300 (1957).
[4]. Glezen, W. P., Taber, L. H., Frank, A. L. & Kasel, J. A. Risk of primary infection and reinfection with respiratory syncytial virus. Am. J. Dis. Child 140, 543–546 (1986).
[5]. Shi, T. et al. Global, regional, and national disease burden estimates of acute lower respiratory infections due to respiratory syncytial virus in young children in 2015: a systematic review and modelling study. Lancet 390, 946–958 (2017).
[6]. McLaurin KK, et al. J Perinatol 2016;36:990-6.
[7]. CDC - 网页链接
[8]. 1997 – 2009 data. Figure adapted from Matias G et al. BMC Public Health 2017;17:271
[9]. V.A. Fulginiti, J.J. Eller, O.F. Sieber, J.W. Joyner, M. Minamitani, G. Meiklejohn, Respiratory virus immunization. I. A field trial of two inactivated respiratory virus vaccines; an aqueous trivalent parainfluenza virus vaccine and an alumprecipitated respiratory syncytial virus vaccine, Am. J. Epidemiol. 89 (4) (1969) 435–448.
[10]. A.M. Killikelly, M. Kanekiyo, B.S. Graham, Pre-fusion F is absent on the surface of formalin-inactivated respiratory syncytial virus, Sci. Rep. 6 (2016) 34108.
[11]. RSV wave hammers hospitals — but vaccines and treatments are coming.
[12]. Novel antigens for RSV vaccines.Curr Opin Immunol. 2015 Aug;35:30-8. doi: 10.1016/j.coi.2015.04.005. Epub 2015 Jun 10.
[13]. S.M. Varga, X. Wang, R.M. Welsh, T.J. Braciale, Immunopathology in RSV infection is mediated by a discrete oligoclonal subset of antigen-specific CD4(+) T cells, Immunity 15 (4) (2001) 637–646.
[14]. J. Shan, P.N. Britton, C.L. King, R. Booy, The immunogenicity and safety of respiratory syncytial virus vaccines in development: a systematic review, Influenza Other Respir. Virus 15 (4) (2021) 539–551.
[15]. DOI: 10.1056/NEJMoa2209604
[16]. DOI: 10.1056/NEJMoa2213836
[17]. DOI: 10.1056/NEJMoa2216480