自2017年PACIFIC研究的首次分析结果发表以来,不可手术的局部晚期非小细胞肺癌(NSCLC)患者的标准治疗已经从根治性同步放化疗(CRT)向前迈进至度伐利尤单抗(durvalumab)巩固治疗。然而,即使使用度伐利尤单抗之后,大多数患者仍然会复发并死亡,因此开发对III期NSCLC患者更好的治疗仍然是重要的未满足临床需求。
今年4月,JCO发表了COAST研究结果,COAST研究是一项随机、开放标签II期临床试验。旨在评估度伐利尤单抗 vs 度伐利尤单抗+CD73抑制剂Oleclumab或者度伐利尤单抗+NKG2A抑制剂Monalizumab治疗接受根治性CRT后不可切除的III期NSCLC的疗效与安全性。研究的主要终点是研究者根据RECISTv1.1评估的客观缓解率(ORR),次要终点包括安全性、缓解持续时间(DoR)、疾病控制率(DCR)、无进展生存期(PFS)和总生存期(OS)。
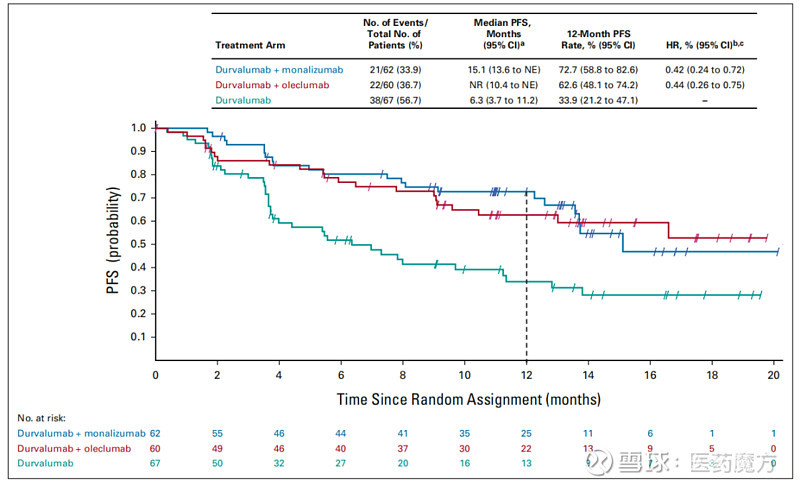
研究结果显示,度伐利尤单抗+Oleclumab和度伐利尤单抗+Monalizumab的ORR在数值上高于度伐利尤单抗单药,两种联合用药的PFS较度伐利尤单抗单药均显著延长,两种联合用药的12个月PFS率显著高于单药。使用度伐利尤单抗+Oleclumab、度伐利尤单抗+Monalizumab和度伐利尤单抗单药的全因≥3级治疗相关不良事件发生率分别40.7%、27.9%和39.4%。


其实,COAST研究并不是为了明确显示两个试验组相对于度伐利尤单抗单药的优效性,而是作为go/no-go试验来验证这两种联合治疗是否有希望进入III期试验开发。那这样的结果是否足以做出YES/NO的决策呢?我们还需思考哪些重要议题?
第一,COAST研究样本量较小的疑虑。
每组约60例患者,样本量较小,COAST研究未对主要终点ORR进行假设,但根据样本量可以在数值附近给出合理的置信区间,以便研究者可以在没有预设差异的情况下决定结果是否有前景。尽管结果表现出很有希望,但确实还有一些需要注意的地方。
第二,研究者评估的ORR主要终点存在质疑。
ORR是肿瘤学中常用的早期试验终点,能有效预测靶向药物疗效预后。但是,预测免疫检查点抑制剂疗效的效果可能较差,免疫反应可能存在延迟或误导,一些专家认为,DoR可能是更有效的终点。其次,这是一项开放性研究,ORR由研究者评估确定,使得评估中检测偏倚的可能性有利于非盲的实验组。最后,在CRT后巩固治疗试验中使用ORR作为主要终点并不是一个常规选择,因为根据RECIST标准,所有病灶均接受了明确的放疗,因此没有病灶符合可测量的条件。在这一人群中,三分之一的患者可能已经通过单独的CRT治愈,其他许多患者可能仍然对之前的CRT有反应,而对巩固治疗没有反应,PACIFIC研究中观察到安慰剂组的ORR有16%证明了这一点。
第三,次要终点PFS是否可以给出决策性参考?
在放化疗后的III期NSCLC人群中,考虑将肿瘤进展的评估作为决定因素的话,PFS可能是一个更好的选择,它能更有效的评估肿瘤进展。在COAST中,联合治疗组的PFS也显著长于单药组,Oleclumab联合治疗组的HR为0.44(95%CI,0.26-0.75),Monalizumab联合治疗组的HR为0.42(95%CI,0.24-0.72)。尽管研究者评估的PFS也容易受到评估偏倚的影响,但对于一项主要为提供疗效指标而不是确定性答案的试验来说,联合用药组显示出了有意义的差异,这一结果似乎更可靠。结合肿瘤反应数据,尽管并不能排除风险,但做出继续进行III期试验的决定也是合理的。
第四,我们是否该对度伐利尤单抗疗效表现不一致表示担忧?
COAST巩固治疗度伐利尤单抗单药组的PFS中位PFS仅为6.3个月,而PACIFIC试验度伐利尤单抗组的PFS为16.9个月。一般而言,随机试验是不受这种表现不佳批评的影响,因为随机分配的魔法假设在组间均匀分布任何不可测量的预后因素。然而,在小样本量的情况下,这种神奇的方法就很难被相信了。在小样本量的情况下,一组中具有不可测量的预后因素的患者的分配不平衡可能导致严重偏差。
第五,除了新型药物组合,还可以采取哪些其他方法来改善不可切除的III期NSCLC患者的结局?
在晚期NSCLC中有效方法是将免疫检查点抑制剂与化疗联合使用,无论PD-L1表达如何,都能改善预后,并可以将免疫加入的时间前移,同步放化疗。该方法的安全性已在Keynote 799研究中进行了检验。III期ECOG/ACRIN 5181研究(NCT04092283)现在正在检验这一假设,比较CRT期间同步使用度伐利尤单抗对比CRT单药治疗,两组随后进行度伐利尤单抗巩固治疗,主要终点为OS。PACIFIC-2研究(NCT03519971)也评估了同步使用度伐利尤单抗和CRT,随后进行巩固度伐利尤单抗方案的疗效与安全性,尽管本研究的对照组(单独使用CRT)已经不再是标准治疗。KEYLYNK-012的III期临床研究(NCT04380636)甚至结合了这两种方法,评估不可切除的局部晚期III期NSCLC患者在经过帕博利珠单抗联合CRT治疗后,以帕博利珠单抗(治疗组A)或帕博利珠单抗联合PARP抑制剂奥拉帕利(治疗组B)作为维持治疗的疗效和安全性,并对比同步放化疗后以度伐利尤单抗为巩固治疗(治疗组C)的疗效和安全性,共同主要终点为PFS和OS。
最后,对于局部晚期NSCLC试验疗效的各种终点指标,我们到底该如何选择?
如下表所示,对于早期试验,考虑到需要更及时评估疗效,PFS可能是最佳终点,即使随后的随访也可能需要数年。另一种选择是使用ctDNA检验治疗后的微小残留病灶,这几乎可以立即提供疗效证据,同时允许基于微小残留病灶状态进行潜在的治疗升级(如果为阳性)或降级(如果为阴性)(NCT04585490)。对于晚期试验,OS显然是疗效评估的金标准,尽管OS的评估确实需要更长的时间和更大规模的试验,并且在中位生存期为多年的III期NSCLC人群中(PACIFIC中为47个月),在OS报告出来之前,存在肿瘤继续进展的风险。
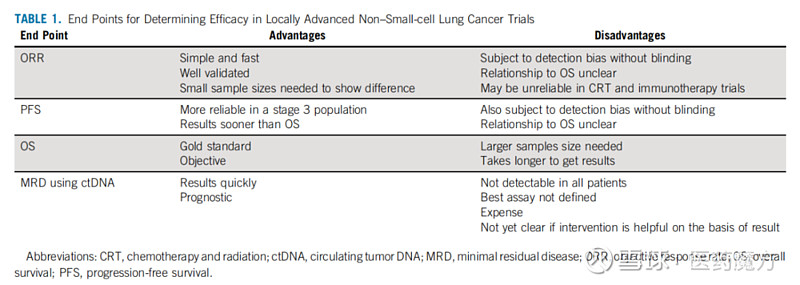
局部晚期NSCLC临床试验各种终点指标的优劣势对比
虽然对于最佳终点指标的选择仍然不确定,但是有许多的潜在的治疗方案正在局部晚期NSCLC患者中进行试验,尽管试验并不是一帆风顺的,但这依然非常令人鼓舞。