7月14日,迈博药业发出公告,称英夫利西单抗生物类似药(CMAB008)上市申请获NMPA批准上市,用于治疗成人溃疡性结肠炎、强直性脊柱炎、类风湿性关节炎、成人及6岁以上儿童克罗恩病、瘘管性克罗恩病、银屑病。这是国内首家获批上市的英夫利西单抗生物类似药!

英夫利西单抗是一种人-鼠嵌合性单克隆抗体,可与肿瘤坏死因子α(TNFα)的可溶形式和透膜形式以高亲和力结合,抑制TNFα与受体结合,从而使TNF失去物活性,改善炎症反应及自身免疫性疾病。强生英夫利西单抗原研产品目前已在全球获批用于治疗类风湿性关节炎、克罗恩病、溃疡性结肠炎、强直性脊柱炎、银屑病关节炎等多种自身免疫性疾病。
强生英夫利西单抗最早于2007年2月在国内获批上市,商品名为类克。原研2020年全球销售额为40.8亿美元。根据灼识咨询报告,英夫利西单抗在中国的市场规模在2019年为人民币6亿元,预计到2023年将增长至人民币32亿元,到2030年将达到人民币75亿元,从2019年到2030年的复合年增长率为25.6%。预计到2030年,生物类似药将在英夫利西单抗中占64.2%的市场份额。
由医药魔方PharmaGo数据库可知,该产品除了百迈博制药上市外,嘉和生物、海正药业、精鼎医药已申报该产品生物类似药上市申请,目前处于审评阶段。

2021年6月28日,迈博药业间接全资附属公司泰州迈博太科药业与科兴生物制药订立独家许可协议,向科兴生物制药授出有关于除中国大陆、日本、欧洲及北 美以外的所有国家及地区开发及商业化CMAB008的独家许可。
各合作区域的独家许可的期限单独计算,且应自CMAB008于该相关合作区域获批上市日期起计不少于十年(可自动再延长十年)。泰州药业与科兴生物制药已就北美地区以外的美洲国家和地区销售目标进行约定:第一个和第二个完整销售年度 合计销售目标为不低于二十万支;第三个完整销售年度起,年度销售目标为不低于二十万支/年。
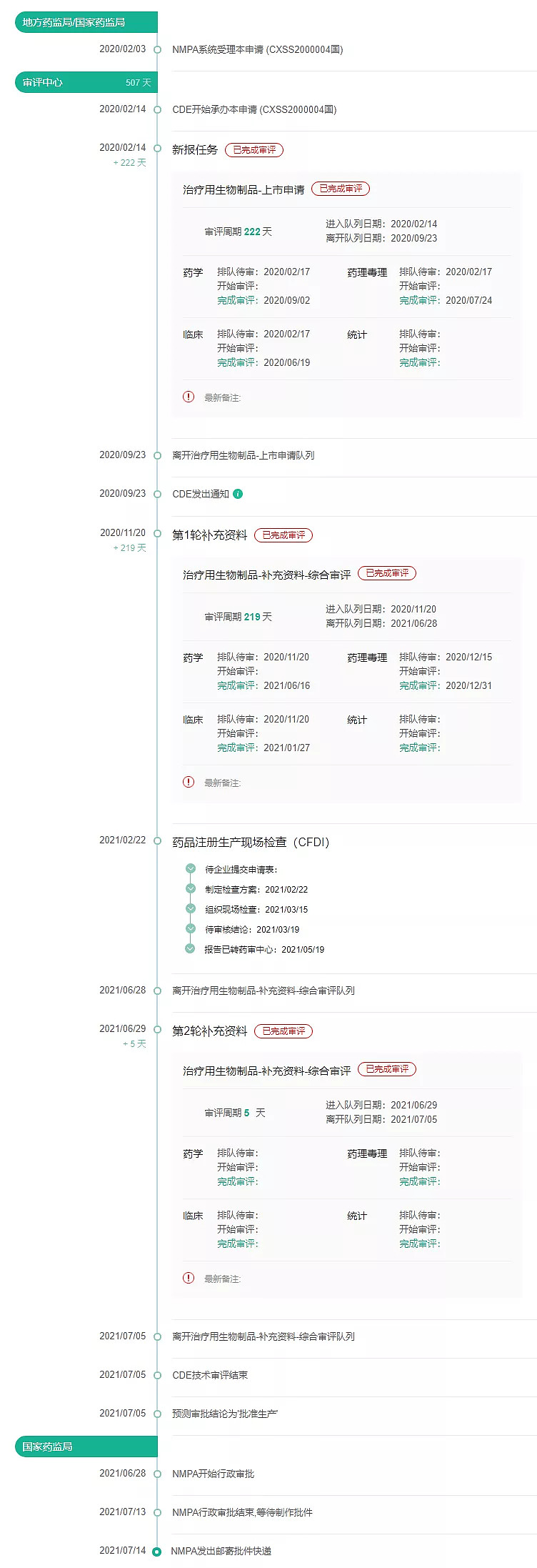
附:审评时间轴(来源于医药魔方PharmaGo数据库)