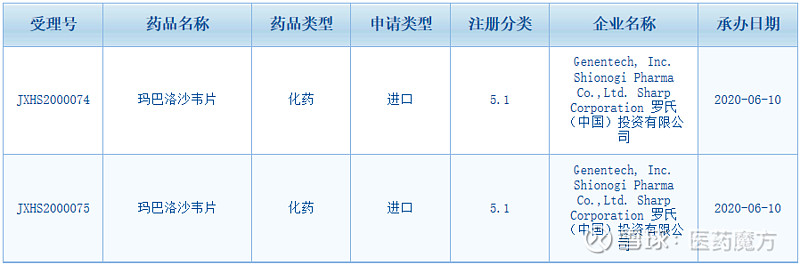
6月10日,罗氏在中国提交的流感药物玛巴洛沙韦片(英文商品名:Xofluza)上市申请获得CDE受理。
Xofluza是一种First-in-Class的口服抗病毒药物,服用一次即可见效,可治疗对奥司他韦耐药的病毒株和禽流感病毒株。Xofluza不同于靶向神经氨酸酶的抗流感药,它通过抑制流感病毒的cap-依赖型核酸内切酶来抑制病毒复制,也就是在流感自我繁殖的早期发挥药效,因此它阻断流感的速度比神经氨酸酶抑制剂更快。
Xofluza由盐野义/罗氏共同开发,于2018年2月在日本率先获批,同年10月在美国获批用于治疗12岁及以上急性无并发症的流感患者,是近20年来全球首款获批的全新机制抗流感药物,该适应症目前已经在中国香港和台湾获批。
2019年10月,FDA批准Xofluza新适应症,用于治疗12岁及以上流感并发症高风险人群。2020Q1,Xofluza销售额为2800万瑞士法郎,同比增长371%。罗氏也已经向FDA提交了玛巴洛沙韦口服混悬液用于1~12岁儿童的流感急性发作治疗和片剂用于流感暴露后预防的上市申请,这2项申请有望在2020/11/23获得批准。
流感每年大约会导致全球300-500万例重症病例,数百万患者住院治疗,65万患者死亡,对公众健康造成巨大威胁。国内市场上的流感治疗药物主要为东阳光的可威(奥司他韦),该药在2019年的销售额达到59.4亿元。目前,国内已有多家奥司他韦仿制药申报上市,获批之后将给东阳光带来一定冲击。预计罗氏新型抗流感药物Xofluza获批上市后,国内流感市场竞争将更加激烈。