12月18日,Seattle Genetics宣布FDA授予tucatinib“突破性疗法”资格认定,联合曲妥珠单抗、卡培他滨用于治疗已经接受过曲妥珠单抗、帕妥珠单抗和T-DM1的局部晚期不可手术切除或转移性HER2阳性乳腺癌,包括出现脑转移的HER2阳性乳腺癌。
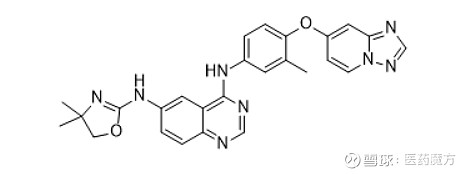
tucatinib是高选择的口服小分子HER2抑制剂。Seattle Genetics曾于今年10月公布一项代号为HER2CLIMB的关键临床试验的积极顶线结果,并在12月11日的SABCS2019大会上公布了额外的详细数据。该结果同步发表于《新英格兰医学杂志》。
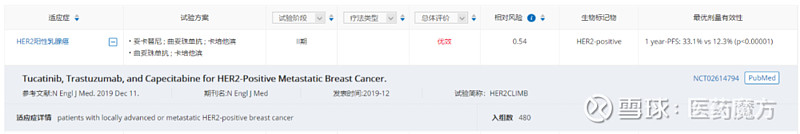
来源:NextPharma
HER2CLIMB研究入组了612例患者,比较tucatinib+曲妥珠单抗+卡培他滨 vs 曲妥珠单抗+卡培他滨的疗效差异。入组的患者总体上既往接受过4线(中位数)疗法,其中47%的患者在入组时发生了脑转移。
试验结果显示,tucatinib+曲妥珠单抗+卡培他滨显著提高患者的无进展生存期(7.8 vs 5.6个月),将疾病进展或死亡风险降低46%,达到试验的主要终点。试验组的12个月无进展生存率为33.1%,对照组为12.3%。
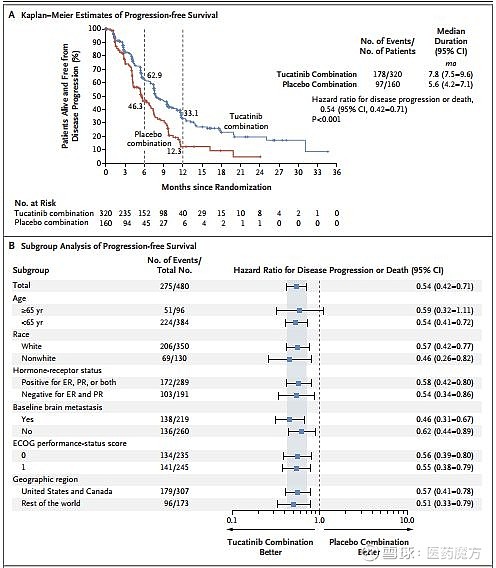
在脑转移亚组中,tucatinib+曲妥珠单抗+卡培他滨组相比对照组也显著延长了PFS(7.6 vs 5.4个月),将疾病进展或死亡风险降低52%,达到了试验的关键性次要终点。
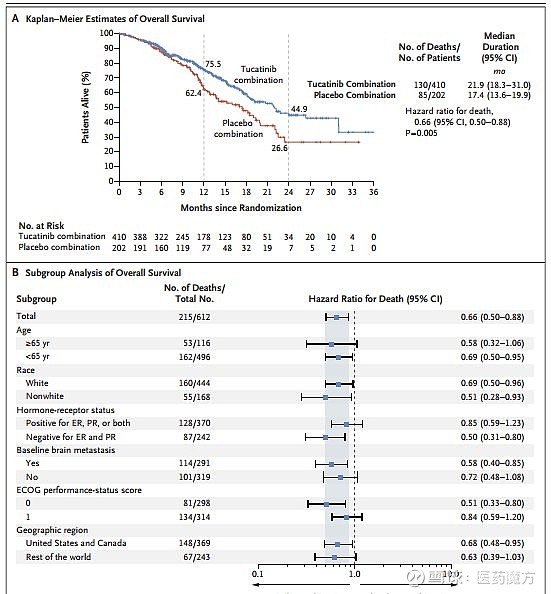
另外,tucatinib+曲妥珠单抗+卡培他滨还显著改善了患者的总生存期(21.9 vs 17.4个月),将死亡风险降低34%。试验组2年总生存率为45%,对照组为27%。
Seattle Genetics首席医学官Roger Dansey表示:FDA授予tucatinib突破性疗法资格,代表了监管机构对这一可以影响患者生命的创新疗法的认可。我们计划在2020年第1季度向FDA和EMA提交上市申请,以尽快将这一创新疗法带给患者。”