炎症性肠病(IBD)是一种以慢性炎症为特征的肠道炎性疾病,主要包括克罗恩病和溃疡性结肠炎。仅在美国,目前就有160万人患终生无法治愈的IBD,每年诊断出的新病例达7万。
IBD患者遭受腹痛、腹泻、乏力、皮肤病变等极度不适的症状,并且随着时间的推移会不断加重,这导致23%−45%的溃疡性结肠炎患者以及75%的克罗恩病患者需要在某个时间点手术切除部分胃肠道。
虽然消炎药可以抑制急性炎症,抗生素可以在IBD发作时对抗局部感染,但它们的使用也要付出代价:前者有严重的副作用,后者会破坏我们身体许多功能所依赖的有益微生物群。然而,目前还没有一种疗法可以直接作用于肠道上皮发炎部位,以加快肠黏膜愈合并尽量减少这些药物的使用。
现在,哈佛大学Wyss研究所的 Neel Joshi 博士团队已经开发出了解决此问题的疗法。基因工程大肠杆菌 Nissle 1917(EcN)产生的纳米纤维网能直接与肠道黏液结合,并像补丁一样填充发炎区域,使其免受肠道微生物和环境因素的影响。这种基于益生菌的疗法能有效保护小鼠免受化学制剂诱导的结肠炎的影响,并促进肠黏膜愈合。相关研究成果于12月6日发表在 Nature Communications 上 [1]。
知识卡片:EcN(血清型为06:K5:H1)是从一次志贺菌痢大爆发时未出现腹泻的士兵的粪便中分离得到的无致病性的革兰氏阴性益生菌。EcN可通过调控抗菌肽的表达,增加免疫球蛋白A(IgA)和黏蛋白的分泌以及促进抗炎症免疫反应,在肠道中发挥重要的免疫功能。

图片来源:Nature Communications [1]
众所周知,外部伤口(例如皮肤割伤或擦伤)通常可以简单地用创口贴覆盖来帮助其愈合。然而,当涉及诸如内脏的一些被黏液层覆盖的内表面时,这种常规的材料是无效的,因为黏液阻碍了它们的牢固附着并迅速将它们带离伤口部位。
在之前的研究中,Joshi团队已经证明,可自我再生的益生菌水凝胶在体外能牢固地粘附在黏膜表面。并且,当对小鼠进行口服给药时,在不影响动物健康的情况下,这种水凝胶能经受住胃和小肠的恶劣pH值及消化环境,从而确保益生菌能安全到达目标部位。
为了制造这种水凝胶,该团队对EcN进行基因编程,使其合成并分泌一种改性的CsgA蛋白。作为大肠杆菌卷曲菌毛系统的一部分,这种蛋白在细菌的外表面聚集成长的纳米纤维,并与肠壁表面的黏液蛋白结合。
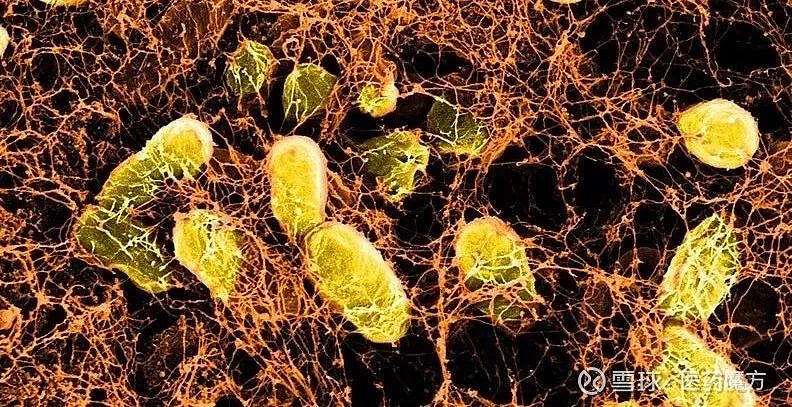
卷曲菌毛纳米纤维网,由基因编程的非致病性大肠杆菌连续产生,能与肠壁表面的黏液蛋白结合。图片来源:哈佛大学Wyss研究所官网
在这项新研究中,Joshi团队在此基础上进一步将基于三叶因子家族3(TFF3)的粘着水凝胶生产机制引入EcN中。TFF3能增加水凝胶在肠道的停留时间,以保护黏膜上皮免受各种损伤,并帮助它们修复损伤。
知识卡片:三叶因子家族(trefoil factor family,TFF)是一群主要由胃肠道黏液细胞分泌的小分子多肽,主要用于促进上皮的修复。目前在哺乳动物体内发现的有3种,即乳癌相关肽(pS2/TFF1)、解痉多肽(SP/TFF2)和肠三叶因子(ITF/TFF3)。TFF在胃肠道的分布具有特异性,但其在生理及病理状态下的表达有所不同。在人正常组织中,TFF3主要在小肠及结肠杯状细胞、胃窦黏膜中表达,其还具有特殊的抗酸、耐酶及热分解的生物学特性。
这个动画解释了可自我再生的益生菌水凝胶如何作为创口贴,来帮助肠黏膜愈合。视频来源:哈佛大学Wyss研究所官网
Joshi 表示:“我们创造了一种生物相容的粘附性生物材料,作用如同稳定的可自我再生的邦迪创口贴,还能提供用于黏膜愈合的生物信号。这些材料是由常驻的工程菌原位分泌的,它们牢牢地附着在黏液层上。我们称该方法为‘益生菌相关的治疗性卷曲菌毛杂交’(Probiotic-associated therapeutic curli hybrids,PATCH)。”
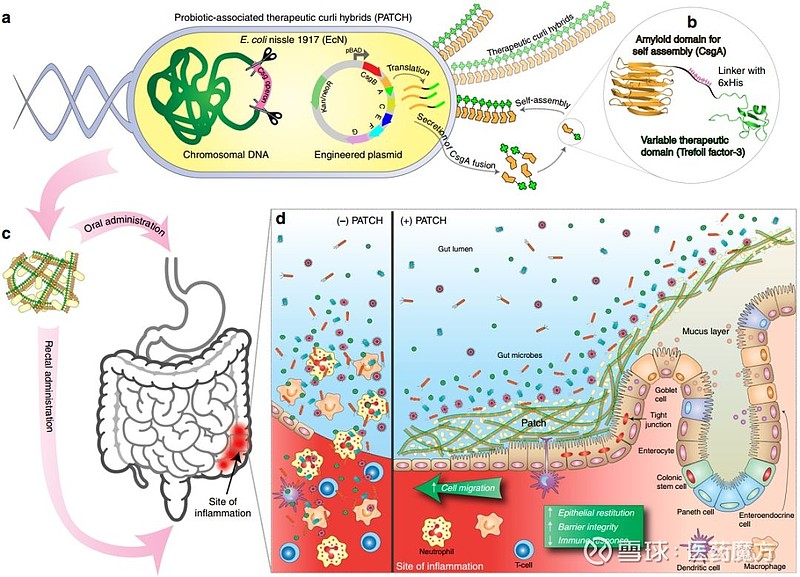
益生菌相关的治疗性卷曲菌毛杂交(PATCH)。图片来源:Nature Communications [1]
进一步实验证明,新的工程EcN口服后会在小鼠肠道内定居并繁殖,它们的卷曲菌毛纤维能与肠道黏液层结合在一起。此外,工程EcN在体内外均能分泌融合的(CsgA-TFF3)卷曲菌毛,且无致病性。
疗效研究显示,在葡聚糖硫酸钠(dextran sodium sulfate,DSS)诱导的小鼠结肠炎模型实验中,从DSS处理前3天开始,每日接受工程EcN给药的小鼠具有明显更快的愈合和更低的炎症反应,与对照组相比,它们体重减轻少得多,且恢复得更快。
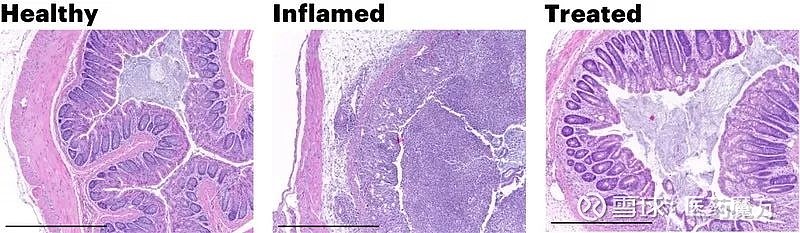
结肠炎疾病模型小鼠的结肠组织切片。损伤小鼠结肠(中)失去了健康肠道(左)特有的柱状细胞结构。当用PATCH方法治疗后,小鼠结肠即使在有炎症损伤的情况下也能保持健康形态(右)。图片来源:哈佛大学Wyss研究所官网
总结来说,通过该研究,Joshi团队开发了一种生物相容的、安全的粘着性生物材料,它不仅能牢固附着在肠道炎症部位,保护其免受环境影响,还有助于促进伤口黏膜愈合。
Joshi和他的团队认为,他们的方法可以发展为现有的IBD抗炎、免疫抑制剂和抗生素疗法的辅助治疗,以帮助患者减少药物暴露,并有可能为IBD复发提供保护。
Wyss研究所创始主任 Donald Ingber 博士表示:“这种强大而简单的方法可能会潜在地影响成千上万IBD患者的生活。”
杂志:Nature Communications
亮点:哈佛大学Wyss研究所的Neel Joshi博士团队利用工程大肠杆菌Nissle 1917开发出了一种可以直接作用于肠道上皮炎症部位的粘着性生物材料,能加快肠黏膜愈合并有助于减少患者药物暴露以降低副作用。该研究可能会潜在地影响成千上万IBD患者的生活。
相关论文:[1] Pichet Praveschotinunt et al. Engineered E.coli Nissle 1917 for the delivery of matrix-tethered therapeutic domains to the gut. Nature Communications (2019).参考资料:
1# Empowering mucosal healing with an engineered probiotic(来源:哈佛大学Wyss研究所官网)
2# Trust your gut to be healed with probiotic hydrogels(来源:哈佛大学Wyss研究所官网)