6月17日, Molecular Templates宣布,FDA已受理其与武田共同开发的TAK-169的新药临床试验(IND)申请,用于治疗复发/难治性多发性骨髓瘤。
TAK-169是把对CD38有亲和力的单链可变片段(scFv)融合到一种基因工程化的志贺样毒素A亚单位(SLTA,一种核糖体失活细菌蛋白[RIP])而组成的一种工程化毒素体( Engineered Toxin Bodies,ETBs)药物,通过SLTA介导的细胞毒作用来特异性杀伤CD38阳性肿瘤细胞。TAK-169诱导的核糖体不可逆抑制并导致肿瘤细胞死亡发生在细胞内,因此会导致肿瘤微环境会发生改变,如CD55/ 59上调,这种效应通常会抑制抗体药物的ADCC或CDC作用,但是并不会对TAK-169的活性有影响。
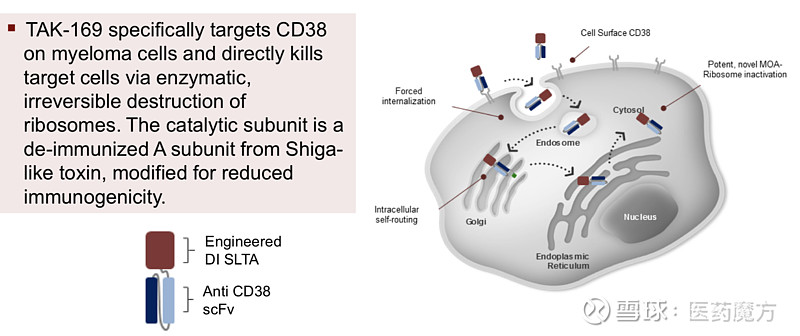
TAK-169作用机制
TAK-169不会与daratumumab(Darzalex,首个获批用于治疗多发性骨髓瘤的单抗药物)和其他CD38抗体药物竞争CD38结合位点,可以克服daratumumab耐药,并且在daratumumab存在的情况下依然具有抗肿瘤活性。因此,TAK-169具有与已批准CD38抗体药物联用的潜力。
Molecular这个专有的工程化毒素体(ETBs)技术平台提供了一种新的靶向生物疗法,目前也有基于这个技术平台的多个I期在研药物,比如靶向HER2的MT-5111。

来源:Molecular官网
2018年9月19日,Molecular宣布与武田达成协议,共同开发用于治疗多发性骨髓瘤的靶向CD38的工程化毒素体药物。其中TAK-169是核心候选药物。根据协议条款,武田将向Molecular支付3000万美元首付款。如果Molecular 行使其共同开发的选择权,则有资格获得后期总额6.325亿美元的开发、监管和商业化里程碑付款;如果不行使选择权或退出共同开发,则可获得最多3.375亿美元的里程金。武田还同意为成功上市产品的销售支付版税。Molecular Templates和武田将平均分担开发成本。