来源:器械之家,未经授权不得转载,且24小时后方可转载。
近日, 美国食品和药物管理局(FDA)对来自中国的塑料注射器进口加强了监管,并计划在必要时阻止中国制造的注射器进入美国。原因是担心其质量问题可能影响医疗安全。
在去年11月收到了几家中国注射器制造商的质量问题报告后,FDA首次建议消费者,医护人员和医疗机构,“如果可能,考虑使用非中国制造的注射器”。
随后分别对江苏神力医疗产品有限公司、江苏彩纳医疗器械有限公司、浙江龙德医药有限公司和上海康德莱企业发展集团有限公司等多家中国制造商发布进口禁令。
截止2024年5月14日,采纳和神力分别有190批和47批产品被拒绝入境,康德莱和龙德暂无拒绝入境记录。
01
美国拟全面禁止中国注射器
同步加征关税
除了加强监管以外,美国还将对我国注射器在内的一系列医疗用品加征关税。
2024年5月14日美国白宫宣布,将对我国的钢铁和铝、半导体、电动汽车、电池、关键矿物、太阳能电池、船岸起重机、部分医疗用品(包括注射器、针头和手术手套)等价值 180 亿美元的产品提高关税。生效时间均于2024年开始,但具体日期不明。
根据条例,医疗产品领域,注射器和针头的关税税率将从0%提高到50%;对于某些个人防护装备(PPE),包括某些呼吸器和口罩,关税税率将从0-7.5%提高至25%。另2026年起,橡胶医用和手术手套的关税将从7.5%提高至25%。
中国是一次性注射器生产大国,也是出口大国。不管是全面禁止中国塑料注射器进入美国,还是加征关税,将给我国注射器出口带来重大影响。
据共研网统计2017-2022年期间,我国一次性注射器年出口数量从138.68亿个增加到202.89亿个。
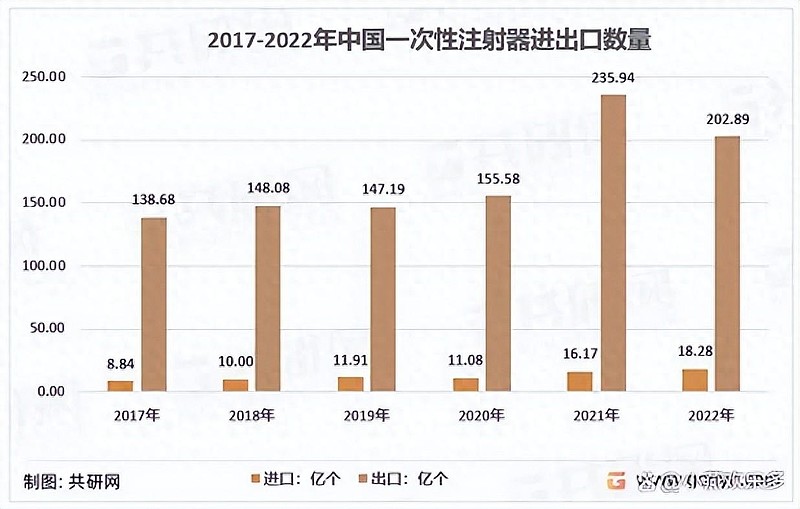
资料来源:中国海关、共研产业咨询(共研网)
我国共向191个国家和地区出口一次性注射器,其中美国是压倒性的海外第一大市场,22年向美国的出口量达到了25.05亿个。
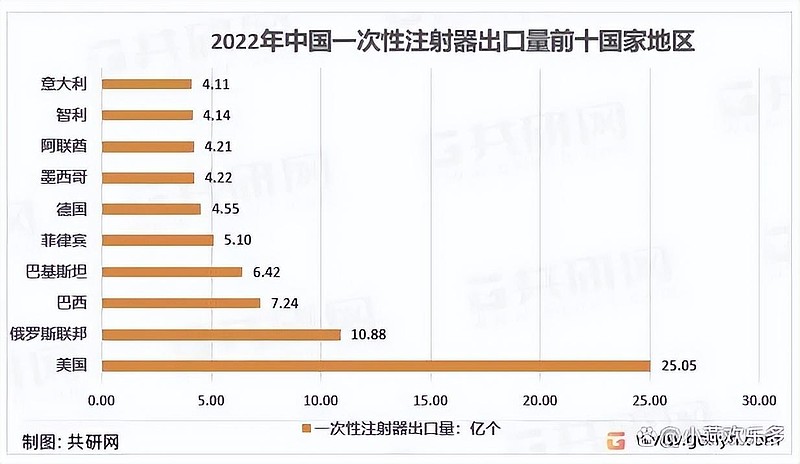
资料来源:中国海关、共研产业咨询(共研网)
江苏省质量和标准化研究院数据显示,近三年中国注射器出口额呈连续下降趋势,2022年和2023年出口额分别为9.08亿美元和7.42亿美元,同比分别下降18.7%和18.3%。美国作为我国注射器第一出口国,在2023年出口美国1.75亿美元,占比23.6%。
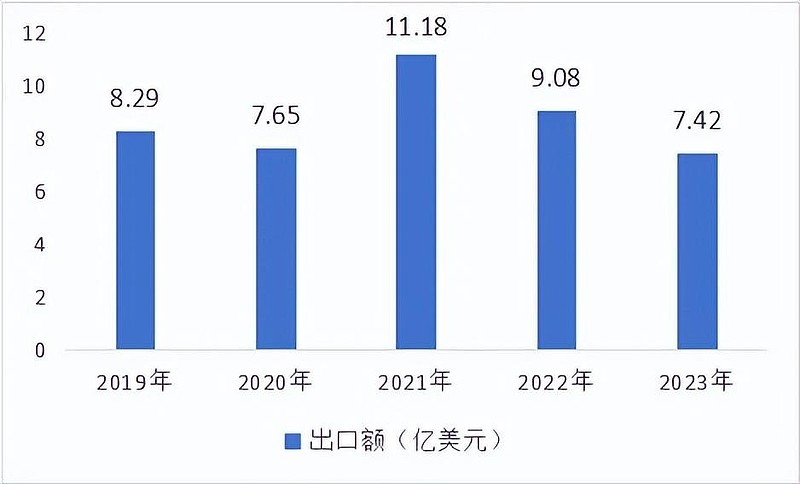
02
注射器事件始末
纵观历史,这还是FDA首次,对中国某个领域的所有制造商“开枪”。
而整件事情的起因,还要从2023年11月说起。彼时,FDA发布安全通知称,收到了有关几家中国注射器制造商的质量问题的信息,建议当地机构避开中国制造的塑料注射器。
2023年12月开始,FDA检查员走访在美国销售分销中国注射器的多家企业。其中包括Medline Industries和Sol-Millennium Medical的工厂。调查发现,这两家企业不仅进口和销售未经批准的中国制造的塑料注射器, 同时还有违反质量体系规定的行为。

今年3月18日,FDA就销售和分销未经批准的相关违规行为,向江苏神力医疗、Medline Industries和Sol-Millennium Medical发出警告信。
根据信件内容,江苏神力仅获得了5mL luer-lock活塞注射器的 510(k) 认证,但却向美国市场销售了3、10、20、50和60毫升鲁尔锁定注射器。
此外,FDA 在给Medline Industries公司的警告信中还提到了江苏采纳医疗科技公司生产的塑料注射器的质量问题和性能测试失败的问题。FDA 了解到,江苏采纳的几款塑料注射器的性能测试显示出现意外且无法解释的故障。
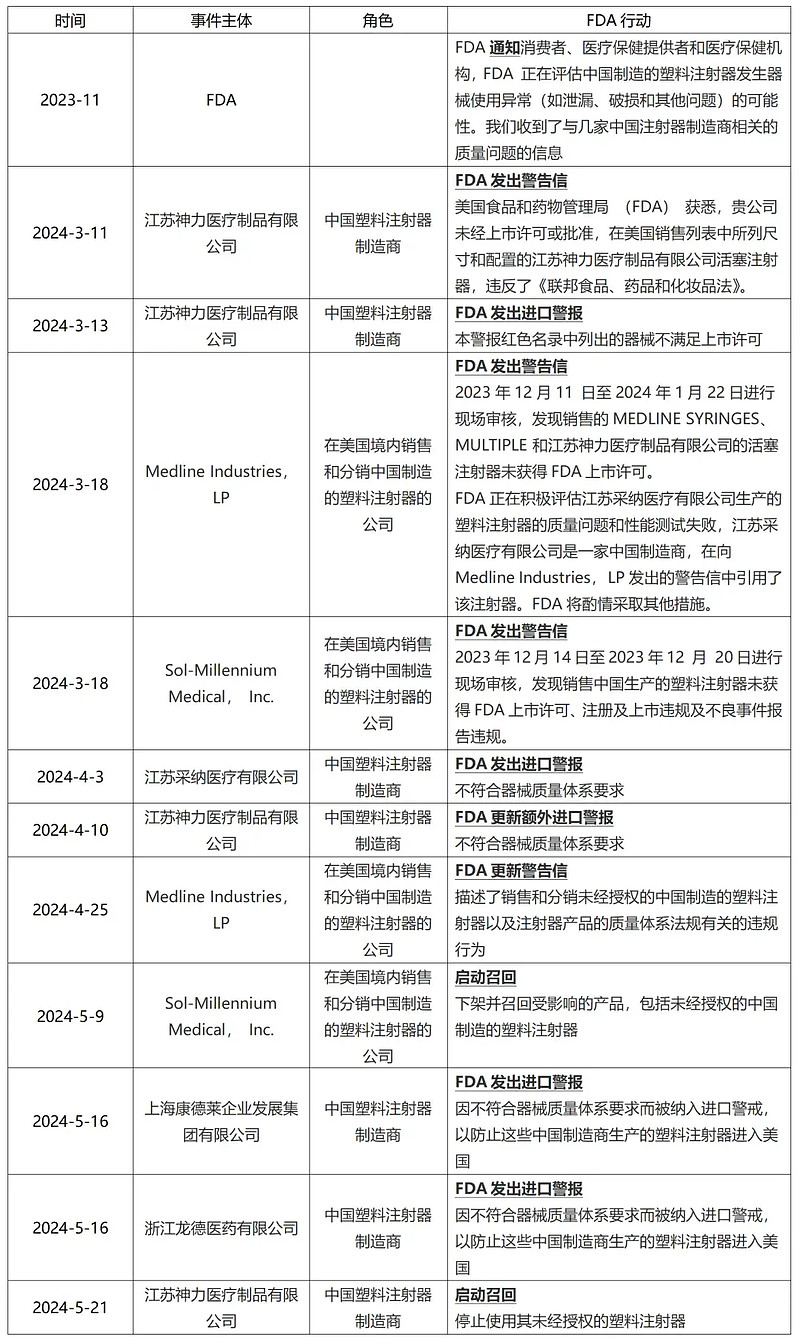
图片来源:国瑞中安法规资讯
随后,FDA扩大对江苏神力的调查,并于4月向Cardinal发出警告。
据悉,Cardinal的手术包套组中涵盖从Merit Medical采购的塑料注射器,而该产品正是由江苏神力生产。Merit 在收到FDA的通知后,召回了这些套件。随后Cardinal也召回了受影响的手术包产品。
禁售名单增加
随着FDA监管的进一步加强,中国注射器企业的禁售名单持续增长:
2024年5月16日,FDA宣布对浙江龙德医药有限公司和上海康德莱企业发展集团股份有限公司发出进口警告,因其不符合器械质量体系要求,所有活塞注射器不允许再进入美国。
加上此前3月28日和4月3日禁止的江苏神力医用制品有限公司和江苏采纳医疗有限公司,已有4家公司被列入禁售名单。
5月底,江苏神力启动召回,召回产品的生产时间横跨2019年5月至2023年12月前后4年半,数量多达1.08亿只。消息一出,全网哗然。
03
市场空白如何填补?
从另一个角度来看,神力医疗的召回在一定程度上为其他国内企业提供了进入美国市场的机会。
由于美国国内产能在短期内无法实现快速提升,神力医疗产品召回后,美国注射器市场将会出现“短暂空白”。而那些不在FDA禁止名单内且暂未受影响的国内企业可能有机会填补这一市场空白,中国塑料注塑器行业或将迎来新的爆发点。
目前,中国注射器械主要生产企业包括三鑫医疗、通化东宝、天松医疗、威高股份、普华和顺。
值得注意的是,这种市场空白能否真正为国内企业所利用,还要考虑多个因素。除了质量和合规问题外,美国对中国进口医疗产品加征的关税将成为未来国内企业进入该国的主要障碍。
在面对这些挑战的同时,国内企业是否能够通过创新和提高效率来降低成本,从而在竞争激烈的国际市场中脱颖而出?又如何在满足美国市场需求的同时,建立起长期的竞争优势?对此,器械之家将持续关注。