猎药人俱乐部研究团队整理
6月13日,圣诺医药(sirnaomics ltd.)宣布,集团发表了其新型寡核苷酸化学药物偶联剂(ODC)的一项重大进展。该 ODC 在多种肿瘤细胞系和小鼠胰腺肿瘤模型中显示出强大的抗肿瘤活性。这项研究成果发表在最新一期的《肿瘤研究与治疗杂志》(Journal of Oncology Research and Therapy)上(2024 年 6 月:第 1-16 页,第 9 卷第 02 期)。

公司认为,这项突破性的工作为公司基于RNAi的癌症治疗计划奠定了坚实的基础,该计划使用专有的抗体-核糖核苷酸-化学药物结合物(AODC)模式。Sirnaomics创始人、董事长兼首席执行官陆阳博士表示:“Sirnaomics专有的ODC制剂的最新进展表明,公司在新型癌症RNAi疗法方面持续的创新和努力,同时推动了我们对STP705治疗皮肤癌症、STP707治疗实体瘤和STP122G抗凝治疗的临床研究。我们希望Sirnaomics的AODC制剂在ADC取得巨大成功的基础上提供一种治疗各种癌症的替代方法,并带来广泛的合作机会。”
01
含有CHK1特异性siRNA的吉西他滨:
提高吉西他滨疗效,显示强大抗肿瘤活性
非核苷类似物吉西他滨一直是治疗胰腺癌的标准药物。这种药物在体外对胰腺癌细胞有很好的疗效,但由于生物利用度较低,需要大剂量输注,这种全身暴露会给患者带来很大的毒性。为对抗胰腺癌的不良预后,人们一直在积极寻求靶向治疗以增强吉西他滨杀死肿瘤细胞的功效,从而减少治疗效果所需的剂量。
在这一探索中,一种重要的方法是使用siRNA来沉默特定基因,从而增加吉西他滨的效力和/或疗效。如Azorsa等人在Synthetic lethal RNAi screening identifies sensitizing targets for gemcitabine therapy in pancreatic cancer中发表了针对CHK1基因的siRNA增强了吉西他滨对胰腺癌细胞的作用。Fredebohm等人随后的一篇论文证实了CHK1是吉西他滨对胰腺肿瘤细胞毒性的增强剂。
因此,Sirnaomics Inc.团队在2020年发表在《NAR Cancer》的研究A novel siRNA–gemcitabine construct as a potential therapeutic for treatment of pancreatic cancer,选择了Azorsa等人在论文中鉴定的19-mer CHK1 siRNA序列,在合成siRNA双链的过程中,在其有义链中加入吉西他滨取代胞嘧啶作为修饰手段。结果显示,与单独使用吉西他滨相比,SiRNA-吉西他滨结构在不同的细胞系中的 IC50 可提高约 100 倍。该团队还研究了这种药物在胰腺癌细胞中的作用,并优化了吉西他滨的数量以提高疗效。
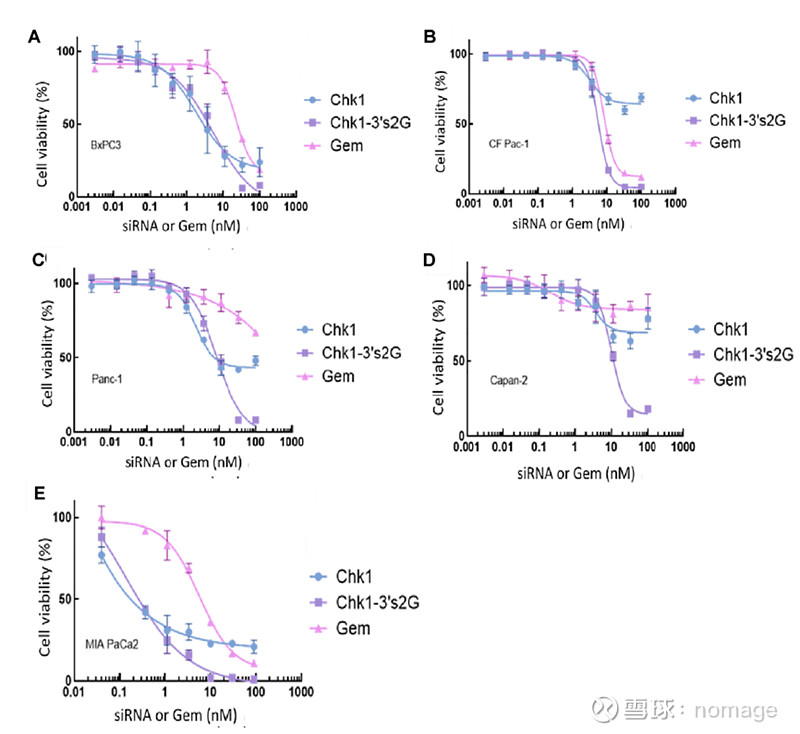
图:用吉西他滨修饰的Chk1 siRNA对各种胰腺肿瘤细胞类型的疗效。用 siRNAs 转染 384 孔板中的每孔一千个细胞,或用吉西他滨治疗 96 小时。细胞活力用 CellTiter-Glo® 2.0 试剂测定。(A) BxPC3、(B) CFPAC-1、(C) Panc1、(D) Capan-2 和 (E) MIA PaCa-2 的剂量曲线。Chk1:针对 CHK1 基因的25-mer siRNA;Chk1-3s2G:在有义链的 3 端用两个吉西他滨修饰的 CHK1;Gem:单独使用吉西他滨。每个数据点以四个重复的平均值 ± SD 表示。实验重复三次,结果相似。所有数据均归一化为未修饰的 NS siRNA 处理结果(数据未显示)。
在最新发表在Journal of Oncology Research and Therapy中的CHK1 siRNA Containing Gemcitabine and Chemically Modified Nucleotides Shows Antitumoral Activity in Vitro and in Vivo一文中,研究人员进一步通过使用化学修饰的siRNA来扩展这些研究,该研究采用了2'-Fluoro和2'-0-Methyl修饰模式,新构建体在所有测试的细胞中都进一步提高了效力。

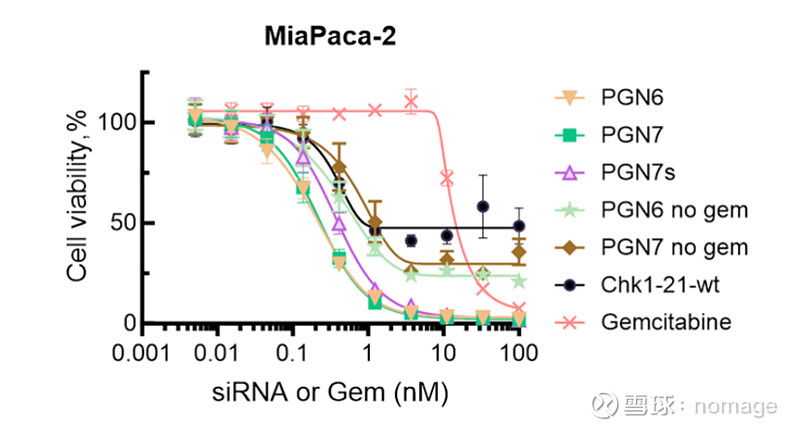
图:
化学修饰和在 CHK1 siRNA 中加入吉西他滨对 MiaPaCa-2 细胞效力的影响
此外,该研究进一步探索了构建物对其他肿瘤类型的抑制作用,发现将吉西他滨添加到SiRNA中,不仅可以对抗胰腺癌细胞模型,还可以对抗肺癌、卵巢癌三阴性乳腺癌和结肠癌。体外测试显示,使用胰腺、NSCLC、TNBC和卵巢细胞培养模型验证了含有CHK1特异性siRNA的吉西他滨的有效抗肿瘤活性。
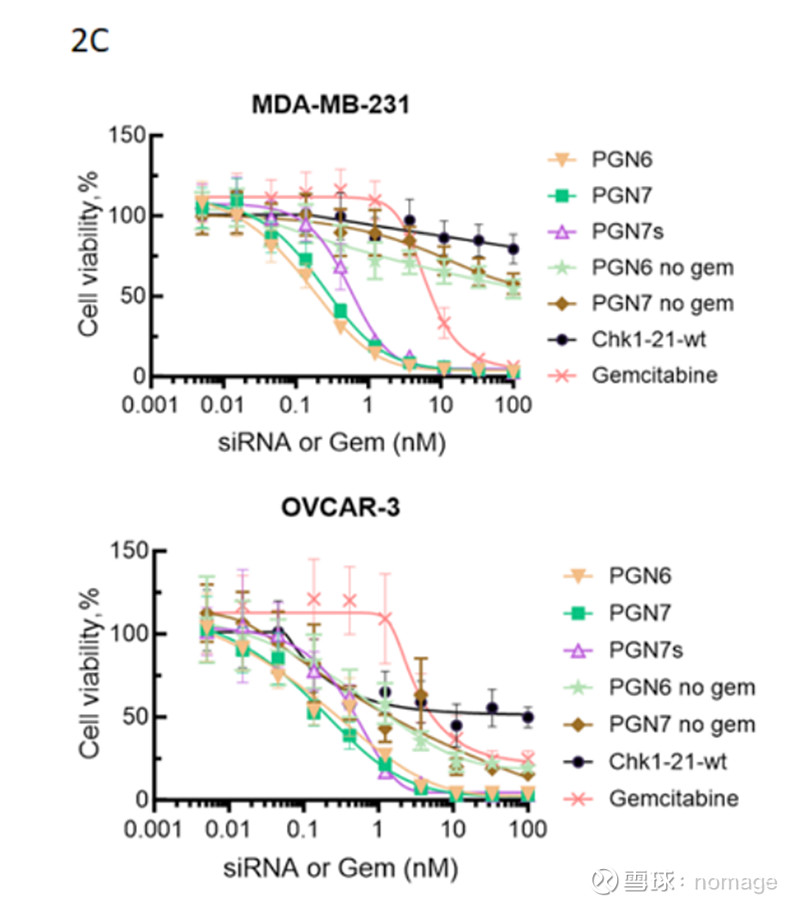
图:不同siRNA构建对TNBC和卵巢肿瘤细胞效力的影响
最后,该研究将不同版本的CHK1 SRNA+吉西他滨配制成具有良好控制尺寸(-82-88nm)和zeta电位(34-36mV)的多肽纳米颗粒。当静脉注射给胰腺肿瘤异种移植小鼠模型时,显示出肿瘤负荷的减轻,与此同时对动物的体重没有影响。
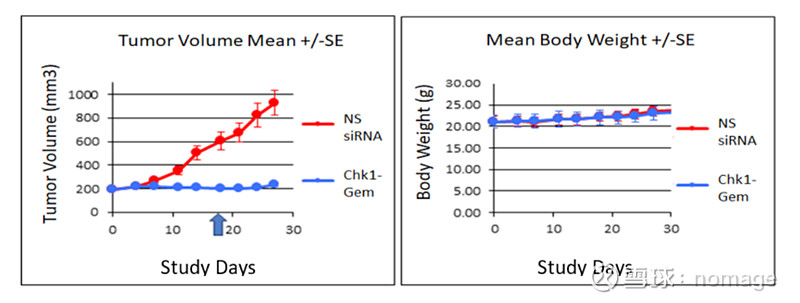
图:含吉西他滨的CHK1 siRNA (PGN6)化学修饰的HKP(+H) (PNP)对小鼠MiaPaca2异种移植瘤的影响
综上,该研究使用一个靶向基因CHK1的寡核苷酸药物缀合物(ODC),包含吉西他滨的CHK1 siRNA双链(STP888),已显示出与小分子吉西他滨诱导抗癌功效的协同作用。结合后,mRNA被降解,最终CHK1的蛋白水平降低 。Sense链被降解,释放吉西他滨,从而观察到协同效应。稳定的化学结构能够直接靶向肿瘤细胞(留下相邻的正常细胞),这将提高疗效并降低毒性。
Sirnaomics发现研究负责人、该出版文章的通讯作者David Evans博士表示:“抗体药物偶联物(ADC)已证明对癌症治疗具有卓越的特异性和疗效。Sirnaomics希望利用其ODC结构的类似优势,提高小分子疗法的效力或持续时间。许多小分子药物最初显示出疗效,但后来由于肿瘤细胞上调某些蛋白质表达而出现耐药性。识别这些蛋白质并设计针对这些靶点的特异性siRNA为克服这些化疗药物诱导的耐药性提供了一种强有力的方法。”
Sirnaomics表示将使用这种结构,与一种抗体(该抗体针对肿瘤中上调但在正常细胞中不上调的标志物)偶联来进行递送。“构建寡核苷酸药物偶联物(ODC)结构将最大限度地减少耐药性,增强化疗药物的疗效,同时降低化疗药物的全身毒性。结合抗体衍生的靶向特性,将为改善癌症治疗提供一种新的药物模式——抗体寡核苷酸药物偶联物(AODC)。”
02
圣诺医药:全球肿瘤RNAi药物的领军企业
Sirnaomics是一家RNA疗法生物制药公司,公司已建立丰富的候选药物管线,候选产品处于临床及临床前阶段。随着公司STP705 和STP707 的临床项目取得多项成功,Sirnaomics目前在推进肿瘤治疗的RNAi药物方面处于国际领先地位。
圣诺医药公司应用在肿瘤领域的核心技术为PNP(peptide nanoparticles)递送平台,该平台旨在解决脂质纳米颗粒(LNP)及传统GalNAc RNAi递送平台的瓶颈。PNP是由人工设计和合成的赖组氨酸多肽共聚物(HKP)构成,HKP是一种可促进siRNA活性成分递送的非活性成分,其包裹在siRNA周围,通过静电和氢键的相互作用缠绕siRNA,自我组装形成PNP。
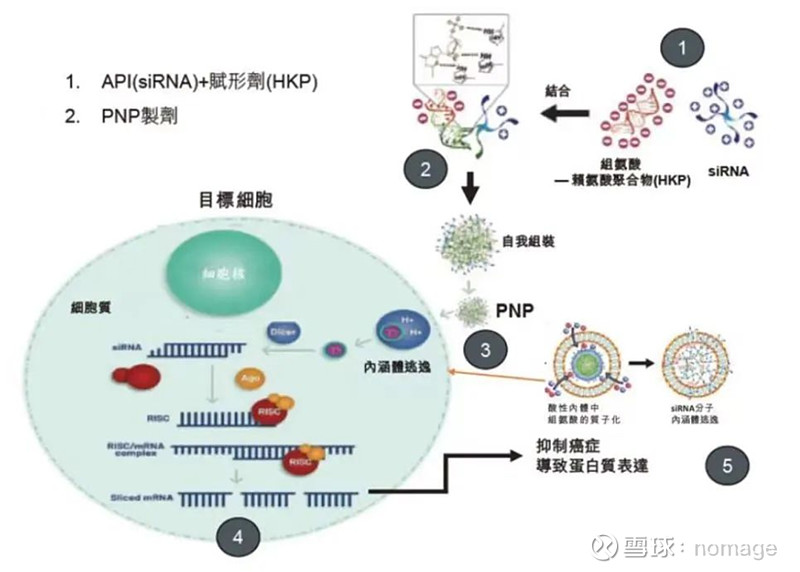
PNP平台
根据insight数据库,圣诺医药在肿瘤领域管线近十项,其中进展最快的STP705用于治疗原位鳞状细胞皮肤癌(isSCC)的II期临床已于2023年完成,进入后期临床研发阶段。
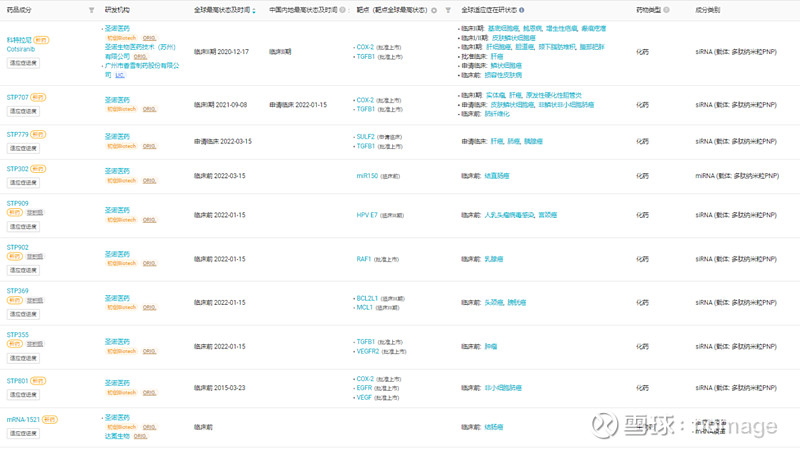
03
小核酸在肿瘤治疗具有独特优势,管线数量庞大
小核酸近年来在多个领域实现突破,也有望在肿瘤领域获得一席之地。通过小核酸技术调控肿瘤细胞关键基因的表达,进而干预肿瘤的正常代谢和细胞生命活动,引起肿瘤细胞凋亡,抑制肿瘤细胞生长,这是极具应用前景的肿瘤治疗方式,既能够进行多基因共同干预,也能同传统治疗方式联合使用。总的来说,小核酸在肿瘤治疗中的优势包括:
1. 基因调控:
通过siRNA技术可以选择性沉默肿瘤抑制基因或促癌基因,如P53、RB、PTEN、RAS、MYC等,从而影响肿瘤细胞的增殖、生存和转移能力。这种基因调控为针对肿瘤的精准治疗提供了新的思路。
2. miRNA的复杂网络:
miRNA在肿瘤中扮演着复杂的调控角色,一个miRNA可以同时调控多个靶基因,而一个靶基因也可以受到多个miRNA的调控。通过研究miRNA的表达和功能,可以深入研究肿瘤的发生和发展机制。
3.纳米粒子递送系统::
小核酸作为药物需要通过合适的载体系统进行递送到肿瘤细胞内。纳米粒子递送系统通过优化结构、表面修饰和靶向性等方面,提高了小核酸的稳定性和靶向性,为肿瘤治疗提供了新的解决方案。
4.个体化治疗的前景:
通过分析患者肿瘤组织或体液中的miRNA表达谱,可以实现个体化的治疗方案。这为患者提供了更有效、更个性化的治疗选择,提高了治疗效果,减少了不良反应。
全球肿瘤小核酸管线数量庞大,根据Frost & Sullivan统计,从临床管线适应症来看,随着小核酸药物研发热情上涨,目前肿瘤已成为小核酸药物临床管线占比最多的适应症,达24%。
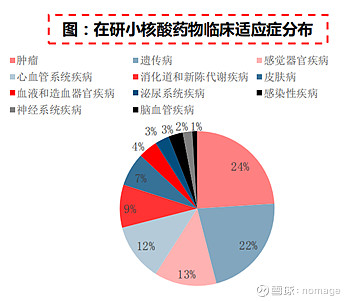
虽然向肿瘤发起冲击的小核酸数量有很多,但是由于存在肿瘤异质性等等难题,有效递送始终难以实现,整体进展缓慢。根据科睿唯安数据库,全球肿瘤小核酸管线共计587个,其中394个(67.1%)处于终止/暂停/无进展阶段,151个(25.7%)处于临床前/基础研究阶段。进展靠前的管线中,有3个(0.5%)处于临床3期及以上,18个(3.1%)处于临床2期,21个(3.6%)处于临床1期。
全球在研肿瘤小核酸发展阶段分布(数据来源:科睿唯安)
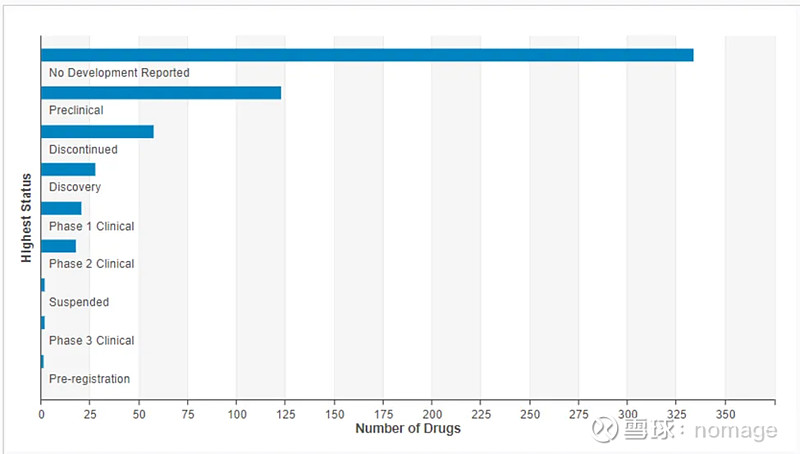
靶点方面,ASO类产品聚焦的靶点更为丰富,数量也更多,如Akt、IGF-1R、STAT3、AR、Hsp27、Bcl-2、TGF-β、PD-1等,都有ASO产品布局;而聚焦于肿瘤领域的siRNA产品,首先从数量来说就略少于ASO,靶点主要有KRAS G12D、TGF-β、HIF-2α、Bcl-2等。
资料来源:
Halami B, Kim W, Ye Z, Neupane N, Bawazir N, et al. (2024) CHK1 siRNA Containing Gemcitabine and Chemically Modified Nucleotides Shows Antitumoral Activityin Vitro and in Vivo. J Oncol Res Ther 9: 10218. 网页链接
Vera Simonenko, Xiaoyong Lu, Eric Roesch, Daniel Mutisya, Chunbo Shao, Qian Sun, Athéna Patterson-Orazem, Marcus McNair, Aranganathan Shanmuganathan, Patrick Lu, David M Evans, A novel siRNA–gemcitabine construct as a potential therapeutic for treatment of pancreatic cancer,NAR Cancer, Volume 2, Issue 3, September 2020, zcaa016, 网页链接
sirnaomics ltd.公司官网、公众号
柏讴生物:小核酸是什么?在肿瘤研究中扮演了什么角色?
贝壳社:突破肿瘤适应症,小核酸药物已箭在弦上!