2023新版国家医保目录 对中药注射液解限,
“中药注射液概念股”王者归来!
更多优选配置,可参看本人开设的雪球栏目:
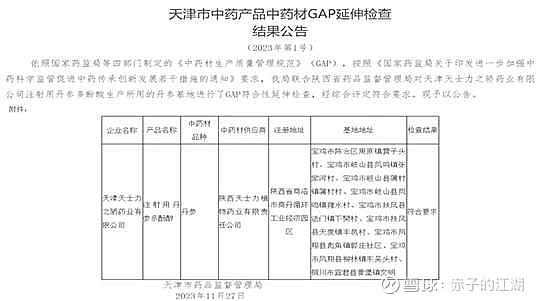
【祝贺丨天士力之骄药业成为全国首家取得中成药产品的中药材新版GAP延伸检查公告生产企业】
津商联合会 2023-12-08 18:05 发表于天津
津商联合会常务副会长单位 天津天士力之骄药业有限公司——注射用丹参多酚酸 丹参药材基地 顺利通过新版GAP符合性延伸检查并正式公告,
成为全国首家开展并通过新版GAP符合性延伸检查的中成药生产企业、全国首家取得新版GAP符合性延伸检查公告的中成药生产企业、天津市第一家顺利通过新版GAP符合性延伸检查并正式公告的药品生产企业。
2022年3月1日国家药监局、农业农村部、国家林草局、国家中医药局正式发布《中药材生产质量管理规范》(简称:新版GAP),进一步推进中药材规范化生产,加强中药材质量控制,促进中药高质量发展。
新版GAP相对比《中药材生产质量管理规范(试行)》(2002年6月1日)(简称:老版GAP)主要变化体现在三个方面:
1、新版GAP以中药生产企业(即中药上市许可持有人)为核心主体来建立并持续完善GAP管理体系并开展GAP符合性延伸检查。
2、借鉴GMP首次引入GAP的管理概念,健全了中药材生产质量管理体系。
3、要求中药材生产全过程关键环节可追溯,“六统一” + “可追溯”成为新版中药材GAP管控关键环节理念的集中体现。
天津天士力之骄药业有限公司作为一家中药注射剂生产企业,
始终视质量为企业的生命,坚持“质量第一、追求卓越”的质量方针,
在天士力医药集团的引领下将“打造中药注射剂第一品牌”作为公司的发展目标,
自产品上市以来一直坚持用GAP的标准来要求和衡量中药材供应商,坚信只有“药材好!药才好!”。
天士力之骄公司自新版GAP颁布之日立即组织中药材供应商开展了GAP体系符合性提升工作并开展了一系列包括中药材基原鉴定、中药材供应商管理模式创新(与供应商签订种植协议)、统一中药材的加工工艺指导原则、统一所供应中药材的内控质量标准、协助供应商建立接受GAP符合性延伸检查的标准流程等关键性工作。
同时组织开展对中药材供应商的反复多轮次的新版GAP符合性内审工作,内审工作克服了疫情的不利影响采用线上线下、远程加现场等多种形式开展,通过对内审自查中的问题的认真研究、反复讨论并咨询专家形成整改方案并有效追踪整改结果,使GAP管理体系持续提升并确保了新版GAP符合性。
2023年4月天士力之骄公司向天津市药监品监督管理局提出GAP符合性延伸检查的申请,
2023年6月份天津市药品监督管理局联合陕西省药品监督管理局并邀请《国家药监局中药材GAP专家工作组》专家共同成立检查组,对注射用丹参多酚酸丹参药材供应商陕西天士力植物药业有限责任公司的基地进行了GAP符合性延伸检查。
检查组对丹参药材的种源、种植、采收、加工、包装、储运等环节开展了现场检查,特别对生产基地管理、种子种苗管理、肥料和农药等投入品管理、种植技术规程、采收与产地加工技术规程、包装与贮存技术规程等对中药材质量有重大影响的关键环节实施重点检查。
最终历经二次现场符合性延伸检查及专家组研讨评估,一致认定符合新版GAP要求。

▲

检查组一行丹参基地现场检查
此次GAP符合性延伸检查也是天士力医药集团持续打造全产业链质量管理的成果体现。
陕西天士力植物药业有限责任公司丹参基地于2003年全国首家通过了原国家食品药品监督管理局的老版中药材GAP认证,并于2009年通过第二次GAP认证,2014年通过第三次GAP认证,2016年国务院取消GAP认证工作,但陕西天士力一直坚持并持续提升GAP管理体系,为此次一次性顺利通过GAP符合性延伸检查奠定坚实基础。
此次顺利通过GAP符合性延伸检查为后续天士力集团相关中药材基地GAP工作奠定发展方向,也为相关中成药产品早日在包装表面增加“中药材符合GAP要求”的标识打下坚实基础,同时进一步提升了中药注射剂质量保障水平。