来源:博药公众号
作者:游游
2023年是抗体药物偶联物(ADC)交易爆发的一年,其中最为引人注目的是辉瑞公司以430亿美元收购Seagen,刷新了ADC领域的交易规模纪录。
ADC领域,辉瑞布局已久。在收购Seagen之前已有2款商业化产品,分别是Mylotarg和Besponsa,来自2009年以680亿美元收购的惠氏(Wyeth)。
收购Seagen后,辉瑞又获得4个已获批ADC产品,包括Adcetris、Padcev、Tivdak、以及合作伙伴荣昌生物开发上市的Disitamab vedotin。同时,Seagen还带来众多临床阶段的ADC管线。另外,辉瑞还从和铂医药引进了一款MSLN靶向ADC。
通过多次交易,辉瑞已成为拥有最多ADC产品的企业。
01
首个ADC
艰难的探索之路
追溯辉瑞研发ADC历史,可以发现FDA批准的首个ADC药物Mylotarg(吉妥单抗)就来自辉瑞,于2000年获FDA加速批准上市,用于CD33阳性AML患者。
不过,后来在临床试验未能继续证实这款药物的临床获益,并且显示其与化疗相比具有更高的毒性后,辉瑞公司主动将该药物撤出美国市场。
2017年,鉴于AML患者的迫切需求,Mylotarg重新获得美国FDA批准,用于AML的成人和2岁及以上儿童患者。
同年,辉瑞的第二款ADC药物Besponsa(inotuzumab ozogamicin,奥加伊妥珠单抗)在欧盟和美国获批上市,用于前体B细胞急性淋巴细胞性白血病。
Besponsa是一种靶向CD22的抗体药物偶联物,由Inotuzumab(伊珠单抗),通过可切割连接子,与ozogamicin偶联而成,属于第三代ADC产品。
但是Besponsa市场表现并不突出,2023年收入2.36亿美元,同比增长7.8%。
此外辉瑞还有不少临床前期的ADC管线,但是亮眼管线不多。
02
430亿美元
成为ADC富翁
Seagen是ADC领域的先驱公司,有着深厚的ADC研发底蕴,以及众多的ADC管线。
迄今为止全球获批上市的ADC药物共16个,Seagen公司拥有3个自主研发的上市ADC,(Adcetris、Padcev、Tivdak),1个合作开发的上市ADC(与荣昌生物联合开发的Disitamab vedotin),还有2款使用了Seagen的ADC技术(Polivy和Blenrep)。
完成收购Seagen后,辉瑞旗下的已上市ADC药物队伍增至6个,成为拥有最多ADC药物的公司。
图1 辉瑞已上市ADC产品(蓝色)
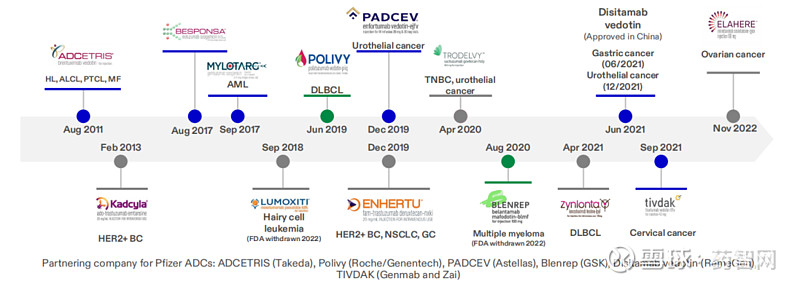
图片来源:辉瑞肿瘤创新日活动PPT
表1. 辉瑞已上市的ADC药物
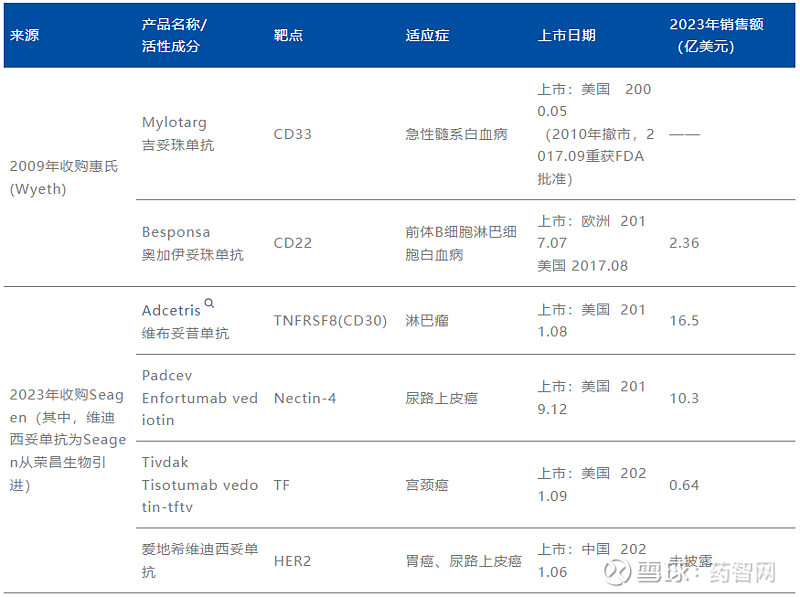
资料来源:辉瑞、博药整理
Adcetris
Adcetris(brentuximab vedotin)是Seagen的首发管线,于2011年首次获FDA批准,用于系统性间变性大细胞淋巴瘤(sALCL)和霍奇金淋巴瘤(HL);于2020年5月,获得我国国家药品监督管理局(NMPA)批准,进入中国市场。
Adcetris是全球第一款获批上市的第二代 ADC 药物,在临床疗效和安全性上都优于第一代。该药由抗CD30单克隆抗体brentuximab和微管破坏剂MMAE(monomethyl auristatin E),通过蛋白酶可裂解连接子(linker)连接。这一连接子在血液循环中保持稳定,被表达CD30的细胞摄入后释放MMAE。
Adcetris上市后商业化表现优秀,销售额逐年增长。2023年Adcetris销售额为16.5亿美元,同比增长12%。
2024年3月13日,辉瑞公布Adcetris联合疗法用于治疗复发/难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)患者的3期试验积极数据。分析显示,与活性对照组相比,接受Adcetris联合疗法患者的总生存期(OS)获得显著改善。辉瑞将与FDA讨论相关的监管递交,如果成功获批,Adcetris 将从较小的市场拓展到DLBCL这一更大的应用市场。
Padcev
Padcev(enfortumab vediotin)是Seagen上市的第二款ADC药物,与安斯泰来联合开发,由靶向nectin-4的全人源性IgG1单抗与MMAE通过可裂解二肽连接子连接。
2019年12月,FDA加速审批Padcev上市,用于接受过PD-1/PD-L1抑制剂和铂类化疗药物的局部晚期或转移性尿路上皮癌治疗,EV-201试验结果显示,相较前期治疗方案Padcev的客观缓解率达44%(55/125)。2021年7月,Padcev获得了FDA完全批准,且将适应症扩展为接受过PD-1/PD-L1抑制剂治疗且不符合顺铂治疗的局部晚期或转移性尿路上皮癌患者。
2023年12月,FDA又提前批准PADCEV联合PD-1单抗K药(帕博利珠单抗)一线治疗局部晚期或转移性尿路上皮癌,成为全球首个获批的“PD-1+ADC”组合疗法。数据显示,联合疗法患者的OS是化疗组患者的近2倍,降低患者死亡风险达53%。
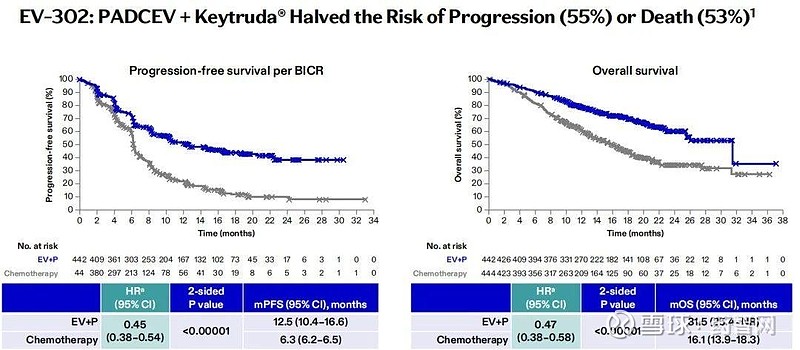
图片来源:辉瑞肿瘤创新日活动PPT
接下来,Padcev将继续向肌层浸润性膀胱癌(MIBC)进军,包括顺铂耐受和顺铂不耐受人群,Ⅲ期研究EV-304和EV-303的数据将在2026年和2027年读出。
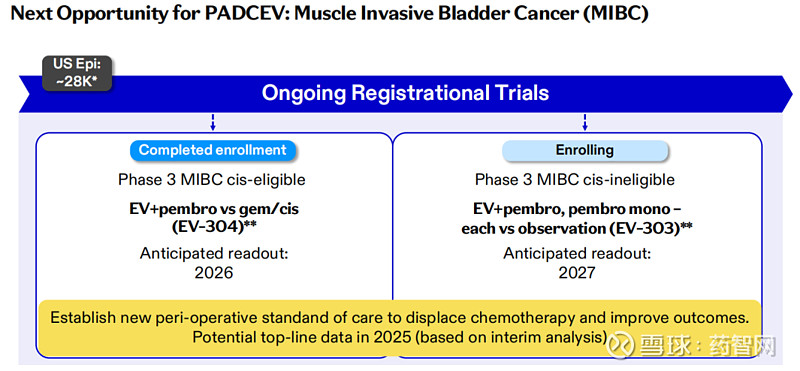
图片来源:辉瑞肿瘤创新日活动PPT
自Padcev获批上市以来,销售额快速增长,2023年销售额迈过10亿美元门槛,达到10.3亿美元。辉瑞高管曾表示,Padcev具有形成“杰出拳头产品”的潜力,认为其年销售额或能超过30亿美元。
03
后劲十足
开发“下一代”ADC平台
在2月底举办的肿瘤创新日活动上,辉瑞宣布,完成Seagen后重组肿瘤部门,将肿瘤药物的开发和商业化纳入一个独立的部门,由公司前研发主管Chris Boshoff领导。
公司将进一步加强ADC药物的开发,正在开发的“下一代”ADC平台,将结合辉瑞的蛋白质工程、抗体设计能力项目和Seagen的ADC技术,瞄准新靶点、改进差异化有效载荷,推出业内最广泛的ADC产品组合。
辉瑞披露的重点推进的临床阶段和临床前的ADC项目有8款。
表2. 辉瑞重点推进的ADC管线
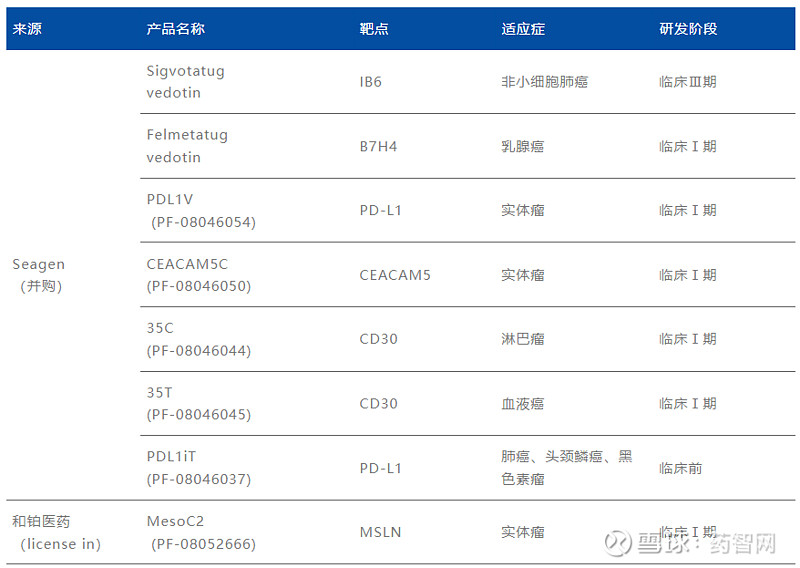
资料来源:辉瑞、博药整理
辉瑞在研ADC中多数来自Seagen的ADC平台,其中进展较快的几款使用与Seagen已上市ADC同样的蛋白酶可切割mc-vc-PABC连接子与MMAE组合,例如:Sigvotatug vedotin、Felmetatug vedotin、PDL1V (PF-08046054)。
Sigvotatug vedotin
Sigvotatug vedotin是一款潜在“first-in-class”整合素β6靶向ADC药物。该药通过对抗体的工程化改造让它对整合素β6(IB6)具有特异性,从而不与其他整合素结合,提高了该ADC的肿瘤选择性。目前正在进行2-3线未经紫杉醇治疗的非鳞状非小细胞肺癌人群的Ⅲ期临床试验,结果预计将在2026或2027年公布。
Felmetatug vedotin
Felmetatug vedotin是一款B7-H4定向vedotin ADC,目前处于Ⅰ期临床阶段,初步结果(SGNB7H4V-001)显示Felmetatug vedotin在乳腺癌和其他实体瘤患者中显示出良好的抗肿瘤活性和可控的安全性。
PDL1V (PF-08046054)
PDL1V是一款潜在“first-in-class”PD-L1靶向ADC。在临床前研究中,该药在PD-L1低表达或表达异质性高的动物模型中也展现出抗癌活性。在PD-L1阳性头颈鳞状细胞癌(HNSCC)患者中进行的Ⅰ期临床试验中,PF-08046054表现出有利的初步疗效。
在下一代ADC中,辉瑞对payload、linker都进行了改进,例如使用新型TOPO1为payload:CEACAM5C (PF-08046050)、35C (PF-08046044)、MesoC2 (PF-08052666);新型Auristatin为payload:35T (PF-08046045);新机制payload:PDL1iT (PF-08046037)。
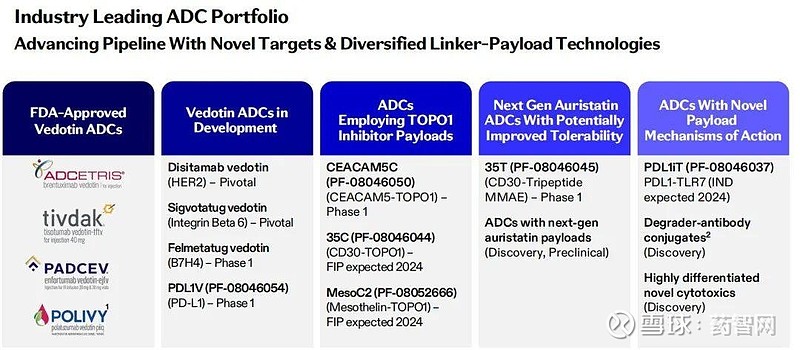
图片来源:辉瑞肿瘤创新日活动PPT
CEACAM5C (PF-08046050)
CEACAM5C是一款CEACAM5靶向ADC,由Seagen和赛诺菲联合开发,使用具有潜在“Best-in-Class”的TOPO1抑制剂,药物抗体比(DAR)为8。PF-08046050在CRC和肺癌PDX模型中展现出了显著的抗肿瘤效果。目前正在进行Ⅰ期剂量递增研究。
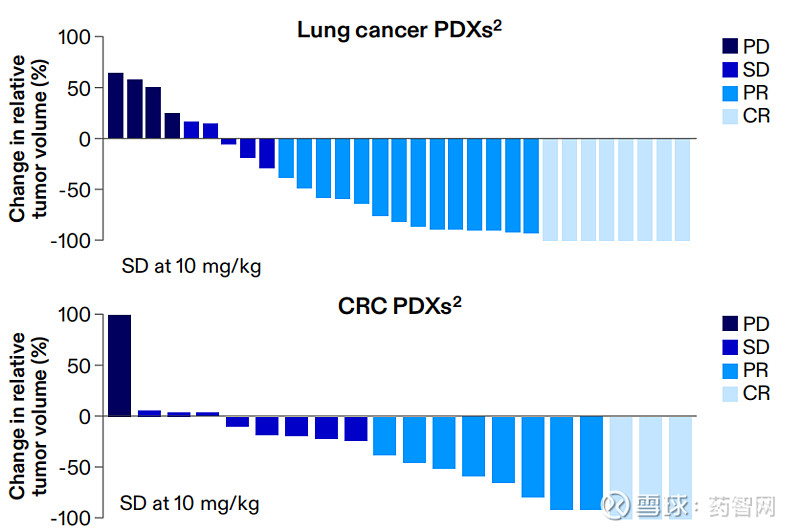
图片来源:辉瑞肿瘤创新日活动PPT
35C (PF-08046044)
35C 是一款CD30靶向ADC,采用了新的TOPO1抑制剂作为payload,临床前展现出更好的耐受性和质量窗口。
MesoC2 (PF-08052666)
MesoC2是一款靶向人间皮素(MSLN)的ADC,来自和铂医药HarbourMice平台产生。2023年12月,辉瑞与和铂医药子公司诺纳生物达成全球权益合作,以5300万美元预付款和近期付款,引进该药。根据协议,诺纳生物获得5300万美元预付款,及最高10.5亿美元里程碑付款和特许权使用费。
35T (PF-08046045)
35T是一款新一代CD30靶向ADC,采用新一代Auristatin为payload,耐受性更好,目前已进入I期临床。
PDL1iT (PF-08046037)
PDL1iT是一款新机制的ADC,旨在向肿瘤微环境递送免疫刺激TLR7激动剂,与PDL1抗体相比,PDL1iT表现出更好的疗效。辉瑞预计将在2024年提交IND申请,目标适应症包括NSCLC、HNSCC和黑色素瘤。
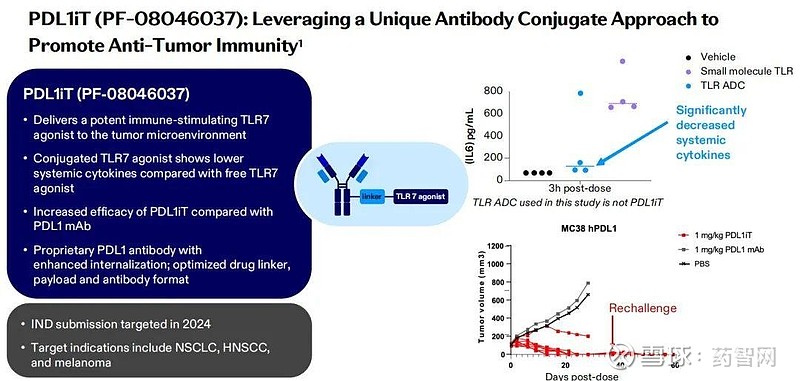
图片来源:辉瑞肿瘤创新日活动PPT
04
小结
辉瑞在ADC领域拥有悠久的历史,曾在2000年推出全球首个ADC药物Mylotarg,但由于安全性和获益问题,2010年无奈撤市;2017年,辉瑞又推出Besponsa,同时带着改良版Mylotarg回归。但或许由于这两个ADC商业回报都不算出色,2023年辉瑞决定并购ADC领域的先驱公司Seagen。
Seagen的加入为辉瑞肿瘤板块注入了强大的活力,带来了三个已上市的ADC产品,其中两个的年销售额更是突破十亿美元大关。不仅如此,Seagen还为辉瑞带来了众多ADC在研管线,通过整合Seagen的研发资源和能力,辉瑞将进一步丰富其ADC产品组合。展望未来,ADC有望成为辉瑞的优势领域,和最重要的收入来源。
参考来源:
1. 辉瑞肿瘤创新日活动PPT
2. BiG生物创新社:Besponsa:辉瑞第二款ADC,这次“命运”会好点吗?
3. Drugs and technology公众号:辉瑞(Pfizer)ADC管线
4. 同写意:买下ADC巨头一年后:辉瑞与它的抗肿瘤王国
博腾股份为全球药企、生物科技公司、科研机构等提供从临床前研究到药品上市全生命周期所需的小分子药物、多肽与寡核苷酸、生物大分子(mAb, ADC等)以及基因与细胞治疗药物等一站式服务解决方案,研发、生产、运营场地覆盖中国(重庆、上海、四川、江苏、江西、湖北)、美国、斯洛文尼亚、比利时、瑞士和丹麦等地。我们致力于以客户为中心,为客户提供卓越的全球化、端到端CDMO服务,让好药更早惠及大众。
声明:本文系药智网转载内容,图片、文字版权归原作者所有,转载目的在于传递更多信息,并不代表药智网立场。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间删除。