来源:博药公众号
作者:游游
凭借Keytruda(K药,帕博利珠单抗)的大获成功,默沙东成为肿瘤领域最为成功的制药企业。根据默沙东2023年报,全年营收601 亿美元,K药全年销售额 250亿美元,占总营收的近乎半壁江山。
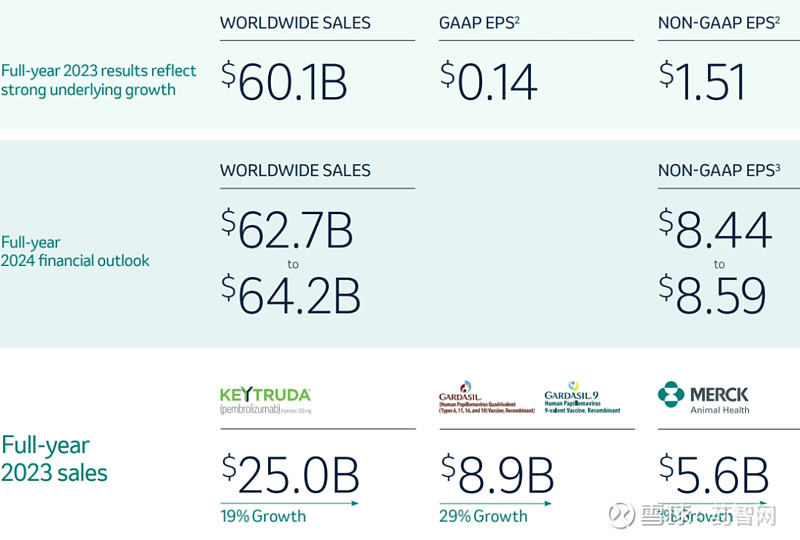
图片来源:默沙东官网
然而,免疫疗法尽管在许多癌症治疗中展现出显著效果,但其局限性亦不容忽视。其最大缺陷是,仅在少数癌种应答率较高。因此,默沙东不断探索K药的联合疗法,拓展K药的应用场景。另一方面,K药的核心专利将在2028年到期,默沙东亟需寻找下一个肿瘤领域的“重磅炸弹”,以维持其在肿瘤领域的市场领导地位。
01
联合疗法
PD-1+ADC展现潜力
截至目前,K药在美国已获批45项适应症,涉及18个癌种。2018年,K药获批在中国上市,目前在国内获批适应症已达到13项,包括单药或联合用药治疗黑色素瘤、非小细胞肺癌、食管癌、头颈部鳞状细胞癌、结直肠癌等。
在联合用药方面,默沙东探索过其与化疗、免疫抑制剂、溶瘤病毒、ADC、mRNA等各类型药物的联合应用。
其中,K药+化疗是探索最充分还是获得监管机构批准最多的联合疗法。早在2017年5月,FDA就批准了K药联合培美曲塞、卡铂、一线治疗转移性非鳞状非小细胞肺癌(NSCLC)。此后又有多种K药+化疗联合方案获得监管机构批准。但这并不适用于所有癌种,例如在KEYNOTE-361试验中,K药在标准化疗背景上未能击败化疗改善晚期膀胱癌患者的OS和PFS。
此外,K药与卫材的仑伐替尼组成的“可乐疗法”曾是PD-1联合疗法中备受关注,获FDA批准用于多个适应症,包括肾细胞癌、子宫内膜癌等,不过后来该组合疗法相继在多项3期临床中折戟,蒙上了失败的阴影。
ADC在肿瘤组织中极大扩大了细胞毒素的治疗窗口,并且可以有效减少全身化疗导致的毒副反应。如果将K药与ADC联用,有望实现比与化疗、靶向疗法联用更好的效果。
12月15日,默沙东宣布FDA提前批准了K药(帕博利珠单抗)联合Nection-4 ADC(Padcev)一线治疗局部晚期或转移性尿路上皮癌,这是全球首个获批的“PD-1+ADC”组合疗法。

图片来源:默沙东官网截图
Padcev为全球首款获批上市的 Nectin-4 ADC,此前已获批单药用于治疗既往接受过 PD-1/PD-L1 抑制剂和含铂化疗治疗的局部晚期或转移性尿路上皮癌(la/mUC)患者。此次获批的是与 K 药的联合疗法。数据显示,联合疗法患者的OS是化疗组患者的近2倍,降低患者死亡风险达53%。
与Padcev联用,只是默沙东K药+ADC联用策略的首个里程碑,默沙东正在开展多个K药+ADC的临床研究:
2020、2021年,默沙东与第一三共/阿斯利康达成3项临床合作 TROPION-Lung02 、TROPION-Lung07 和 TROPION-Lung08 研究,旨在评价 Dato-DXd(Trop2 ADC)和 K 药联合治疗NSCLC的疗效。
2021年,默沙东与吉利德达成合作协议,共同推进K药和Trodelvy(Trop2 ADC)一线治疗三阴乳腺癌。2022年,默沙东又与吉利德签订了两项临床试验合作和支持协议,以评估Trodelvy与Keytruda联用一线治疗NSCLC的疗效。
2023年,默沙东与科伦博泰共同宣布多项 SKB264+K 药联合疗法即将启动包括肺癌、乳腺癌在内的国际多中心3期临床试验。2024年2月,默沙东宣布 SKB264联合K药用于PD-L1表达大于或等于50%的转移性NSCLC的关键 3 期临床试验已启动。
在看到相应临床释放出积极信号之后,默沙东更加看好ADC的潜力,不仅要开拓K药与其他企业的ADC的联用方案,还要拥有自己的ADC。
02
全力布局
400亿美元快速打造ADC军团
在去年的投资者会议上,默沙东将其肿瘤学管线分为3类:K药为代表的肿瘤免疫疗法,以LYNPARZA(奥拉帕尼)、LENVIMA(仑伐替尼)为代表的精准靶向疗法,以及以ADC为代表的组织靶向疗法。
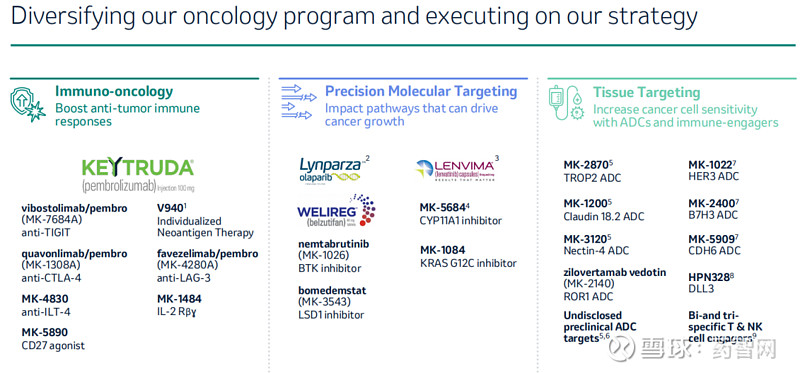
图片来源:默沙东2023Q4 PPT
目前两类都已有畅销药诞生,而组织靶向疗法尚缺少商业化产品。但从近期的频频动作可以看出,默沙东正在倾斜资源,大力布局这一领域。
默沙东首次布局ADC在2020年9月,与Seagen达成合作,共同开发LIV-1 ADC药物ladiratuzumab vedotin、并对Seagen进行10亿美元的股权投资。此后曾试图通过大收购扩增ADC管线;但2022年在“错失”对Seagen的收购后,转而瞄准科伦博泰、第一三共的ADC技术平台,通过多次合作快速扩充ADC管线。
表1 默沙东在ADC领域的交易汇总
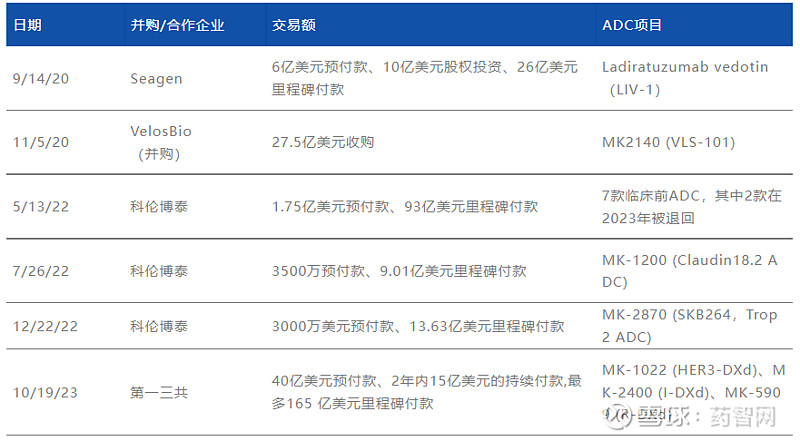
资料来源:博药根据企业公开信息整理
几次大手笔交易让默沙东以近400亿美元快速纳入12款在研ADC管线。根据默沙东最新公开的资料,有7个ADC管线正在积极推进临床研究。
表2 默沙东临床阶段的ADC项目概况
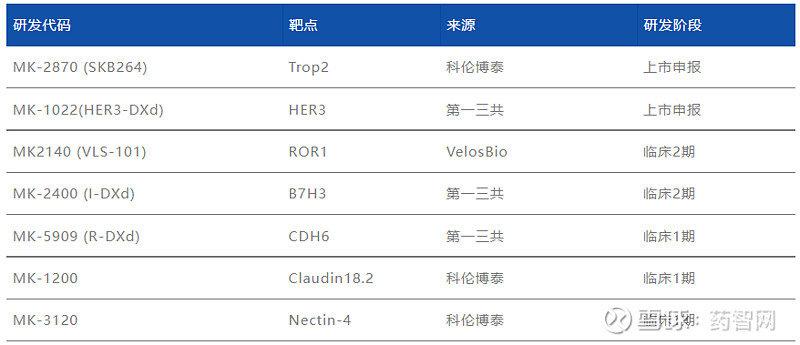
资料来源:博药根据企业公开信息整理
这7个ADC来自3个技术平台,分别靶向7个靶点,有利于互补和分散风险,下面对每个项目做简要介绍。
MK-2870(SKB264)
来自科伦博泰的ADC研发平台—OptiDC研发,由具有高亲和力和靶向性的人源化抗TROP2单抗,通过稳定性经过优化的CL2A连接子与自研毒素小分子T030(拓扑异构酶Ⅰ抑制剂)结合而成,药物抗体比(DAR) 7.4。
目前默沙东围绕SKB264已启动三项关键3期临床试验,包括 SKB264单药一线治疗EGFR突变的晚期或转移性NSCLC,单药二线治疗子宫内膜癌(EC),以及与K药联合一线治疗PD-L1高表达(TPS≥50%)的转移性NSCLC。
吉利德的Trodelvy是全球首款Trop2 ADC,但在非小细胞肺癌3期临床失利。SKB264已启动两项针对NSCLC的3期临床,有望率先在肺癌领域取得突破。
MK-1022(HER3-DXd)
采用第一三共独有的DXd ADC技术设计,由全人源化抗HER3 IgG1单克隆抗体通过可裂解四肽连接子与拓扑异构酶I抑制剂有效载荷(一种依喜替康衍生物,DXd)连接组成。
2023年12月,HER3-DXd的生物制品许可申请(BLA)获美国FDA受理并授予优先审评资格,用于治疗既往接受过两种或两种以上全身治疗的局部晚期或转移性EGFR突变非小细胞肺癌(NSCLC)成人患者。《处方药使用者付费法案》(PDUFA)日期为2024年6月26日。
此次BLA基于HERTHENA-Lung01研究结果:HER3-DXd对225例既往接受EGFR TKI和含铂化疗后出现病情进展的EGFR突变局部晚期或转移性NSCLC患者产生持久且具有临床意义的疗效,客观缓解率(ORR)为29.8%(95% CI:23.9~36.2),其中包含1例完全缓解(CR),66例部分缓解(PR)。中位缓解持续时间(DOR)为6.4个月(95% CI:4.9~7.8)。
MK2140(VLS-101)
来自VelosBio公司,又名Zilovertamab vedotin,靶向ROR1的单克隆抗体与甲基澳瑞他汀E(MMAE)连接而成。FDA曾授予MK2140治疗套细胞淋巴瘤(MCL)的孤儿药资格和快速通道资格。
在ESMO 2021上,默沙东公布了MK-2140治疗淋巴系统恶性肿瘤患者的I期、首次人体剂量递增研究结果。数据显示,候选药在15名套细胞淋巴瘤患者中的7名中诱导了肿瘤客观缓解(ORR为47%),其中4名部分缓解,3名完全缓解。在5名弥漫性大B细胞淋巴瘤患者中,3名达到客观缓解(ORR为60%),其中1名部分缓解,2名完全缓解。根据Clinicaltrials.gov官网显示,MK-2140目前正在全球开展多项Ⅱ/Ⅲ期临床研究,其中,针对复发性或难治性弥漫大B细胞性淋巴瘤(DLBCL)适应症的Ⅱ/Ⅲ期多中心临床试验已经于2021年12月启动。
MK-2400(I-DXd)
采用第一三共独有的DXd ADC技术设计,由人源化抗B7-H3 IgG1单克隆抗体通过可裂解四肽连接子与拓扑异构酶I抑制剂有效载荷(一种依喜替康衍生物,DXd)连接组成。
目前I-DXd正在名为IDeate-01的2期临床试验中接受评估,用于治疗既往接受过治疗的广泛期小细胞肺癌(SCLC)患者。在IASLC 2023世界肺癌大会上,第一三共公布了DS-7300治疗SCLC的1/2期试验亚组分析的更新结果。数据显示,I-DXd的客观缓解率达52.4%,中位无进展生存期为5.6个月,中位总生存期达12.2个月。
MK-5909(R-DXd)
采用第一三共独有的DXd ADC技术设计,由人源化抗CDH6 IgG1单克隆抗体通过可裂解四肽连接子与多个拓扑异构酶I抑制剂有效载荷(一种依喜替康衍生物,DXd)连接组成。
DXd正在进行治疗既往接受过治疗的卵巢癌患者的I期研究。在ESMO 2023大会上,第一三共公布了首次人体I期研究亚组分析结果,R-DXd在治疗既往接受过多种治疗的卵巢癌患者中观察到令人鼓舞的客观缓解率达46%和98%的疾病控制率,缓解持续时间为11.2个月。
MK-1200(Claudin18.2 ADC)
来自科伦博泰的ADC研发平台,是靶向Claudin 18.2的第三代ADC药物,采用了一种拓扑异构酶I (TOPO1)抑制剂毒素,其DAR 值为7.8。目前处于临床1期阶段。
MK-3120(Nectin-4 ADC)
来自科伦博泰的ADC研发平台,是靶向Nectin-4的ADC。科伦博泰在2023年4月启动了该药的 I 期临床试验,用于晚期实体瘤受试者的安全性、耐受性、药代动力学和初步疗效。
02
小结
目前K药是默沙东最重要的收入来源,占默沙东总营收的41.6%,这也意味一旦K药上演“专利悬崖”,默沙东业绩将会遭遇极大挑战。目前来看,ADC就是默沙东看重的下一个肿瘤领域接棒产品,为此不惜重金引进多款ADC资产。从已公布的临床阶段ADC来看,7个项目7个靶点,几乎涵盖了所有ADC热门靶点和潜力靶点,而且这些项目来自3个ADC技术平台,有利于互补和规避风险。除了默沙东,近几年其他制药巨头也在纷纷“抢购”ADC项目,辉瑞430亿美元收购Seagen、艾伯维101亿美元并购ImmunoGen、阿斯利康、GSK、强生等企业都曾重金引入ADC项目。
过去,默沙东凭借Keytruda引领了肿瘤免疫治疗,成为抗肿瘤领域最成功的药企。在备受瞩目的下一个肿瘤治疗领域的新星——ADC疗法,默沙东又率先拿下首个获批上市的PD-1+ADC联合疗法,并布局了丰富的ADC管线。未来,默沙东能否继续在肿瘤领域保持领先地位,我们拭目以待。
参考资料:
默沙东2023年报
科伦博泰生物:科伦博泰与默沙东就核心产品SKB264(MK-2870)的合作触发相关临床里程碑付款
第一三共:HER3-DXd在美国获得优先审评资格,用于治疗既往接受过治疗的局部晚期或转移性表皮生长因子受体(EGFR)突变非小细胞肺癌患者
第一三共:I-DXd在晚期小细胞肺癌患者的早期临床研究中表现出持久疗效
第一三共:Raludotatug Deruxtecan在治疗晚期卵巢癌患者的早期研究中持续显示出具有前景的临床疗效
博腾股份为全球药企、生物科技公司、科研机构等提供从临床前研究到药品上市全生命周期所需的小分子药物、多肽与寡核苷酸、生物大分子(mAb, ADC等)以及基因与细胞治疗药物等一站式服务解决方案,研发、生产、运营场地覆盖中国(重庆、上海、四川、江苏、江西、湖北)、美国、斯洛文尼亚、比利时、瑞士和丹麦等地。我们致力于以客户为中心,为客户提供卓越的全球化、端到端CDMO服务,让好药更早惠及大众。
声明:本文系药智网转载内容,图片、文字版权归原作者所有,转载目的在于传递更多信息,并不代表药智网立场。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间删除。