中华医学会儿科学分会肾脏学组 中华儿科杂志编辑委员会 张爱华,罗小平
儿童慢性肾脏病(CKD)已成为影响儿童健康的重要慢性疾病之一,合并生长障碍是CKD患儿特有的并发症之一,生长障碍影响患儿身体和心理健康。规范评估CKD患儿生长水平有助于制订合理的治疗策略,对延缓患儿肾脏病变进程、改善其生活质量等具有重要意义。中华医学会儿科学分会肾脏学组组织专家组及成员通过借鉴国内外相关领域经验,结合我国儿童CKD生长障碍诊治现状,制订我国儿童CKD生长障碍诊治循证指南,旨在指导和帮助儿童肾脏科医师在临床中对CKD合并生长障碍患儿进行规范诊治,改善CKD患儿的生长发育,提升生活质量。
儿童慢性肾脏病(chronic kidney disease,CKD)已成为影响儿童健康的重要慢性疾病之一,不同国家和地区儿童CKD的发病率差异较大,总体上儿童CKD发病率为(2.8~15.8)/100万,其中现有CKD登记注册系统中大部分为终末期肾病(end stage kidney disease,ESKD)。近年来,多项研究报道儿童CKD和ESKD的发病率呈逐年上升趋势。我国1项91家医院参与的调查报告显示,CKD G3期及以上者在泌尿系统疾病的构成比逐年升高,2002年较1990年增长了1.3倍,人数年平均增长13.67%。儿童CKD及并发症的早期诊断和治疗是改善预后的关键。儿童CKD可合并多种并发症,其中生长障碍是CKD患儿特有的并发症之一。北美儿科肾脏移植合作研究组织报告显示,36.9%的CKD患儿存在生长障碍,严重影响患儿身心健康及预后,我国尚缺乏CKD患儿合并生长障碍的流行病学数据。近年来,尽管青春期前需要肾脏替代治疗的CKD患儿身高较过去有明显改善,但仍有40%患儿成年后身材矮小。此外,随着医疗水平和国民生活水平的提高,医生和患儿家属愈加关注如何提高患儿的生活质量。因此,正确、规范评估CKD患儿生长水平有助于制定合理的治疗策略,对延缓患儿肾脏病变进程、改善其生活质量等具有重要意义。儿童CKD生长障碍的诊治经验大多来自国外文献报道,尚缺乏适合我国国情、具有指导意义的指南。中华医学会儿科学分会肾脏学组组织专家组及成员通过借鉴国内外相关领域经验,结合我国儿童CKD生长障碍诊治现状,联合中华儿科杂志编辑委员会制定“儿童CKD生长障碍诊治循证指南”(以下简称本指南),旨在指导和帮助儿童肾脏科医师在临床中对CKD合并生长障碍患儿进行规范诊治,改善CKD患儿的生长发育水平,提升生活质量。资金支持由中华国际医学交流基金会公益基金和江苏省社会发展基金提供,用于专家咨询以及共识会议的召开。
一、指南编写的方法
1.证据来源:检索PubMed、Embase、Cochrane Library、Web of Science、中国生物医学文献服务系统、中国知网、万方全文数据库等中英文数据库发表的相关文献,以及检索国际指南联盟、英国国家临床医学研究所、改善全球肾脏病预后组织(Kidney Disease:Improving Global Outcomes,KDIGO)等网站发布的专家共识和指南。中文检索词包括“儿童”“慢性肾脏病”“矮小”“生长发育迟缓”“生长发育障碍”等,英文检索词包括“children”“pediatric”“chronic kidney diseases”“end-stage renal disease”“growth”等,以逻辑符号组合相关检索式。语种限制为中文或英文,涉及的研究对象≤18岁,研究类型为系统评价或Meta分析、随机对照试验(randomized controlled trial,RCT)、队列研究、病例对照研究等。检索时间为从建库到2021年12月。
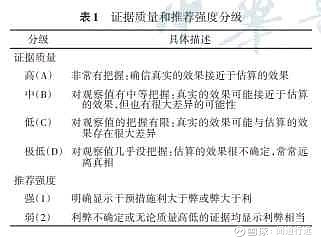
2.证据质量分级和强度分级:采用推荐意见分级评价、制订与评估方法评价各临床问题证据体的质量(表1)。推荐强度根据证据质量、利弊平衡等最后形成推荐意见。
3.指南的制定方法:制订工作由儿童肾脏病学、内分泌学、消化学、流行病学等多个学科的专家共同完成,指南的设计和规划参考“中国制订/修订临床诊疗指南的指导原则(2022版)”。指南工作组召开多次会议,对每个具体的临床问题和干预措施进行了充分的讨论。最终所有推荐意见通过投票表决。对持续存在分歧的部分,推荐或反对某一干预措施至少需要获得50%的参与者认可,且持相反意见的参与者比例需低于20%,未满足此项标准将不产生推荐意见。推荐意见被列为强推荐而非弱推荐,则需要得到至少70%的参与者认可。本指南已在国际实践指南注册与透明化平台进行注册(PREPARE-2022CN427)。
4. 指南的发布、传播与更新:指南发表后将以学术会议、学习班等形式在全国范围进行传播,促进指南在临床上被广泛使用,以助指导临床实践。指南制订工作组将定期进行文献检索、证据更新和评价,计划每3~5年对指南进行更新。
二、儿童CKD合并生长障碍概况
1.儿童CKD的定义和分期:2012年KDIGO临床实践指南将CKD定义为肾脏结构或功能异常持续超过3个月,并影响患者健康。CKD判定标准为肾小球滤过率(glomerular filtration rate,GFR)下降[GFR<60 ml/(min·1.73 m2)]或存在以下1条或以上且持续时间超过3个月:(1)蛋白尿(尿白蛋白排泄率≥30 mg/24 h,尿白蛋白肌酐比值≥30 mg/g);(2)尿沉渣异常;(3)由于肾小管原因导致的电解质和其他异常;(4)组织学检测异常;(5)影像学检测结构异常;(6)肾脏移植病史。GFR<60 ml/(min·1.73 m2)的标准不适用于2岁以下儿童。依据GFR水平,儿童CKD分为G1~G5期。因CKD患儿存在身高及性别差异,估算肾小球滤过率(estimated glomerular filtration rate,eGFR)公式多采用Schwartz公式。即儿童eGFR[ml/(min·1.73 m2)]=K ×88.4×身高/血清肌酐,身高单位为cm,血清肌酐单位为μmol/L,根据血清肌酐不同的检测方法有不同K值。Jaffe′s法测定血清肌酐0~28日龄K=0.33,>28日龄~1岁K=0.45,2~12岁K=0.55,12岁以上的男性K=0.77,12岁以上的女性K=0.55;酶法测定血清肌酐K=0.413。
2.儿童CKD合并生长障碍的病因:儿童CKD生长障碍与多种因素相关,包括宫内生长受限、父母身高、原发性疾病、营养状况、出生因素如早产、生长激素-胰岛素样生长因子-1轴紊乱等。CKD并发症如矿物质和骨异常(mineral and bone disorders,MBD)、代谢性酸中毒、贫血、水和电解质紊乱也可能影响CKD患儿生长障碍。此外,药物如长期应用外源性糖皮质激素也会影响生长发育。
三、儿童CKD合并生长障碍评估策略
(一)生长评估指标
推荐意见1:CKD患儿应定期评估身高,当身高低于同种族、同年龄、同性别正常儿童平均身高2 s或低于P3时,考虑为生长障碍(1A)。
生长和发育是儿童区别于成人的重要特点,各年龄阶段儿童生长速度不同,在一定范围内受遗传、环境影响,存在相当大的个体差异。因此儿童生长的水平有一定的正常范围。2008年制定的“矮身材儿童诊治指南”中,将生长障碍定义为身高低于同种族、同年龄、同性别正常儿童平均身高2 s或P3(-1.88 s)。CKD患儿生长水平评估指标包括身高、体重、生长速率、生长潜力。应定期进行规范化监测,校正年龄和性别后,与参考值进行比较。我国多为3岁以下婴儿测量身长,3岁以上测量身高。早产儿身长评估时应考虑胎龄,如无法评估站立高度,可使用仰卧长度测量方式。年龄较大的儿童可使用壁挂式测距仪测量站立高度。建议采用中国0~18岁儿童生长参照标准及生长曲线进行评价,婴幼儿阶段尤其是母乳喂养婴幼儿也可采用世界卫生组织(World Health Organization,WHO)生长标准。
推荐意见2:CKD患儿应进行生长速率评估,当生长速率低于儿童生长速率参考值的P25时,考虑为生长障碍(1A)。
生长速率即身高和体重的月平均增长速度,需定期检查,连续测量。生长速率可以清晰记录儿童个体发展轨迹,对识别儿童不良生长情况、及时发现儿童偏离自身发育轨迹情况具有重要价值。2009年首都儿科研究所生长发育研究室牵头制定了“中国0~18岁儿童、青少年身高、体重的标准化生长曲线”,研究表示男童15岁、女童13岁之前,中国儿童身高略高于美国及WHO标准,之后逐渐低于美国及WHO标准,18岁时男童身高低于美国3.5 cm,女童低于美国2.5 cm,作为我国儿童青少年的生长参照标准,用于生长速率的评估,当儿童生长速率低于参考值的P25时,考虑为生长障碍。
推荐意见3:CKD患儿可根据左手腕关节X线片腕骨骨骺的开放程度,评估生长潜力(1C)。
常用左手腕关节X线片检查,评估左手腕骨骨骺的开放程度,从而评估生长潜力。临床常用的遗传身高预测方法包括:(1)CMH计算公式,男孩遗传身高(cm)=(父亲身高+母亲身高+13)/2,女孩遗传身高(cm)=(父亲身高+母亲身高-13)/2;(2)FPH公式,男孩遗传身高(cm)=45.99+0.78(父亲身高+母亲身高)/2±5.29,女孩遗传身高(cm)=37.85+0.75(父亲身高+母亲身高)/2±5.29。
(二)生长评估频率
推荐意见4:根据患儿年龄和CKD分期个体化监测患儿生长水平,病情较重者需要增加监测频率(1A)。
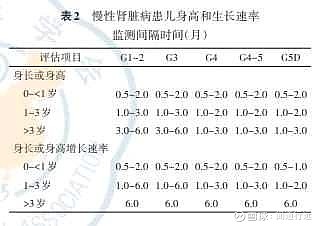
参照2019年欧洲肾脏病学会制定的儿童CKD生长激素使用指南推荐,监测频率应基于患儿年龄和CKD分期,见表2。病情较重,发育迟缓、合并其他疾病(中枢神经系统疾病、肝脏疾病或心脏疾病等)的患儿需要增加监测频率。
四、儿童CKD合并生长障碍的治疗
儿童CKD生长障碍与多种因素相关,需要进行全面综合评估,明确影响患儿生长的相关因素,再给予适当的治疗措施。
(一)改善营养状况
推荐意见5:合并生长障碍的CKD患儿的能量摄入应与同龄儿相仿,并根据体重和生长增减速度进行调整(2D)。CKD G2~5D期患儿的目标蛋白质摄入量为建议膳食摄入(suggested dietary intake,SDI)上限,不应低于SDI下限,以促进最佳生长(2D)。透析患儿蛋白质摄入量可高于非透析患儿,以弥补透析时蛋白质的损失(2D)。对于血尿素水平持续偏高的患儿,在排除其他导致血尿素水平升高的原因后,将蛋白质摄入量调整至SDI下限(2D)。
营养不良是CKD患儿生长障碍的主要原因之一,且与CKD进展、心血管事件及死亡事件相关。我国1项调查数据显示,CKD患儿营养不良发生率高达58.5%,其中生长迟缓的比例约占45%,CKD患儿病程越长、分期越高,发生营养不良的风险越高。Rees等对来自18个国家153例受腹膜透析的2岁以内的CKD患儿进行回顾性分析发现,胃造瘘喂养可显著改善患儿营养不良,促进患儿线性生长。因此口服不能满足营养需求时可给予部分或完全肠内营养管饲,以改善营养状况。1项观察性研究表明,在CKD患儿2岁后至青春期前进行肠内营养管饲可改善身高和体重,且年龄较小的患儿和未接受透析治疗的患儿受益更大。营养治疗主要包括能量、蛋白质、液体和无机盐4个方面。
多项研究表明,CKD患儿在接受健康同龄儿童推荐的膳食能量摄入量,可正常生长。对于体重和生长不理想的患儿建议能量摄入在推荐范围的上限。蛋白质是细胞和器官维持正常功能的基本组成部分。当肾功能下降时,蛋白质摄入过多会导致肾脏高滤过,同时蛋白质分解产生的产物会体内蓄积,从而损伤靶器官。但低蛋白质饮食可能会导致营养不良、发育不良和蛋白质能量消耗,应避免在CKD早期限制蛋白质摄入。1项RCT研究证明,CKD患儿低蛋白饮食可显著降低生长速率。但另1项荟萃分析研究显示,低蛋白饮食对患儿生长发育的危害存在不确定性。CKD G2~5期患儿的蛋白质摄入应不低于同龄儿推荐摄入量低限;对于透析患儿,因透析过程中有部分蛋白丢失,这类患儿蛋白质的摄入应高于非透析患儿;但对于血尿素持续增高的CKD患儿,除外脱水、糖皮质激素等因素,蛋白质摄入应为同龄儿推荐摄入量的低限。2020年国际儿童肾脏营养组制定了儿童CKD G2~5期的能量和蛋白质摄入推荐,具体需结合我国儿童营养状况进一步综合评估。
(二)纠正贫血
推荐意见6:合并生长障碍的CKD患儿,需纠正贫血(2D)。
贫血是儿童CKD常见的并发症之一,贫血对生长发育的影响仍存有争议。2019年1项关于欧洲CKD患儿生长障碍的多中心队列研究显示,贫血对生长发育的影响较小。但Boehm等通过队列研究发现予重组人促红细胞生成素纠正贫血,可改善CKD患儿的生长发育。因此仍建议对于伴生长障碍的CKD患儿,需积极纠正贫血。
(三)纠正CKD-MBD
推荐意见7:合并生长障碍的CKD患儿,需纠正钙磷代谢紊乱,纠正继发性甲状旁腺功能亢进(2D)。
CKD-MBD是儿童CKD的常见并发症之一,因为肾功能下降而引起矿物质和骨代谢异常,多认为临床可引起生长发育落后,但欧洲的多中心研究显示CKD-MBD对生长发育的影响较小,尚缺乏有力证据证实CKD-MBD可引起生长发育落后。但国外指南均建议在使用生长激素前需纠正继发性甲状旁腺功能亢进。因此,对于伴生长障碍的CKD患儿,仍建议需积极维持正常的血钙、血磷和纠正继发性甲状旁腺功能亢进。
(四)提高透析充分性
推荐意见8:合并生长障碍的CKD透析患儿,需提高透析充分性(1C)。
多项对照实验发现延长血液透析时间、频率,每日透析、血液透析滤过相比血液透析可促进CKD患儿追赶生长,提高透析充分性可提高生长激素敏感性。此外,1项对比3种不同透析方式对CKD患儿生长影响的研究发现,与自动腹膜透析机行间歇性腹膜透析及传统血液透析相比,接受连续非卧床腹膜透析的患儿生长更好,实际年龄身高增加量标准差评分最佳,此外还可促进葡萄糖吸收补充能量,连续非卧床腹膜透析以及其他延长留腹时间的每日腹膜透析方式,对于年龄更小的正在透析、等待移植的患儿来说可能更利于生长。
(五)补充外源性生长激素
推荐意见9:合并生长障碍的CKD G3~5期患儿,在改善营养状况、纠正贫血、纠正继发性甲状旁腺功能亢进、纠正代谢性酸中毒、提高透析充分性等基础上,如动态评估后仍存有生长障碍可考虑加用外源性生长激素(1A)。在接受肾移植的CKD患儿,如果1年内没有追赶生长,可在移植1年后开始生长激素治疗(1A)。
自20世纪90年初开始有多项RCT、队列研究结果表明生长激素治疗可有效提高CKD患儿生长速率,改善身高。1项关于CKD患儿应用生长激素的Meta分析显示,纳入10项RCT研究共481例患儿,给予补充生长激素可显著提高患儿生长速率,且大剂量组[28 U/(m2·周)]较小剂量组[14 U/(m2·周)]年身高增长1.4 cm(0.6~2.2 cm)。另1项关于CKD肾移植后患儿的Meta分析显示,纳入5项RCT研究共378例患儿,肾移植后患儿使用生长激素亦可显著提高生长速率。2012年Cochrane 系统综述纳入了16项RCT,结果显示给予生长激素治疗组,身高显著改善、生长速率增快,且给药1年后虽生长速率低于给药1年内的生长速率,但仍高于对照组。因此对于青春期前的CKD患儿,无论是否透析或肾移植,若出现生长障碍,可考虑补充重组人生长激素以促进患儿追赶生长,生长激素治疗对终身身高有益。但由于仅2项RCT研究纳入CKD G2期的患儿,所以主要对合并生长障碍的CKD G3~5期患儿提出推荐意见。此外,对G3~5期的年龄大于6月龄的CKD患儿包括透析患儿,身高在P3~P10,如生长速率低于P25,在其他可能导致生长障碍的相关因素得以纠正后,也可以考虑使用生长激素(2D)。
此外,对于肾移植患儿,多项RCT研究显示尽早减停激素可显著促进追赶生长,外源性生长激素的补充也可以促进患儿追赶生长。考虑到患儿肾移植术后尽早停用激素可出现追赶生长,建议如果1年内没有追赶生长,可在移植1年后开始生长激素治疗。
推荐意见10:在使用生长激素前,需与患儿家长充分讨论使用生长激素的利弊和经济成本效益,同时需充分评估患儿病情,严格掌握生长激素的适应证、禁忌证、停药指征等(2D)。
对于CK患儿在使用生长激素前需充分评估病情,且与家长充分沟通讨论。生长激素治疗前评估、禁忌证、治疗方案、停药指征参照于2008年定的“矮身材儿童诊治指南”、2013年“基因重组人生长激素儿科临床规范应用的建议”和2019年欧洲肾脏病学会制定的儿童CKD生长激素使用指南。
生长激素治疗前建议评估(1)生长水平(身高或身长、体重、生长速率和生长潜力、左腕关节X线片、遗传身高和矮小症相关检查);(2)肾脏指标(eGFR、血清肌酐、尿素氮);(3)钙磷代谢相关指标(血清钙、磷、甲状旁腺激素、碱性磷酸酶和25-羟基-维生素D);(4)血清白蛋白、血红蛋白、血气分析;(5)血糖水平(包括糖化蛋白);(6)甲状腺激素水平;(7)胰岛素样生长因子1 和胰岛素样生长因子结合蛋白3水平 ;(8)垂体磁共振成像;(9)眼底检查;(10)肿瘤标志物,如甲胎蛋白、癌胚抗原等。
存在生长激素治疗禁忌证的CKD患儿应避免使用生长激素治疗。禁忌证主要包括:(1)骨骺闭合;(2)已知对药物或相关成分过敏;(3)重度继发性甲状旁腺功能亢进症[甲状旁腺激素(parathyroid hormone,PTH)>500 ng/L];(4)增生性或重度非增生性糖尿病视网膜病变;(5)肾脏移植术后第1年;(6)急性危重症患儿;(7)活动性恶性肿瘤患儿。
关于儿童长激素使用剂量尚无统一标准,针对不同剂量生长激素的多项RCT研究显示,每周给予生长激素 28 U/m2(相当于每天0.046 mg/kg),患儿生长速率增加更为明显,尤其是使用生长激素1年后,生长速率显著优于低剂量组(生长激素每周14 U/m2,相当于每天0.023 mg/kg)。本指南主要根据“矮身材儿童诊治指南”和2019年欧洲肾脏病学会制定的儿童CKD生长激素使用指南中的生长激素剂量使用推荐,剂量范围为0.1~0.2 U/(kg·d)(每周0.23~0.46 mg/kg),并根据体重、治疗反应等定期调整剂量。根据剂型可将生长激素分为短效和长效,短效生长激素每天给药,为了模拟内源性生长激素分泌的生理昼夜节律,建议晚上睡前30 min皮下注射,注射侧需每天更换。长效生长激素每周只需注射1次,注射频率短,更方便住校、注射不方便及小年龄患儿使用。常用注射部位为大腿中部外侧面,也可以选择上臂或脐周等处。
推荐意见11:建议每3~6个月监测生长激素治疗情况,包括生长水平(身高或身长、体重、生长速率、青春期性发育、骨骼成熟情况)、肾功能、甲状旁腺激素水平、钙磷代谢情况、血糖、血红蛋白、血气分析、血胰岛素样生长因子1及不良反应等(2D)。
应用生长激素的患儿需定期监测治疗的有效性和安全性,根据生长水平、生化指标等,及时调整治疗方案。在监测疗效的同时,需监测不良反应。多项队列研究显示,生长激素即使治疗长达10年,不会增加CKD生长障碍患儿的eGFR下降速度。儿童肾脏移植受者接受生长激素治疗后,不增加移植后排斥和恶性肿瘤风险。尚无证据证明生长激素治疗与青春期发育提前或加速骨成熟相关,但仍需要对10岁以上患儿每年进行青春期评估,排除骨龄加速成熟,骨成熟加速的患儿应考虑停用生长激素。尽管现有证据显示生长激素并没有增加CKD患儿的不良事件发生,但临床试验仍随访观察时间相对短,有待临床进一步观察。
美国通过对国家合作生长研究项目数据库分析发现,1985年至2010年6月纳入使用生长激素的65 204例患儿中,71例患儿出现了颅内高压,其中2 144例患儿因慢性肾功能不全使用生长激素,10例患儿出现了颅内压增高,虽发生率不高,但为了尽可能降低风险,建议在开始生长激素治疗前进行眼底检查。如果生长激素治疗期间出现持续性头痛或呕吐,应立即行眼底检查等。
生长激素治疗可能会加重糖代谢异常,建议在治疗前和治疗中定期监测葡萄糖代谢水平。生长激素使用后快速生长可能会导致股骨头滑脱,如果出现症状,建议进行X线片检查,如果确诊为股骨头滑脱,需停止生长激素治疗。当出现以下事件时建议停止生长激素治疗,(1)骨骺闭合(已经没有生长潜力);(2)肾脏移植时;(3)合并持续性继发性甲状旁腺功能亢进(PTH>500 ng/L),当PTH水平恢复到目标范围,可重新开始使用;(4)发生颅内高压;(5)股骨头骨骺滑脱患儿;(6)除外其他影响生长发育的因素后,生长激素使用6个月无反应;(7)骨成熟加速患儿;(8)eGFR出现不明原因下降;(9)严重疾病或创伤;(10)治疗后患儿达到遗传身高。
推荐意见12:对于正在使用糖皮质激素治疗的合并生长发育障碍的CKD患儿,生长激素使用需谨慎,不建议高剂量糖皮质激素治疗时使用生长激素(2D)。
部分CKD患儿使用糖皮质激素,也会引起生长障碍,同时会影响生长激素治疗反应。尚缺乏关于糖皮质激素剂量对生长激素影响的RCT研究,但1项小样本回顾性分析显示,糖皮质激素剂量高于0.35 mg/(kg·d)时,外源性生长激素的促生长作用显著减弱。此外,2020年意大利儿科内分泌学会和肾脏病学会进行了生长激素使用相关问题的调查研究,结果显示68%的专家不推荐生长激素应用于仍使用高剂量糖皮质激素治疗的合并生长发育障碍的CKD患儿。建议在使用糖皮质激素时,尽可能减至小剂量后再考虑使用生长激素。
儿童生长发育受遗传、营养、消化吸收、内环境等多种因素综合影响,CKD导致的生长障碍会对患儿的生理、心理造成非常不利的影响。CKD患儿生长障碍的管理需要儿科及肾科专家、药剂师、护士、家庭与社会等多方面的共同支持。为了预防CKD患儿生长障碍的发生,应定期监测患儿生长状况。一旦出现生长平缓甚至下降趋势,应尽早探寻原因并予以纠正。当出现生长障碍时,在改善营养状况、纠正贫血、纠正继发性甲状旁腺功能亢进、纠正代谢性酸中毒、提高透析充分性等基础上,仍存有生长障碍,可考虑加用外源性生长激素,促进生长,改善CKD患儿的生存质量和改善预后。本指南制定中也存有不足之处,证据来源多基于国外指南和国外临床研究,缺乏多中心RCT,缺乏本土数据,有待在指南指导下开展我国CKD患儿合并生长发育障碍的临床研究,如我国CKD患儿的蛋白质能量摄入与生长的关系、激素剂量及累积剂量对生长的影响,不同生长激素剂量对生长的影响及评估指标、拟肾移植的患儿生长激素最佳使用时机等,从而进一步更新完善、建立适合我国CKD患儿的临床循证指南。
参与本指南审核的专家指导组名单(按单位和姓氏拼音排序):北京大学第一医院(王芳);成都市妇女儿童中心医院(程昕然);重庆医科大学附属儿童医院(李秋、李廷玉、王墨);复旦大学附属儿科医院(李智平、沈茜、徐虹、严卫丽);华中科技大学同济医学院附属同济医院(罗小平、周建华);江西省儿童医院(杨玉);南京医科大学附属儿童医院(黄松明、张爱华、朱春华);上海交通大学医学院附属上海儿童医学中心(张顺国);上海交通大学医学院附属新华医院(沈理笑);上海市儿童医院(黄文彦);首都儿科研究所附属儿童医院(陈晓波、王琳);首都医科大学附属北京儿童医院(沈颖、王晓玲);浙江大学医学院附属儿童医院(江米足、毛建华);中山大学附属第一医院(蒋小云)