编辑:云影
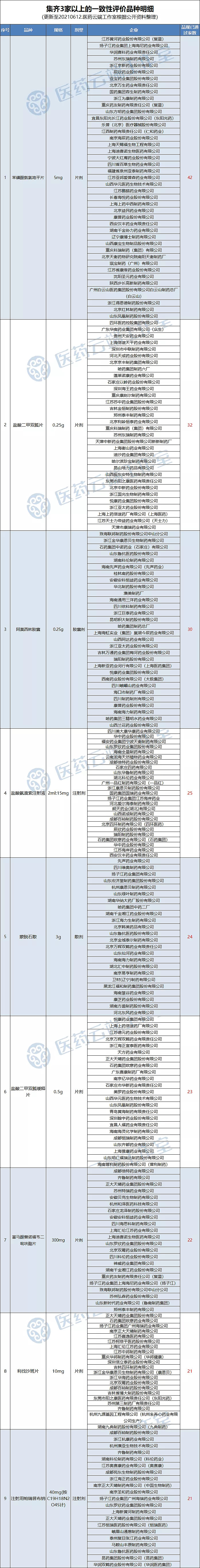
根据医药云端工作室不完全统计,目前已有2534个品规通过一致性评价,292个品规集齐三家以上(含三家)过评
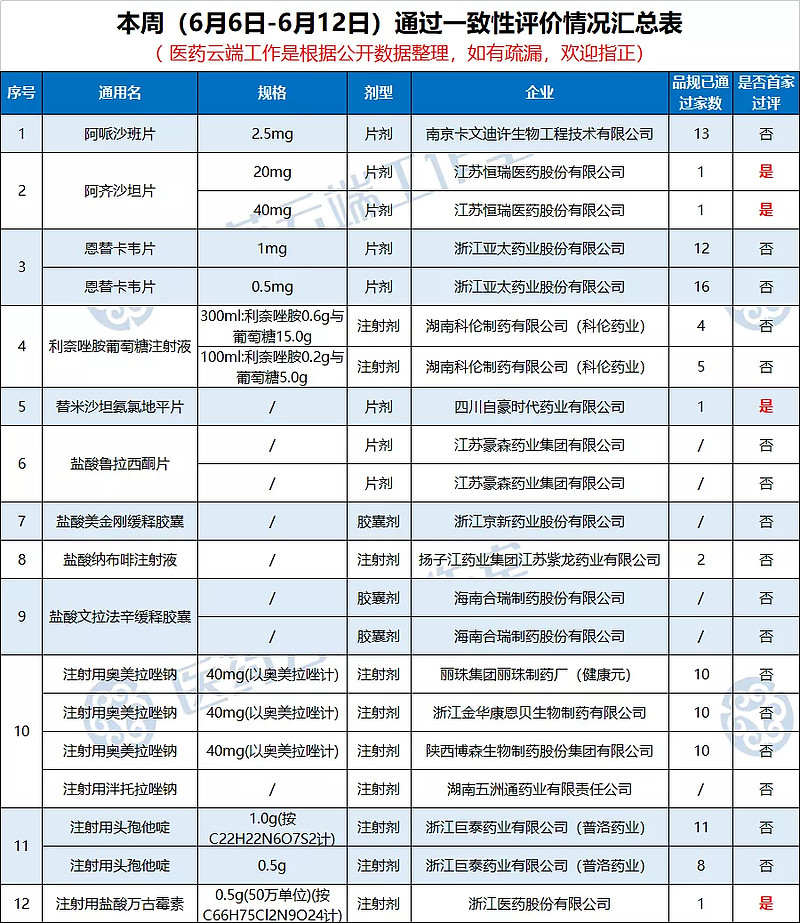
根据医药云端工作室统计,本周(2021年6月6日-2021年6月12日),新增12个品种(视同)通过一致性评价,其中3个为全国首家过评,具体如下:
浙江医药:注射用盐酸万古霉素全国首家过评
注射用盐酸万古霉素属于糖肽类抗菌药,用于治疗对万古霉素敏感的耐甲氧西林(β-内酰胺耐药)的葡萄球菌引起的严重或致命感染,以及由葡萄球菌、草绿色链球菌、牛链球菌或类白喉杆菌引起的心内膜炎。
盐酸万古霉素由礼来从土壤中分离出来并完成研制,并于1958年获得FDA批准上市,商品名Vancocin。
米内网数据显示,2018年中国公立医疗机构终端注射用盐酸万古霉素销售额为17.02亿元,同比增长10.64%,其中原研厂家礼来占据70%以上的市场份额。
恒瑞医药:阿齐沙坦片获批视同过评,为全国首家
阿齐沙坦是一种血管紧张素 II 受体拮抗剂(ARB)。阿齐沙坦片由 Takeda Pharmaceutical(以下简称“武田制药”)开发,商品名为 AZILVA,最早于 2012 年 1 月在日本批准上市,适用于治疗高血压症。
目前国内已有多家企业申报生产, 除恒瑞外,暂未见其他企业获批信息。经查询 EvaluatePharma 数据库,2019 年武田制药阿齐沙坦片全球销售额约为 7.06 亿美元,暂未查到 2020 年度销售数据。
据恒瑞医药公告显示,截至目前,阿齐沙坦片相关项目累计已投入研发费用约为 2465 万元。
四川自豪时代药业:替米沙坦氨氯地平片获批视同过评,为全国首家
替米沙坦氨氯地平是由替米沙坦(特异性血管紧张素Ⅱ受体拮抗剂)和苯磺酸氨氯地平(钙离子拮抗剂)组成的复方制剂,用于治疗原发性高血压。
该药品是由德国勃林格殷格翰制药公司研制的,于2009年10月16日获得美国FDA批准上市,商品名为TWYNSTA®,此外该复方制剂于2010年7月10日在欧洲批准上市。2017年9月20日替米沙坦氨氯地平片获中国CFDA批准上市(商品名:双加,规格80mg/5mg)。
替米沙坦氨氯地平片已被列入《中国高血压防治指南(2018年修订版)》,具有良好的市场前景。
四川自豪时代药业于2018年10月以仿制3类提交替米沙坦氨氯地平片上市申请,2021年5月进入行政审批阶段,此次获批成功拿下首仿。
全国最新过评数据通报:
根据医药云端工作室不完全统计,目前已有2534个品规通过一致性评价,292个品规集齐三家以上(含三家)过评。