全文复制坚守开拓兄“开拓药业投资策略之我见 ——写在新冠非住院Ⅲ期临床试验中期分析前夕”,担心他删除了特别复制下来,向他的严谨研究精神致敬,作为医药研究范文学习
前言
对开拓药业的投资极具吸引力也极具挑战性,特别是在普克鲁胺非住院患者MRCT中期分析前夕,很想给自己写点什么,留作纪念。球友不必求同,也不必因异而争,拿来主义吧。
普克鲁胺是中国药科大学科学研究院药物代谢动力学重点实验室王广基院士、孙建国副教授团队与苏州开拓药业合作研发的第二代雄激素受体(AR)拮抗剂,针对前列腺癌和乳腺癌,尤其是去势抵抗性前列腺癌(“mCRPC”)和AR表达阳性的晚期乳腺癌,分别于2015和2016年获得中国和美国的临床批件,目前仍在临床研究阶段。
普克鲁胺是基于美国最新上市的抗前列腺癌新药恩杂鲁胺(Enzalutamide,MDV3100)的核心结构、采用基于靶蛋白晶体结构的计算机辅助设计并反复优化得到的新型化合物。该药的化学结构与恩杂鲁胺(MDV3100)相比较有了多处改变,从而改善了分子溶解度和动力学性质。
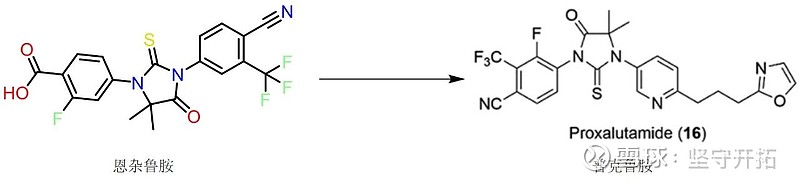
图1:普克鲁胺和恩杂鲁胺分子结构
第一章 普克鲁胺治疗新冠可信吗?
背景:2021年6月,开拓药业的普克鲁胺在巴西由研究者发起的治疗新冠住院患者的临床试验(IIT)结果显示:住院患者的死亡率下降了78%(普克鲁胺组11%/安慰剂组49.4%)。这一结果,在引发巨大轰动的同时,也带来巨大的争议。美国Science杂志、巴西CNS以及其他各方从不同的角度对结果提出了质疑。面对新冠治疗药物巨大的市场利益诱惑,只有对这些质疑分析并做出自己的判断后,我才敢做出投资决策。因此,我把不信与信分为反方与正方,试图通过梳理给自己的判断提供依据。
一、反方:不信
1、2021年7月7日,美国Science杂志发表文章《Too good to be ture:“Doubts swirl around trial that saw 77% reduction in COVID-19 mortality”》,(原文:网页链接)从多个角度提出质疑。我把质疑一一列示如下,并试图对质疑寻找答案。
(1)试验PI曾经推过多个没有被证明的新冠药物
质疑:

图2:科学杂志相关节选
Flavio Cadegiani作为Applied Biology的一名内分泌学家,他曾经推荐过许多没有被证明的新冠药物,包括ivermectin、azithromycin以及抗蠕虫的复合物,使得他的言论看起来很不可靠。
解读:
Flavio Cadegiani博士及其团队确实一直以来都在致力于新冠药物的发现和临床试验相关工作。比如今年7月,他的团队就发表了使用Azithromycin加Nitazoxanide, Ivermectin或者Hydroxychloroquine来治疗非住院新冠患者的试验结果和论文。但是用吹捧来形容他对潜在治疗药物的态度就有点言过其实。在公开资料里,我没有发现任何直接引用的他的原话可以表明他在吹捧。如果说有人在吹捧,那也许是Flavio Cadegiani博士在接受科学杂志采访时提到的一个人————巴西总统博索纳罗,一个一直以来极力反对疫苗并推荐使用药物来抗疫的争议人物。如果巴西的国家领导人鼓励这样的抗疫政策,那么上传下达到基层研究人员,促使他们朝着药物发现和研究的方向努力就不难理解了。
(2)为什么其他AR拮抗剂没有效果或者效果不明显?
质疑:
除了巴西的试验外,迄今为止对COVID-19患者的抗雄激素测试并不令人鼓舞。克利夫兰诊所(Cleveland Clinic)的前列腺癌研究人员尼玛·沙里夫(Nima Sharifi)在2月份发表在《泌尿学杂志》(Journal of Urology)上的一项研究发现,在1779名前列腺癌患者中,雄激素剥夺疗法(ADT)对他们感染SARS-CoV-2的风险没有影响。范德比尔特大学(Vanderbilt University)的研究人员领导的另一项研究发现,对近600名前列腺癌患者进行ADT治疗,对死于COVID-19的人数没有影响。这项研究在美国临床肿瘤学会(American Society of Clinical Oncology)最近的一次会议上提出。

图3:科学杂志相关节选
解读:
普克鲁胺具有双重作用原理,同时抑制AR信号功能和降低AR蛋白的表达,通过调节AR信号通路同时调节人体ACE2和TMPRSS2表达。而其它AR拮抗剂不具备这样多重机制。公开资料显示,临床前研究普克鲁胺可以下调人体肺癌细胞、前列腺癌细胞和鼠肺上皮细胞中的ACE2和TMPRSS2表达。

图4:普克鲁胺临床前数据

图5:普克鲁胺作用机制
中国科学院分子细胞科学卓越创新中心高栋研究组和复旦大学陆教授、孙艺华教授、谢幼华教授自发研究了恩杂鲁胺是否能够用来治疗新冠。根据其2月28日发表于Nature Communications研究论文“Distinct mechanisms for TMPRSS2 expression explain organ-specific inhibition of SARS-CoV-2 infection by enzalutamide”,恩杂鲁胺并不具备用于新冠治疗潜力,是因为虽然在前列腺细胞中,恩杂鲁胺能够通过下调TMPRSS2表达水平进而抑制新冠病毒的入侵,但是在肺的细胞中恩杂鲁胺并不能调控TMPRSS2的表达,不具有抑制新冠病毒的疗效。
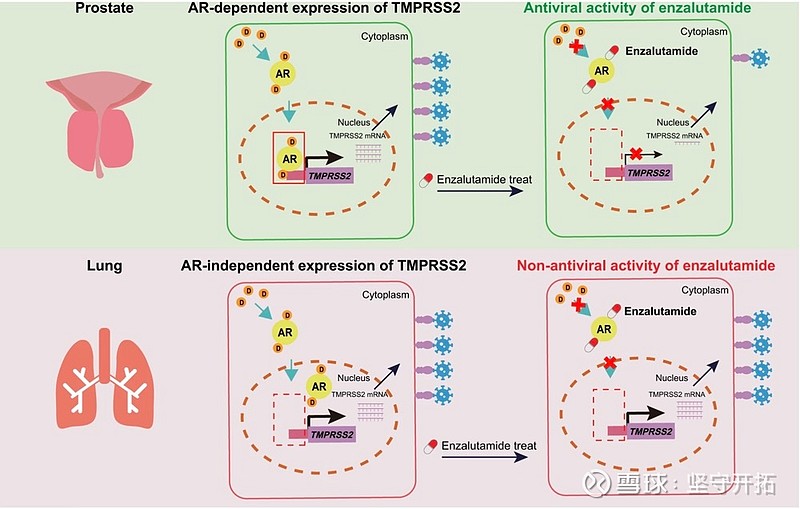
图6:恩杂鲁胺在不同细胞系中调节机制
我个人认为,虽然都是AR拮抗剂,但毕竟不是完全相同的药物,药物分子结构存在一定差异,在下面瑞士大学的有关研究中又似乎能找到其他AR拮抗剂有效的证据,最终这些疑问需要药物学家在未来的研究中一一找到答案。但以这一思路否定普克鲁胺肯定是缺乏依据的。
来源:公司官网、“Distinct mechanisms for TMPRSS2 expression explain organ-specific inhibition of SARS-CoV-2 infection by enzalutamide”
(3)对照组死亡人数过多
质疑:
文章中多位研究者表示对试验中出现的死亡人数感到震惊。在对照组死亡率达49.4%,使得药效看起来更好,但这一住院死亡率远远高于美国不到10%的住院死亡率。
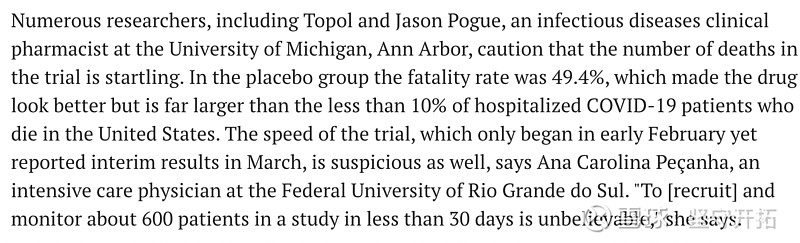
图7:科学杂志相关节选
解读:
普克鲁胺试验医院位于马瑙斯城市,巴西的西北部的城市,当时是巴西疫情最为严重的城市之一。根据2021年1月15日发表在柳叶刀上的论文“Characterisation of the first 250 000 hospital admissions for COVID-19 in Brazil: a retrospective analysis of nationwide data”,文章回顾性分析了2020年2月16日至2020年8月15日250000巴西住院患者的特征,在此期间巴西整体住院死亡率高达38% (87515/232036名患者);ICU死亡率为59%,使用呼吸机患者死亡率80%,其中北部地区住院死亡率更是高达50%。
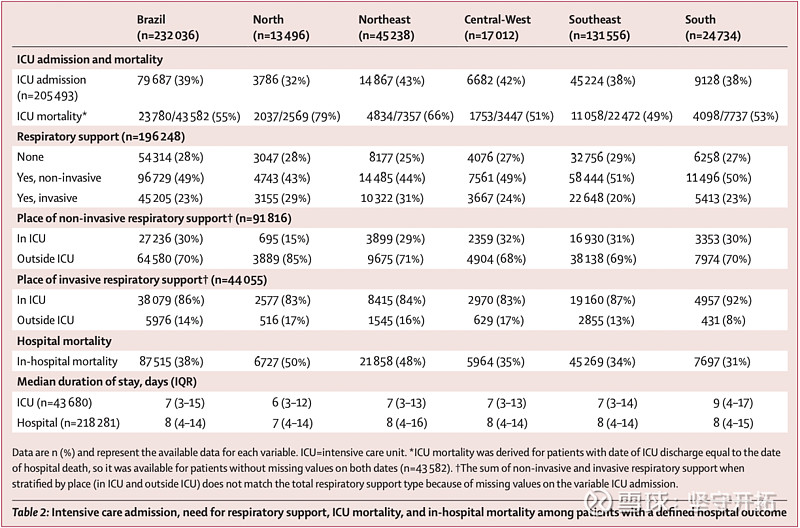
图8:巴西不同地区的住院死亡率
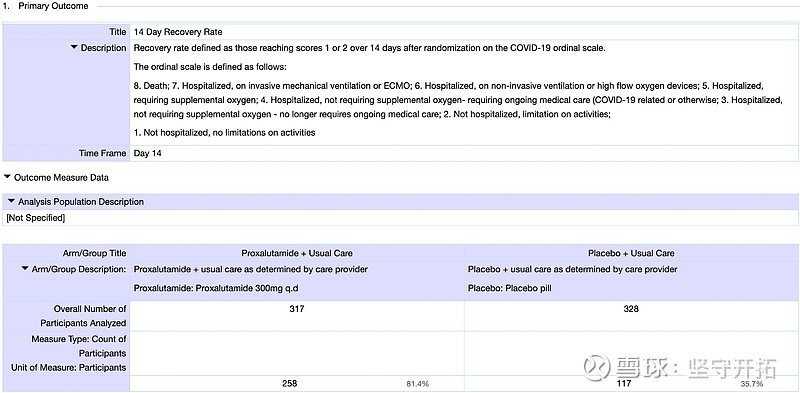
图9:ClinicalTrial网站普克鲁胺重症临床结果
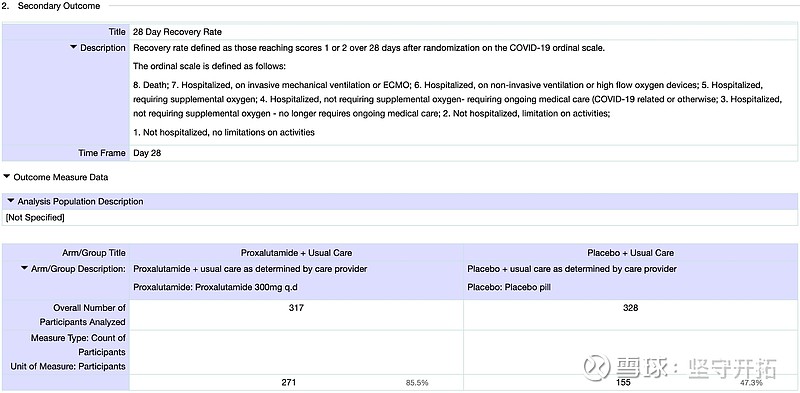
图10:ClinicalTrial网站普克鲁胺重症临床结果
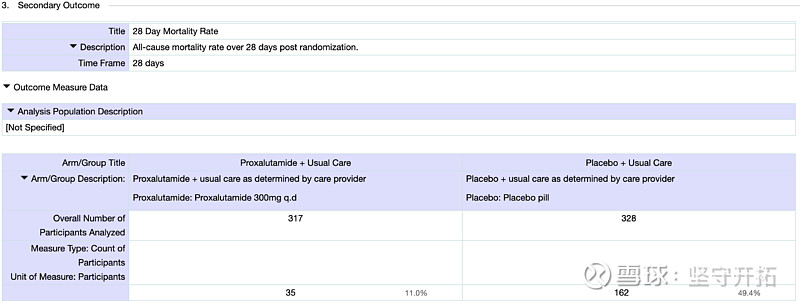
图11:ClinicalTrial网站普克鲁胺重症临床结果
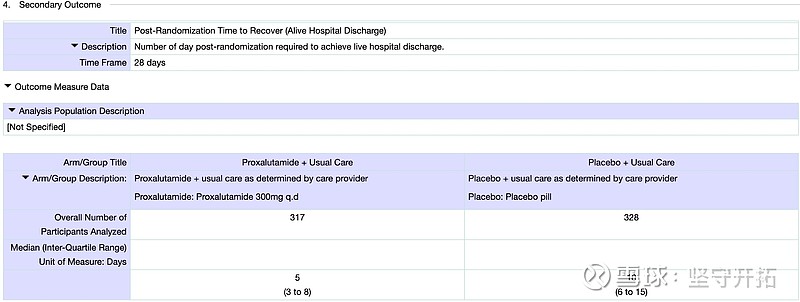
图12:ClinicalTrial网站普克鲁胺重症临床结果
根据ClinicalTrial结果显示普克鲁胺组28天死亡率11%,而对照组28天死亡率则是49.4%,与论文中的北部地区死亡率50%较为近似,由此可以判断死亡率并非过高。
另一方面,病毒的变异和疫情政治化也影响着巴西疫情。2020年12月以来,Gamma变异株成为马瑙斯主要的流行株,截至2021年1月&2月Gamma变异感染占比超过92%,普克鲁胺临床试验的入组时间为2021年1月,恰好是病毒蔓延的期间。由于疫情政治化,巴西马瑙斯地区疫苗接种率极低,导致感染者人数激增,能进入医院接受救治病人情况都较为严重,导致普克鲁胺入组患者普遍为5分至6分的重症患者[1],其中5-6分的患者占比超过95%,6分的患者超过65%,加之当时巴西氧气设备匮乏,来不及被救治的病人很快进入紧急状态。
WHO等级量表评分:1分-未住院,且可继续从事日常活动;2分-未住院,但无法继续从事日常活动;3分-住院治疗,不需要吸氧,不需要其他相关医疗护理;4分-住院治疗,不需要吸氧,需要其他相关医疗护理;5分-住院治疗,需要吸氧;6分-住院治疗,需要鼻高流量氧疗、无创机械;7分-住院治疗,需要ECMO;8分-死亡。 ↑
综上,考虑到巴西当时疫情情况,普克鲁胺入组病人基线情况及论文中阐述的真实世界数据,我认为普克鲁胺对照组死亡率接近真实世界数据,且合情合理。

图13:巴西日均死亡人数创新高,因新冠死亡人数超过25.1万人

图14:亚马逊地区氧气匮乏

图15:“我祖母因为氧气供应短缺而去世”,家属围在医院门口等待消息。
来源:柳叶刀论文“Characterisation of the first 250 000 hospital admissions for COVID-19 in Brazil: a retrospective analysis of nationwide data”、ClinicalTrial网站、The Guardian新闻、YouTube网站视频
(4)入组过快
质疑:
文章中一位南里奥格兰德联邦大学的ICU医生曾指出:“试验开始于二月初,然而到了三月就公告了中期结果,这样的试验速度让人感到怀疑,从入组并观察600名患者仅用了不到30天,这让人难以置信。”

图16:科学杂志相关节选
解读:
巴西当时入组速度的确很快,一方面是疫情严重程度会很大程度影响入组速度,开拓药业的董事长童有之博士(以下简称“童博”)在采访中也曾经提到“在巴西进行的研究,可能仅需几个月时间就能完成。在巴西开展的研究中,590名重症病人仅21天就在疫情最严重的亚马逊州玛瑙市的12家医院完成入组,而之前近300名轻中症病人入组的时间也只有2个月。”
另一方面,巴西当时医疗资源较为紧张,入组筛查可能相对简单,试验消息保密性较差。Science文中PI对于试验进度解释中讲到“随着人们听闻普克鲁胺试验组的参与者几天内就恢复出院了,纷纷踊跃报名参加试验”。
虽然,巴西当时的情景我们不可能身临其境地去感知,但武汉当初的情形我们是略知一二的,我咨询过有丰富临床经验的专家,即使保密手段再好,如果一款药的疗效很突出,参与实验的医院的医护人员是有方法感知到的,进而影响重症入组也是可以理解的。

图17:科学杂志相关节选
(5)国际权威期刊拒绝发表巴西试验论文。
质疑:

图18:科学杂志相关节选
解读:
如上图,其实《科学》杂志已经自问自答了,杂志拒绝发表的原因并不是因为造假,而是结果太好。比如《科学》杂志提到《The New England Journal of Medicine》拒绝的原因是该试验的结果太好,如果发表,杂志需要分析所有的原始数据 ,而NEJM现在没有足够的能力审阅这么多的数据。
2、2021年10月15日,巴西CNS(国家卫生委员会)阐述了普克鲁胺试验中的不符合规则的情况。质疑主要集中在过程而不是结果。
(1)重症研究,只经过了国家级伦理委员会的批准,没有获得全部试验医院的批准。
质疑:
巴西联邦政府国家卫生委员会(CNS)指出普克鲁胺重症研究虽然于2021年1月27日获得国家伦理委员会(Conep)批准在巴西利亚一家机构开展研究,研究者却声称批准在全国进行试验研究。经过证实国家伦理委员会曾明确进行试验的地点,并且从未批准将试验范围扩大至全国。更不用说,国家伦理委员会并没有这样的权利,每个中心都有一个伦理委员会审批相关联的机构是否进行试验。

图19:巴西联邦政府国家委员会公开信内容
解读:
试验进行过程中,医生如果在未经过各个中心批复情况下,擅自扩大试验范围,确实会违反相关试验管理条法。但由上述论文中,已知巴西当时疫情十分严重,医院挤兑和供氧设备严重不足,许多患者来不及被救治便匆匆离去,医生很有可能不能顾及规章流程,按照规定申请批准才开始用药救人。如果回顾2020年初武汉疫情爆发时,我国医院挤兑情况,我国医生也使用了一切能用的药物和方法来挽救患者生命。
换个角度,没有一个医院一个医院的经过伦理批准,确实能大幅提升试验的进度,这也不排除IIT研究者为了尽快获得试验结果而有意为之,我们也不得而知。但从投资的角度,这个质疑不会影响普克鲁胺的有效性。
(2)对照组数据无法溯源
质疑:

图20:巴西联邦政府国家委员会公开信内容
联邦政府国家委员会公开信曾写道“尽管伦理委员会要求一个澄清,研究者们始终没有提供可以追溯用药情况(包括药物流通和分发),无法验证对照组使用的究竟是什么样的药物,因此不排除对照组在不知情的情况下服用安慰剂以外的可能有毒的药物,这样一来对照组中高频出现肾和肝功能衰竭问题也就解释的通了”
解读:
首先对照组的死亡率并没有畸高,柳叶刀论文中也提到了巴西当时较高的死亡率。关于肾和肝功能衰竭,研究者在预印版论文里阐述:“不良反应在普克鲁胺组仅为腹泻,而对照组则出现严重肝和肾功能衰竭,我们理解这一现象是随着新冠病情发展出现的自然过程”。 根据BBC新闻,其它研究也有表明,新冠还会严重破坏肾脏、肝脏、心脏以及身体的几乎所有器官系统。因此,这一现象是有可能由于新冠病毒发展至后期引起的,但在无法确认研究者们是否有提供进一步数据及确切判决出来之前,我无法排除是否有人为干预导致这一结果。
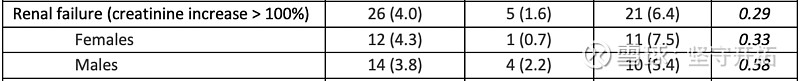
图21:预印版论文

图22:预印版论文

图23:BBC新闻
来源:网页链接、“Efficacy of Proxalutamide in Hospitalized COVID-19 Patients: A Randomized, Double-Blind, Placebo-Controlled, ParallelDesign Clinical Trial”、网页链接
(3)独立数据委员会的独立性
质疑:
联邦政府国家卫生委员会(CNS)曾质疑试验独立性,指出试验的独立数据监察委员会的负责人由实验赞助方来担任不符合国际惯例。

图24:巴西联邦政府国家委员会公开信内容
解读:
如果这一指责为真实的话,的确会导致数据独立性和可信度受到怀疑。对此问题,由于我无法获得更多的资料和数据,因此难以进行更深入的研究分析并得出进一步的结论。
3、其他质疑
(1)巴拉圭EUA真实性?
质疑:
法新社曾报道,巴拉圭卫生部否认普克鲁胺获批进行临床试验和EUA。根据法新社报道,巴拉圭卫生部表示“我们没有任何证据去证明他们的结果,在没有任何根据情况,我们不会盲目批复。”

图25:法新社新闻
解读:
首先,该报道并未指出这段回复出自于卫生部的哪位人物,其次在Youtube有相关采访视频,巴拉圭卫生部副部长表示:“根据Barrio Obreiro医院,实验非常好,结果是非常振奋人心的。非常感谢Samel公司。现在,我们欢迎能抗击新冠病毒的一切药物。我们离抗疫成功还很远。同时,我认为我们随时可能面临着新的新增潮,因为现在有了这些变种毒株。我们拖得时间越长,变种毒株就越猖獗。我们很清楚,我们目前还处在疫苗免疫的初期阶段。所以,不幸的是,新冠还会持续在我们身边一段时间。所以,谢谢你们的努力,我们希望能将实验扩张至其它医院并获得相同的结果。“为了进一步确保采访的可信度,我比对了采访中巴拉圭卫生部副部长的长相,发现与MSPBS其它报道一致;并且比对人物姓名,并未发现不一致地方。因此进一步验证了巴拉圭用药的真实性。
巴拉圭用药相关链接:网页链接

图26:视频中巴拉圭副部长长相和名字

图27:其它采访中巴拉圭卫生部副部长

图28:巴拉圭MSPBS官网展示卫生部副部长名字
(2)普克鲁胺的作用机制与其他国际制药巨头的药物研发作用机制完全不同。
解读:
普克鲁胺是由观察到男性和女性新冠患者重症比例不同的现象出发,想到是否能用AR拮抗剂治疗新冠,跟传统从机制出发研发抗病毒药物不同。辉瑞及默克的药物都是从新冠病毒感染人体机理出发,在不同环节寻找靶点来开发治疗药物。
(3)原本治疗前列腺癌的药物,怎么突然能治疗新冠了?
解读:
首先,“老药新用”的研发策略在新冠疫情中并非第一次出现,开发一种全新的药物到最终获批上市一般至少需要10年的时间,而“老药新用”显然是一种更为经济和可靠的策略。事实上,药品的新机制、新适应症的发现很常见,例如:现在属于美国COVID-19住院标准疗法的瑞德西韦原先用于治疗埃博拉;获批用于COVID-19住院治疗的巴瑞替尼原先用于治疗患有中度至重度活动性类风湿性关节炎 (RA) 的成人患者;获批用于COVID-19住院治疗的罗氏托珠单抗原先被用于类风湿性关节炎治疗。开拓曾探索AR拮抗剂的多种疗法,包括肿瘤治疗、脱发/痤疮等,因此治疗新冠是公司发现普克鲁胺作为一款雄激素受体(AR)拮抗剂用于治疗前列腺癌后的又一个治疗机制。
其次,开拓发现普克鲁胺具有潜在治疗新冠的作用是一次有据可寻的科学探索,而并非偶然行为。(具体论述参见“正方—信”部分)
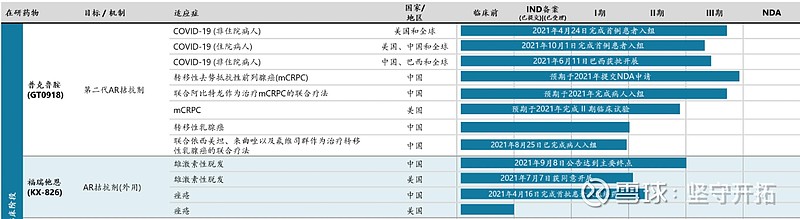
图29:普克鲁胺在研适应症
二、正方:可信
1、普克鲁胺治疗新冠的历史演进过程清晰
(1)SSRN关于两个关键蛋白和新冠关联的论文
2020年4月,SSRN期刊上的一篇论文,揭示了AR拮抗剂抑制新冠病毒入侵宿主的两个关键蛋白ACE2、TMPRSS2的通路可能对男性新冠患者有益。这一成果来自开拓药业和苏州大学的早期探索。
在这项临床前研究合作里,开拓药业发现普克鲁胺作为AR(雄激素受体)拮抗剂,能降低ACE2和TMPRSS2在正常肺细胞及来自前列腺与肺癌的癌细胞的表达。但因为国内的疫情得到控制,缺乏新冠患者,更多的探索一度被搁置。
“我们注意到一个很奇怪的现象,按理说,在疾病大量感染和传播阶段,性别造成的差异应该是非常小的,但新冠患者中,男性的病情进展、住院与死亡情况非常严重,女性则相对好一些。”童博回忆,“于是,2月份的时候,我们收集了1339例新冠患者的临床数据,对背后的机制进行分析。”
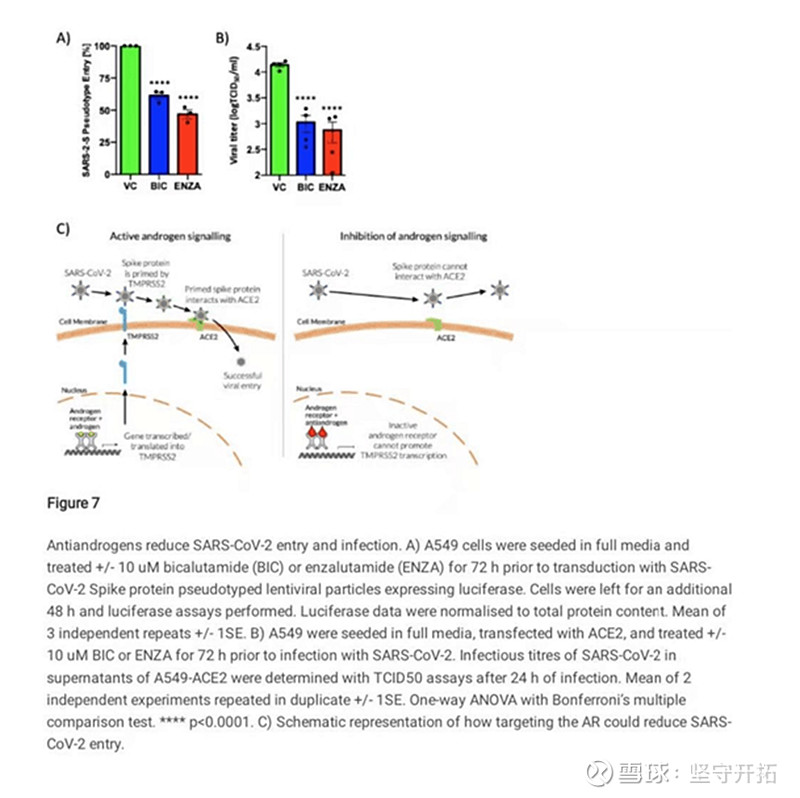
图30:论文中的机理解释
来源:网页链接
(2)瑞士提契诺大学关于雄激素和新冠感染关联的论文
2020年5月6日,来自瑞士提契诺大学Andrea Alimonti 教授领导的研究团队在国际顶尖肿瘤学临床期刊《肿瘤学年鉴(Annals of Oncology)》上发表论文,首次揭示了雄激素剥夺疗法和新冠肺炎感染之间的关系,阐述了雄激素剥夺疗法有可能会降低男性感染新冠肺炎的风险。雄激素剥夺疗法是前列腺癌患者用的一种治疗方案。有研究表明,一种名为TMPRSS2的蛋白可以帮助新冠肺炎病毒感染健康的人类细胞。TMPRSS2是II型跨膜丝氨酸蛋白酶蛋白家族的成员之一,这一蛋白质参与人体许多过程,包括癌症和病毒感染。前列腺癌患者体内的TMPRSS2 水平很高,而且作用主要受雄激素受体调节,而雄激素受体又是一系列雄激素剥夺疗法的靶标。雄激素受体还调节费前列腺癌组织包括肺部中的TMPRSS2水平。因此,Alimonti 教授怀疑雄激素或许与新冠肺炎的感染有着某些关系。
于是,他们收集了大量新冠肺炎感染者的数据对意大利威尼托地区所有的癌症患者资料进行分析,然后发现,即使总体而言癌症患者感染新冠肺炎的风险较高,但那些接受过雄激素剥夺疗法的前列腺癌患者似乎受到什么东西的保护,他们感染新冠肺炎甚至死于新冠肺炎的风险都显著降低。他们发现,5273名接受雄激素剥夺治疗的前列腺癌患者新冠肺炎感染率只有76/100000,没有接受雄激素剥夺治疗的37161名前列腺癌患者新冠肺炎感染率高达 318/100000,而79661名其他类型癌症患者新冠肺炎的感染率也高达392/100000。更重要的是,那些接受雄激素剥夺疗法的前列腺癌患者中,并没有人死于新冠肺炎,而没有接受雄激素剥夺疗法的前列腺癌患者中已有 18人死于新冠肺炎,其他类型癌症患者中已有57人死于新冠肺炎。
这一研究解释了为什么受新冠肺炎感染的男性往往比女性更容易出现严重的并发症甚至死亡,也预示着,雄激素剥夺疗法或许可以用于新冠肺炎的预防以及治疗。
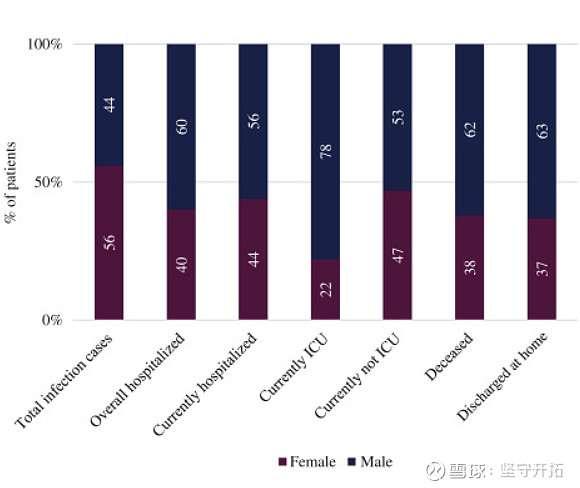
图31:感染新冠风险的男女差异
来源:网页链接(20)39797-0/fulltext#relatedArticles
(3)美国布朗大学教授关于雄脱和新冠关联的论文
2020年6月,美国布朗大学Wambier教授、Applied Biology公司的总裁兼首席医学官Andy Goren教授,发表了有关雄激素性脱发与新冠发病机理具有潜在关联性的研究结果,进一步为AR拮抗剂作为早期药物干预新冠提供科学依据。
童博看到这一新闻后,与Andy Goren教授取得联系,并最终促成开拓药业与Applied Biology公司的合作。根据协议,双方将共同进行普克鲁胺治疗新冠的研究。2020年8月20日,第一例患者成功入组,而这也是首次将抗雄激素药物用于治疗新冠的尝试。Applied Biology公司还在巴西发起一项抗雄激素治疗新冠患者的临床研究,计划招募254名年龄在50岁以上的男性新冠检测阳性入组者,划为两组接受度他雄胺、安慰剂分别联合标准治疗,主要终点是30天内入组者入院的比例。
来源:网页链接
(4)PNAS美国国家科学院院刊
2020年11月,美国密歇根大学Chinnaiyan教授团队在PNAS上发表论文,进一步详细地论述了AR抑制剂治疗新冠轻症的机理。雄激素调节肺部上皮细胞中的ACE2、TMPRSS2和雄激素受体(AR)的表达。这项研究的结果表明,靶向宿主进入因子TMPRSS2和ACE2的转录调控是预防SARS-CoV-2感染的可行治疗策略。特别是,雄激素受体(AR)或溴结构域和末端外结构域(BET)蛋白的抑制剂可有效抵抗SARS-CoV-2感染。
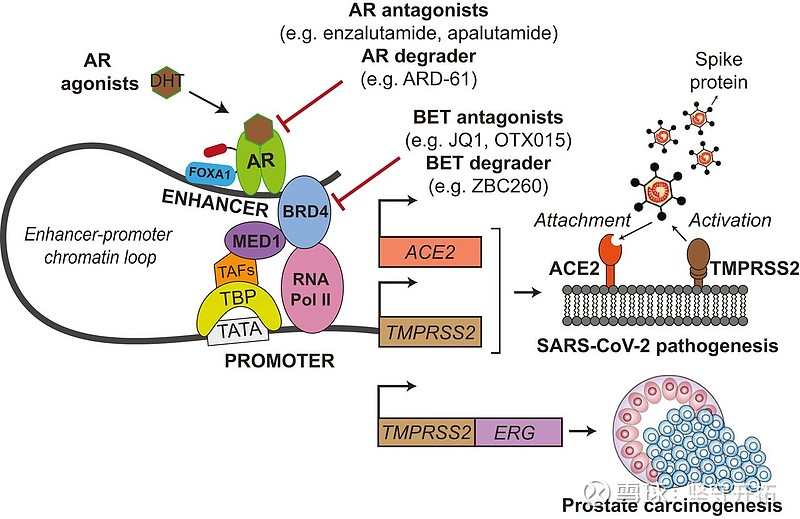
图32:AR抑制剂作用机制
来源:网页链接
(5)巴西两个IIT分别得到非住院和住院患者的临床数据
2020年11月,基于普克鲁胺治疗新冠男性入组者展示出的良好疗效,巴西政府卫生部门建议开拓药业继续与美国和巴西的临床研究者合作,由研究者发起普克鲁胺治疗新冠女性入组者的临床试验。
最终公布的有268名患者参与的非住院临床结果中,用药组和对照组分别有3人和35人住院,住院率分别为2.2%和26.1%,住院率降低了91.6%。
而在今年二月开展的由645名住院患者参与的另一项临床试验,主要终点14天康复率,用药组和对照组分别为81.4%和35.7%,次要终点28天死亡率,用药组和对照组分别为11%和49.4%,死亡率降低了77.8%。
(6)启动3个全球MRCT
基于普克鲁胺治疗新冠的机理研究、在中美两国进行治疗mCRPC用药的安全性数据、以及在巴西的两个IIT的临床结果,美国FDA分别于今年3月和5月同意开拓药业开展普克鲁胺治疗新冠非住院和住院患者的Ⅲ期临床。考虑到一些国家对住院标准设置的不同,公司又在中国、巴西等国家开设了第三个全球MRCT,用于普克鲁胺治疗男性非住院患者,将临床终点设置为28天需要氧气支持的患者比例。该MRCT于今年9月1日获得中国国家药监局批准开展。
来源:公司公告
(7)巴拉圭获批EUA,得到首个真实世界数据
开拓药业于7月16日公告,普克鲁胺在巴拉圭由国家卫生和社会福利部授予EUA,用于治疗新冠住院患者。这是普克鲁胺治疗新冠在全球获得的首个EUA。已经呈报的初步治疗结果,在25名患者中,经过14天的给药,22名患者病情得到缓解,1人死亡,远低于巴拉圭入院死亡平均水平。
来源:公司中期报告
2、世界各国药监机构批准临床,侧面验证巴西IIT数据的可信度
(1)美国FDA
FDA凭什么批准普克鲁胺不在美国做I期和II期临床试验,直接进行III期临床实验呢?理解药品临床试验的基本流程就会知道,I期试验解决的是药品的安全性问题,II期试验解决的是药品的安全性和初步的有效性,在美国这样一个命比什么都值钱的国家,在FDA这样一个全世界水平最高、标准最严格的药监部门,能够批准普克鲁胺直接III期临床实验,只能说FDA认同了开拓药业提供的资料,认同了普克鲁胺对于临床参与患者的安全性,并也看到了普克鲁胺治疗新冠的有效性希望!那开拓药业提供的资料来自哪里呢?巴西的IIT临床结果一定是其中最重要的一部分。这个问题就分析到这里,大家自己去品。
图33:FDA关于Ⅱ期临床的描述
顺便科普一下,FDA有一个IND审查团队,由不同科学领域的专家组成,负责对公司提交的资料进行审查,包括临床设计、临床数据、临床前数据、药代动力、药物化合物、其他数据等。在进入Ⅲ期临床试验前,FDA会和药企开会讨论,并敲定Ⅲ期临床的设置细节。

图34:IND审查团队的构成
FDA从最开始2021年3月5日的只批准了男性轻症临床试验,后来又陆陆续续批准了女性轻症、男女重症临床试验。特别是批准重症非同儿戏,重症患者离死亡近在咫尺,稍有不慎,耽误了治疗就会危及生命,FDA不会拿美国人的生命开玩笑。
来源:公司公告
(2)中国国家药监局、巴西ANVISA、印度CDSCO
除了美国的FDA,普克鲁胺在中国和巴西都获得治疗非住院以及住院新冠患者的Ⅲ期临床。和美国FDA一样,中国的药监局也以严谨和专业著称。而巴西的ANVISA,在国际上的地位也丝毫不逊色,和中国的NMPA同为ICH联盟的监管成员,在全球临床标准的制定中扮演重要角色。普克鲁胺治疗新冠的Ⅲ期临床是由FDA、中国药监局、ANVISA分别独立审批的。从这个角度考虑,如果巴西IIT的数据有重大问题,那么同时骗过三家顶级药审机构的概率会是多少呢?
中国的临床批复,是严格按照规定的流程办理。目前普克鲁胺是国内唯一一家被批准进入Ⅲ期临床的新冠小分子药,足以看出国家对于普克鲁胺战略地位的重视。
在巴西被ANVISA批准临床,意义同样重大,因为自始至终针对普克鲁胺的质疑都集中在巴西的重症IIT临床试验上。巴西总统多次提到普克鲁胺,也让该临床试验成为众矢之的(注:巴西总统博索纳罗一直以来都反对疫苗,自己也未接种新冠疫苗,他本人推崇的抗疫策略就是使用各种药物治疗,他也因此饱受多方批评)。ANVISA能在反对派媒体的密集炮火下,顶住压力批准普克鲁胺的临床试验,一定做了周密的审查和论证,在确定药物安全性没有问题的情况下,才给普克鲁胺开了绿灯。
在印度申请开展非住院临床的过程中,开拓药业也遇到了当地监管机构的为难。比如CDSCO在收到申请后,就提出了例如“为什么治疗前列腺癌的药物可以用来治疗新冠”这样一个对于专业药审机构来说显得比较业余的问题,但开拓药业仍旧按照CDSCO的要求对疑问做了一一解答并补交了相关材料,最后才获得批准。
除了以上国家外,开拓药业也没有停止在其它国家开展临床的努力。比如10月18日,印度尼西亚海关事务及投资部部长在一个新闻发布会上表示,除了默克的莫努匹韦,也会考虑罗氏以及开拓药业的新冠药。他的话在11月得到了进一步验证。11月8日下午,印度尼西亚驻华大使周浩黎、印度尼西亚驻沪总领事戴宁、中国印尼商会主席Liky Sutikno一行就来到开拓药业进行实地调研。
来源:公司公告、公司公众号
3、巴拉圭的真实世界数据。
这个很重要,因为这是独立于巴西IIT试验结果之外的,可以独立证明普克鲁胺治疗重症有效性的证据。首批给药的巴拉圭25名重症患者,服药14天后,有22名病人病情缓解,1名死亡。如果按照1名死亡计算,死亡比例4%,如果按照其余2名最终也死亡计算,死亡率是12%。和当时南美洲地区的重症死亡率比较,普克鲁胺的死亡率下降幅度是巨大的,而且和巴西的IIT重症数据相吻合。
熟悉统计学的都知道,当你在一个样本中发现了一个规律,要知道这个规律是真实存在的还是偶然的,最好用一个全新的样本去检验。如果在新的样本中也验证了这个规律,那么这个规律的可信度就会大大提升。同理,巴拉圭真实世界的数据就是巴西临床之外的新样本,而在这个新样本中,普克鲁胺给出了同样的疗效,从而大大降低了巴西IIT临床结果的偶然性。
来源:公司中期报告
4、开拓药业及其整个团队所做的努力有目共睹
判断一个人或者一家公司,我们不仅要听他怎么说,更要看他怎么做。真的是一种做法,假的是另一种做法。截至目前我看到的,无法让我认为是假的。
(1)资金、资源大量投入,全力以赴三个MRCT
2021年上半年,开拓药业通过资本市场增发配售股份募集资金11.6亿港元,这笔宝贵的资金,已经有超过一半都投入到普克鲁胺治疗新冠的三个全球MRCT中了。如果没有此前一步一步的机理探索以及临床数据的初步检验,如此大规模的投入一个适应症的临床试验,对于一个小的biotech公司来说简直难以想象。
(2)试验覆盖新冠疾病的全周期
不同于其它新冠治疗药物,普克鲁胺是目前唯一一款覆盖新冠非住院和住院全病期的小分子药物。在非住院病人治疗领域,直接竞争对手默克、辉瑞都交出了不同的答卷,但在住院患者治疗领域,默克因莫努匹韦疗效不佳直接宣告放弃,而辉瑞自始至终就没有开展过住院患者相关临床。普克鲁胺是目前全球唯一一款进入Ⅲ期临床的治疗住院患者的新冠口服药,并且已经在美国完成了首例给药。近日,我从乌克兰政府网站的公告中得知,普克鲁胺用于治疗新冠住院患者的Ⅲ期临床试验正式获批。而乌克兰是目前全球疫情最严重的国家之一。进入10月下旬以来,日均死亡人数超过600人,仅次于俄罗斯,排在全球第二。在这样的疫情下,临床试验的入组速度会是怎样,不难想象。
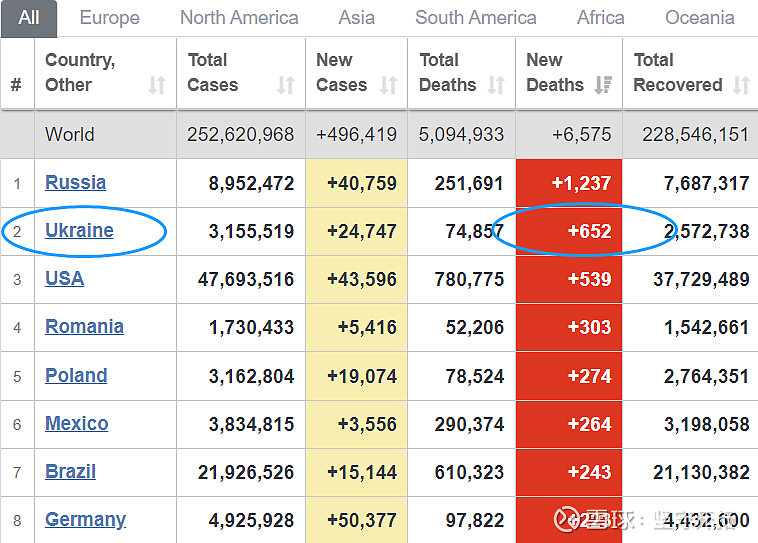
图35:乌克兰疫情数据
(3)机理补课持续进行中,不断有新的成果(重症机理、动物试验)
除了临床试验的有序推进,开拓药业也在对机理的研究不断深入探索。在今年年中业绩发布会上,公司公布了普克鲁胺治疗新冠重症的机制——提高巨噬细胞和单核细胞中Nrf2转录因子反应元件与DNA结合的活性,通过激活Nrf2通路,诱导细胞保护基因及相关基因的表达,并进一步提高抗氧化和细胞保护蛋白质的表达,从而减弱或消除病毒病原体。这一研究是和北京蛋白研究中心共同完成的。另一方面,公司也在持续进行动物试验的补充,以便让不同国家临床申请流程更加顺畅。比如在印度,开拓药业就因缺少动物试验数据未通过初次IND申请。到了11月初,公司在补交了动物试验的数据后,才得到了印度药监局(CDSCO)的批准,在印度开展普克鲁胺治疗新冠非住院病人的Ⅲ期临床试验。
(4)临床试验条件最苛刻,彰显对普克鲁胺的信心
在临床设置上,开拓药业、默克、辉瑞的新冠药看似大同小异,其实暗藏玄机。在10月1日默克公布的首份试验结果公告上,只字未提一个重要信息——莫努匹韦的入组患者全部都没有接种过新冠疫苗。更让人难以置信的是,默克公司甚至都没有在clinicaltrials网站上公布这一入组规则,直到10月11日公司再次公告向FDA申请EUA的时候,才将这一信息向公众公布。这条可能会对莫努匹韦获批EUA的适用范围产生较大影响的信息,公司却没有第一时间公告。同样,辉瑞也没有在公告里提示入组患者未接种疫苗,但稍好的是,在clinicaltrials网站上是可以查到相关描述的。两家制药巨头在这个问题上如出一辙的小动作,骗不过FDA这样的专业机构,但却足以达到迷惑普通投资人的效果。
反观普克鲁胺的临床设置,就没有包含这一标准。疫苗作为第一道防线,能在很大程度上降低患者住院率。那么在以降低住院率为主要临床终点的试验中,就会很大程度上降低对照组的住院率。理论上,疫苗会对试验组和对照组产生同样的影响,但在真实世界中,在第一道防线的基础上,更多一层的防护一定是边际效用递减。换句话说,因为疫苗的存在,会在很大程度上拉低药效的统计学差异。如果再考虑样本大小,那么实际结果中,一两个病人的差异,就会对结果产生非常大的影响。这样的设置,侧面印证了公司对药效的信心——即使在诸多不利的客观条件下,依然有很大希望在小的样本中得到统计学显著性。当然,这样的设置也有好的一面,在申请EUA的时候,能不挑病人、最大程度反应真实世界数据的临床结果一定会更容易说服专业的药审机构(FDA等)。
(5)自产与CDMO合作双管齐下提前储备产能
为了新冠口服药潜在的巨大市场需求,开拓药业已经提前在苏州、浙江以及海南做好了产能准备。预计到今年Q4,可以达到每月5000万片的产量,即每年超过2000万疗程的供应。考虑到中国世界工厂的重要地位,以及小分子药扩产的难度较低,如果市场需求超过预期,我相信公司也可以很好地应对。
来源:公司中期报告、公司公众号、clinicaltrials网站
今年7月15日,开拓药业公告,和复星医药就普克鲁胺治疗新冠在印度和非洲商业化达成合作协议。复星医药没有公告该合作协议,但我直接致电复星医药,得到了肯定的答复。在复星医药稍后发布的半年报上,该信息得到了进一步确认。复星医药的战略眼光有多厉害,从一组数据比对就可以看出。BioNTech公司的mRNA新冠疫苗,是在2020年3月17日和辉瑞公司达成合作协议的。而复星医药在2020年3月14日就和BioNTech达成了合作协议(复必泰),他们的动作甚至比辉瑞还要快。以复星医药的专业眼光,这么着急签下开拓药业的普克鲁胺,告诉我们什么呢?
来源:公司公告
三、我的判断——信
在我们相信一家上市公司之前,首先应该不相信它。因为历史上发生过太多的造假事件。对开拓药业也应该是这个态度。我一直提醒自己,应该以客观的态度去面对不信与信反正两方,因为这关系到我们的本金安全。把上文分析的反正两方论点和论据结合起来思考,我认为:
1、我确实没有能力搞清楚巴西IIT的所有细节,所以我很关注独立于巴西以外的可以验证巴西数据真实性的证据。很庆幸,我找到了巴拉圭真实世界的有效性证据,在对相关官员、视频、具体言论的反复研究后,我认为巴拉圭的论据造假的可能性很低,一个没有和中国建交、身居高位的巴拉圭政府官员且是医院院长的专业人士,没有动机、面对国家灾难、面对自己国家人民的生命威胁的大背景下,如果不是因为普克鲁胺确有奇效,是不会为普克鲁胺背书的。巴拉圭25名重症患者的真实世界数据与巴西IIT临床试验数据的高度吻合,是我相信普克鲁胺最终能成功的重要基础。(为啥只是25名,紧急授权了可以扩大范围啊)
2、即使我们回到巴西IIT临床试验本身,一是我没有看到任何关于普克鲁胺治疗新冠非住院临床试验结果的质疑报道。二是针对住院临床的质疑集中在过程的合规和严谨性方面,而对于有效性方面,只有一个独立数据委员会签字的疑问,没有找到其他质疑的报道。三是巴西ANVISA已经批准了普克鲁胺非住院和住院的MRCT临床试验,如果ANVISA认为开拓之前的临床存在严重的问题,为什么还会批准呢?当然,还有其他了解的信息,我至今无法作为信与不信的依据,在此列出以备反思之用:巴西总统的三次称赞反而引来反对派的狂轰乱炸?临床试验所处时期正是巴西疫情最严重的时期,那时候PI所做的非常规操作到底能否理解和解释呢?PI造假所要付出的代价与其可能获得利益之间合乎逻辑吗?
3、我们做投资再怎么研究都不可能作到专业的程度,所以借助其它专业机构的言、行来辅助我们判断是一个有效的方式。FDA、ANVISA、NMPA和CDSCO先后批准临床(且在过程中都各自提出不同的难题,最终都被开拓药业克服),复星医药快速签署里程碑合作(复星医药历史上买买买体现的稳准狠),都是我选择相信的辅助依据。
4、投资归根结底是投人,是投资一家企业的灵魂人物及其带领的团队。从普克鲁胺被世人瞩目的过程,我看到的是以童友之博士为核心的开拓药业团队,以自己敏锐的眼光、专业的素养以及攻坚克难地执行力,一步一个脚印的努力结果。而并非某些人说的撞大运得来的。我按照识别造假的标准流程,试图搜索有关开拓药业及其创始团队的负面报道,但一无所获。从童友之博士的履历,我看到的是师出名门的背景,其在美国著名高等学府康奈尔大学攻读博士时,师从大师Joseph Bertino教授(美国癌症研究领域的顶级专家,曾担任美国癌症研究协会(AACR)主席)。在难得的几次联合调研中,我也不断地验证开拓药业高管团队的言、和后来的行之间是否吻合,一一验证不断给我信心。
综上,我认为巴拉圭真实世界数据的独立性验证了巴西IIT临床数据的可信性,加之我对开拓药业及其高管团队言行一致的观察,进一步确认了开拓药业在普克鲁胺治疗新冠的可信性和可行性。从而给了我判断普克鲁胺最终能够成功的信心。也只有得出之前信息的可信性判断后,才能得出以下的判断:普克鲁胺治疗新冠非住院和住院的MRCT临床试验并不是一次对有效性的赌博,而是按照标准临床要求,重现之前有效性的过程,成功概率极高!
作者:坚守开拓
链接:网页链接
来源:雪球
著作权归作者所有。商业转载请联系作者获得授权,非商业转载请注明出处。
风险提示:本文所提到的观点仅代表个人的意见,所涉及标的不作推荐,据此买卖,风险自负。
粗斜体是自己的疑问