近日,复星医药旗下万邦医药的冻干制剂生产线顺利通过欧盟GMP现场检查,并收到了荷兰卫生监督机构Health and Youth Care Inspectorate签发的GMP现场检查最终报告、检查关闭信及GMP检查证书,标志着其质量管理体系和生产能力再次得到国际权威认证机构的认可,进一步提升了公司的全球竞争力。
6月25日,国家药品监督管理局官网显示,药友制药的注射用尼可地尔(12mg)获批上市并视同通过仿制药质量和疗效一致性评价。
7月5日,国家药品监督管理局官网显示,药友制药的阿仑膦酸钠片(70mg)获批上市并视同通过仿制药质量和疗效一致性评价。
复星医药:万邦医药冻干制剂生产线再次通过欧盟GMP现场检查,质量管理获国际认可
近日,复星医药旗下万邦医药的冻干制剂生产线顺利通过欧盟GMP现场检查,并收到了荷兰卫生监督机构Health and Youth Care Inspectorate签发的GMP现场检查最终报告、检查关闭信及GMP检查证书,标志着其质量管理体系和生产能力再次得到国际权威认证机构的认可,进一步提升了公司的全球竞争力。
本次现场检查生产线为注射剂生产线4,目标产品为注射用帕瑞昔布钠,主要用于手术后疼痛的短期治疗。该生产线于2019年首次通过欧盟GMP现场检查。

欧盟(European Union)作为全球重要的药品市场之一,近30个成员国之间的“GMP认证/检查(GMP Inspection)”结果是彼此互认/共享的,同时也与美国、日本、澳大利亚及加拿大共享检查结果,这使得欧盟GMP认证/检查在全球范围内的影响越来越大。
复星医药持续推进生产体系的整合,强化规模化、有成本竞争力的制造体系,最终实现全球产能产型的统筹规划。截至2023年末,复星医药集团核心制药板块国内控股子公司所有商业化生产线均已通过国内GMP 认证,并有9条生产线通过美国、欧盟等主流法规市场GMP 认证。同时在国内,复星医药正在建设两大综合制剂制造中心及三大原料药生产基地,逐步夯实原料制剂一体化的产业优势。
多年来万邦医药始终秉持“质量第一,客户至上,全面管理,持续改进”的质量方针,积极理解、执行GMP、EU GMP、cGMP 及相关附录,并充分参考ICH、WHO、PIC/s及各类指南要求,不断提升质量管理体系,持续对标世界一流标准,推进公司质量体系与国际接轨。
未来,万邦医药将继续完善质量管理体系,为更多国际化产品实现商业销售做好充分准备,发挥协同效应,以更高标准服务全球患者,为更多大众提供更优质、更可及、更可负担的产品与服务。
复星医药:药友注射用尼可地尔获批上市
6月25日,国家药品监督管理局官网显示,药友制药的注射用尼可地尔(12mg)获批上市并视同通过仿制药质量和疗效一致性评价。
注射用尼可地尔
注射用尼可地尔最早于1993年在日本获批上市,用于不稳定型心绞痛。后在2007年增加适应症,用于急性心功能不全(包括慢性心功能不全的急性加重期)。
尼可地尔是全球首个上市的钾离子通道开放剂,既能有效控制心绞痛症状,又能改善预后,兼具ATP依赖的钾通道开放作用及硝酸酯样作用,且对血压、心率和心肌收缩力无影响。
尼可地尔通过阻止细胞内钙离子游离,增加细胞膜对钾离子的通透性,实现冠状动脉扩张作用,有效扩张各级冠状动脉,尤其是冠状动脉微小血管,从而缓解痉挛,显著增加血流量。
目前,国内外多指南推荐尼可地尔用于各类型冠状动脉综合征的治疗,如:《非ST段抬高型急性冠状动脉综合征诊断和治疗指南(2024)》:尼可地尔可用于硝酸酯类药物不能耐受或血管痉挛性心绞痛的患者;《ST段抬高型心肌梗死基层合理用药指南(2021)》:推荐尼可地尔用于对硝酸酯类不能耐受的ST段抬高型心肌梗死患者;《欧洲心脏病学会慢性冠脉综合征诊断和管理指南(2019)》:尼可地尔显著降低冠心病死亡、非致死性心肌梗死或因疑似心绞痛症状意外入院的复合情况,推荐其作为慢性冠脉综合征的二线用药;《冠心病合理用药指南(2018)》:尼可地尔对稳定型心绞痛和其他各型心绞痛均有明显疗效,可作为减轻症状的治疗药物。
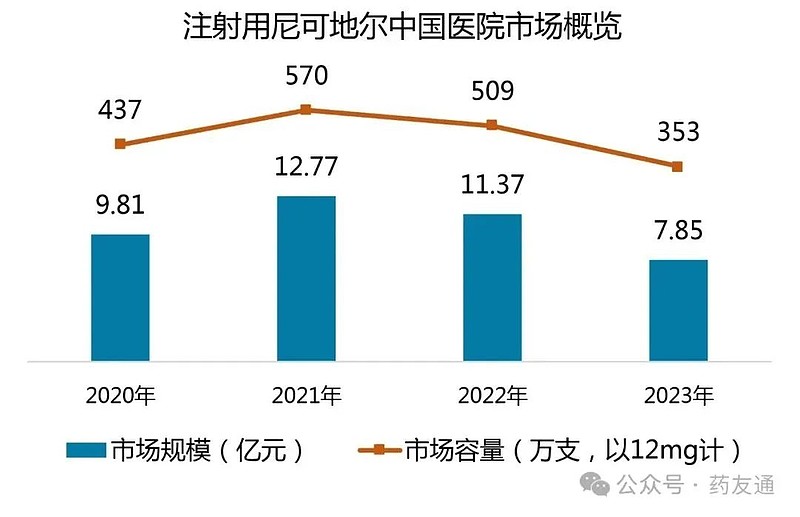
2012年,注射用尼可地尔在我国获批上市,用于不稳定型心绞痛。IQVIA数据显示,2023年该产品中国市场规模7.85亿元,市场容量353万支(以12mg计)。
截至发稿,注射用尼可地尔已有10+家企业通过或视同通过一致性评价,有望纳入第十批国家带量采购。
药友制药在心血管领域已有多款产品上市,此次注射用尼可地尔的获批,将进一步丰富产品群,助力产品布局更加完善和多元化。
复星医药:药友阿仑膦酸钠片获批上市
2024年7月5日,国家药品监督管理局官网显示,药友制药的阿仑膦酸钠片(70mg)获批上市并视同通过仿制药质量和疗效一致性评价。

阿仑膦酸钠片
1993年在意大利首次上市,后于1995年在美国上市,现已获批用于:
治疗和预防绝经后妇女骨质疏松症
治疗男性骨质疏松症以增加骨量
治疗糖皮质激素诱导的骨质疏松症
治疗Paget骨病
阿仑膦酸钠片是首个获得FDA批准用于治疗绝经后骨质疏松症的双膦酸盐类药物,也是第一个被FDA批准用于治疗男性骨质疏松症的药物。双膦酸盐能够特异性结合到骨重建活跃的骨表面,抑制破骨细胞功能,从而抑制骨吸收,防止骨丢失,增加骨量。阿仑膦酸钠片用于骨质疏松症的治疗已有30年历史,其疗效和安全性得到了充分的临床认证和医患认可。
目前,阿仑膦酸钠被国内外多指南推荐用于各类型骨质疏松症的初始治疗,如:
《美国医师协会(ACP)临床指南:药物治疗成人原发性骨质疏松症或低骨量以预防骨折(2023)》:双膦酸盐应作为女性和男性原发性骨质疏松的一线治疗药物。
《原发性骨质疏松症诊疗指南(2022)》:对于骨折高风险者建议首选口服双膦酸盐(如阿仑膦酸钠)。
《老年脆性骨盆骨折临床诊疗指南(2022)》:双磷酸盐类药物是抗骨质疏松药物治疗的首选药物。所有老年脆性盆骨患者均应尽早、序贯、长期抗骨质疏松治疗。双磷酸盐类药物因安全、有效、依从性佳等而被临床广泛应用。
《男性骨质疏松症诊疗指南(2020)》:无论是原发性骨质疏松症或部分继发性骨质疏松症,非转移性前列腺癌接受雄激素剥夺治疗、HIV相关性骨质疏松症、糖皮质激素诱导的骨质疏松症等,口服阿仑膦酸钠均有效增加腰椎、髋部或股骨颈骨密度。
《欧洲绝经后妇女骨质疏松症诊断和治疗指南(2019)》:口服双膦酸盐(如阿仑膦酸钠等)可作为初始治疗,阿仑膦酸钠可以同时降低椎体骨折和非椎体(包括髋关节)骨折风险。
1999年,阿仑膦酸钠片在我国获批上市,用于治疗绝经后妇女的骨质疏松症,以预防髋部和脊柱骨折(椎骨压缩性骨折),还可用于治疗男性骨质疏松症以增加骨量。
目前,阿仑膦酸钠片为国家医保乙类品种,国家基药。近年市场持续攀升,国内市场规模已达4亿元,市场容量1140万片(以70mg计)。
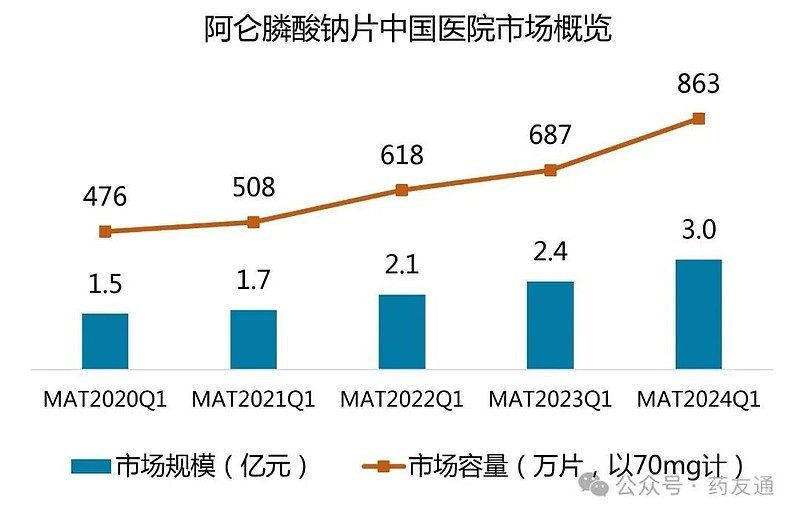
数据来源:IQVIA
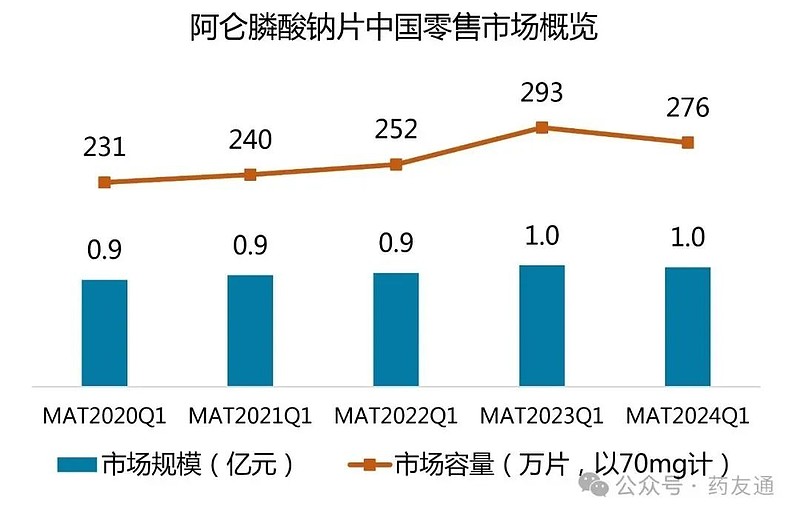
数据来源:RPDB
截至发稿,阿仑膦酸钠片已有5家企业通过或视同通过一致性评价,尚有6家企业正在审评审批中,可能纳入第十批国家带量采购。
通过/视同通过一致性评价的企业
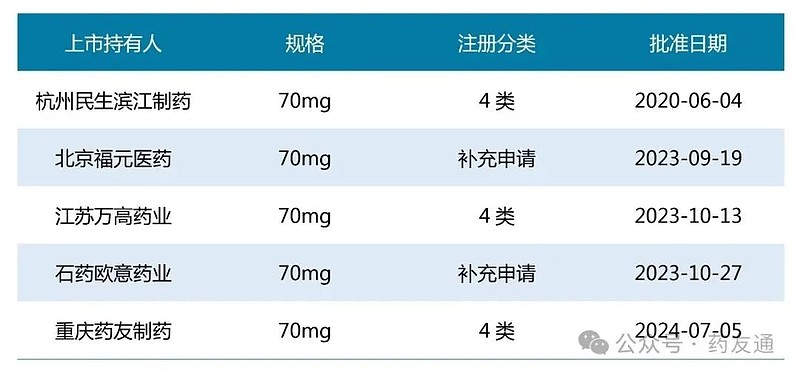
正在审评审批的企业
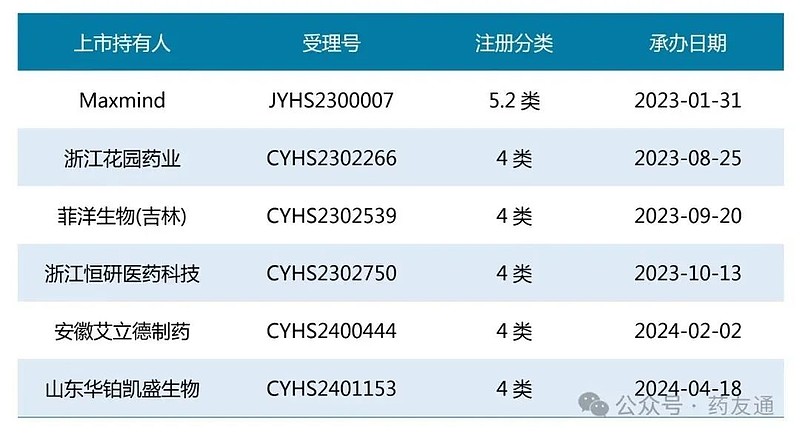
骨质疏松是药友制药重点布局的领域之一,核心产品“立庆®(阿法骨化醇片)”市场占有率处于全国第1位,全球第2位。(数据来源:IQVIA)
此次阿仑膦酸钠片的获批,将进一步丰富药友制药骨质疏松产品管线,为患者提供全新的用药选择。$复星国际(00656)$