
2024年6月17日
医麦客新闻 eMedClub News
近日,IN8bio在2024欧洲血液学协会(EHA)年会上展示了其在研现货型γδ T细胞疗法INB-100的最新1期临床试验结果。试验结果显示,100%可评估的白血病患者(n=10)在接受治疗一年后维持完全缓解(CR)。数据同时显示接受单次治疗后365天里,同种异体γδ T细胞长期持久的体内扩增。新闻稿指出,这是首次同种异体细胞疗法表现出持续的扩增和持久性。

γδ T细胞因其可异体移植的天然优势和在实体肿瘤治疗中展现出的巨大潜力,开始获得越来越多的关注。γδ T细胞是人体先天免疫系统的一部分,它们表面用于识别抗原的T细胞受体由γ链和δ链组成,而不是常规的α链和β链。与其他类型的T淋巴细胞不同,γδ T细胞不需要与主要组织相容性复合物(MHC)分子结合,可以直接识别并结合靶细胞抗原,因此肿瘤细胞不能通过下调MHC蛋白表达来逃脱攻击。这一特性意味着肿瘤可能更难对γδ T细胞产生耐药性。此外,γδ T细胞在具有和自然杀伤细胞类似的杀伤能力同时,具有分辨健康细胞和肿瘤细胞的能力。
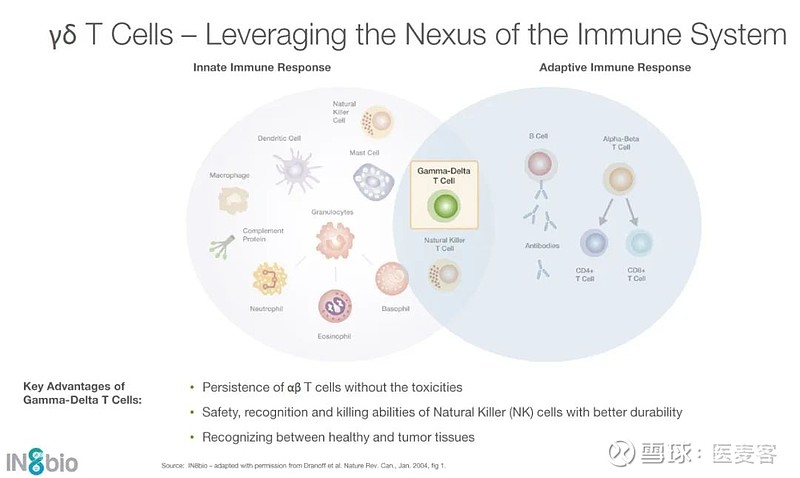
▲γδ-T细胞简介(图片来源:IN8bio公司官网)
INB-100是一款来自健康供体的同种异体γδ T细胞,在体外经过扩增和激活后,被输注到白血病患者体内。在这项研究者发起的1期临床试验中,白血病患者在接受造血干细胞移植后,接受一剂INB-100的治疗。这些患者包括高风险和复发急性髓系白血病(AML)患者,他们此前已接受过多种疗法治疗,包括CAR-T细胞疗法。
试验数据显示,截至2024年5月31日,100%可评估的白血病患者仍然存活并且维持完全缓解达到1年。此前发表的历史数据显示,高达50%的血液癌症患者在接受造血干细胞移植和减轻强度预处理(reduced intensity conditioning)的情况下会出现复发,并且在复发后不久去世。在这10名患者中,两名接受INB-100治疗的患者已经无癌三年半,另一名患者接近3年无癌。
安全性方面,INB-100没有出现剂量限制性毒性,未发现细胞因子释放综合征(CRS),神经毒性或免疫效应细胞相关神经毒性综合征(ICANS),未发现严重感染。在这项临床试验中,一名患者由于特发性肺纤维化去世,这是移植治疗的已知毒性。两名携带TP53突变的患者(包括一名费城染色体阳性急性淋巴细胞白血病患者和一名骨髓增生异常/骨髓增生性肿瘤综合征患者)虽然出现复发但仍然活着。
这项临床试验已经扩展患者注册,将招募10名新患者接受2期临床试验推荐剂量的治疗。IN8bio计划在今年夏天与FDA会晤,讨论注册性临床试验的规划。
参考资料:
[1] IN8bio Presents Positive Data Demonstrating Durable 1-year Complete Remission in 100% of Evaluable Patients in Phase 1 Trial of INB-100. Retrieved June 13, 2024, from 网页链接
[2] IN8bio. Retrieved June 13, 2024, from 网页链接
声明:本文旨在于传递行业发展信息、探究生物医药前沿进展。文章内容仅代表作者观点,并不代表医麦客立场,亦不构成任何价值判断、投资建议或医疗指导,如有需求请咨询专业人士投资或前往正规医院就诊。

点点“分享”、“点赞”和“在看”,给我充点儿电吧~