
2024年6月7日
医麦客新闻 eMedClub News
近日,Intellia Therapeutics宣布其在研疗法NTLA-2002正在进行的1/2期研究中1期部分的长期数据。NTLA-2002是一款CRISPR基因编辑疗法,正在开发为治疗遗传性血管性水肿(HAE)的一次性治疗方案。
HAE是一种罕见的遗传病,会导致可能危及生命的肿胀发作,大约50000人中有1人患病。其特征是身体各个器官和组织中出现严重、反复和不可预测的炎症发作,让患者倍感痛苦、衰弱。目前的治疗选择通常是终身治疗,需要每周两次慢性静脉内给药或皮下注射给药,或每天口服给药。但即使长期用药,仍会发生突破性发作。
NTLA-2002的1/2期临床研究长期随访数据显示,单剂量NTLA-2002给药导致HAE患者的每月发作率平均减少98%,中度至重度发作平均减少了99%,所有患者平均随访超过20个月。在测试的每个剂量水平上,HAE发作率均显著减少。单次输注后,患者最长的无发作期超过26个月,并且仍在持续。
此外,HAE症状最严重的患者中,发作减少的效果也非常显著。研究开始时每月HAE发作率最高的两位患者(分别为16.8和14.0次/月)在16周的主要观察期结束时无发作,并且在最新的随访中依然无发作。这两位患者中最长的无发作持续时间为23.5个月,并且仍在持续。此外,100%接受NTLA-2002治疗的患者在停止其他预防性治疗后后无需再进行预防性治疗。
6月14-15日
IBI EXPO
主题论坛推荐
上下滑动查看更多
扫码
限时领取
免费门票

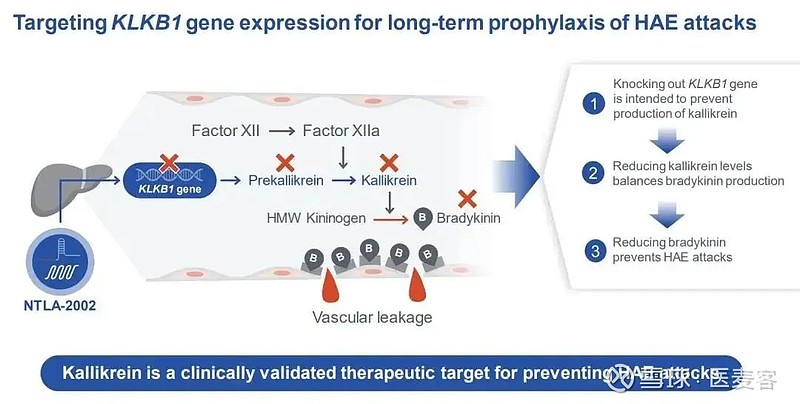
NTLA-2002是一种体内CRISPR基因编辑候选疗法,通过脂质纳米颗粒(LNP)以mRNA形式递送CRISPR-Cas9基因编辑系统,靶向敲除血浆前激肽释放酶基因(KLKB1),以永久性降低血浆中激肽释放酶活性,从而防止遗传性血管水肿的发作。
2023年3月2日,Intellia Therapeutics宣布,FDA批准了NTLA-2002的新药临床试验研究(IND)申请。这也是首个获得FDA批准用于人体临床试验的LNP递送的体内CRISPR基因编辑疗法。
今年2月,著名医学期刊《新英格兰医学杂志》(NEJM)重磅发表NTLA-2002治疗遗传性血管水肿成人患者的1期剂量递增部分试验数据。
参考来源:
[1]网页链接
声明:本文旨在于传递行业发展信息、探究生物医药前沿进展。文章内容仅代表作者观点,并不代表医麦客立场,亦不构成任何价值判断、投资建议或医疗指导,如有需求请咨询专业人士投资或前往正规医院就诊。



了解行业、洞察趋势、发掘潜力。来这里,就对了!