2024年4月29日
医麦客新闻 eMedClub News
1980年,人类就通过疫苗灭绝了天花病毒。自此,疫苗领域繁荣发展,乙肝、HPV、狂犬、百白破、乙脑等。然而,治疗性癌症疫苗却进展缓慢,40年来一直很难有所突破……
随着由Moderna和默沙东(MSD)主导的新型癌症疫苗mRNA-4157接近关键临床试验读数,FDA生物制品评估和研究中心(CBER)主任——“疫苗沙皇”Peter Marks博士表示,“尽管人工智能(AI)存在相关的未知数,FDA 已准备好审评这些疫苗。”
在2024年世界疫苗大会(WVC)上,Marks博士谈到癌症疫苗时说:“我们准备好了审查,我们对这类疗法的商业化持开放态度。面对到来的治疗性mRNA癌症疫苗的审评审批,我认为我们会像审评CAR-T细胞或其他治疗产品一样对它们进行审评。”
FDA之前已经批准了一种癌症疫苗,即Dendreon的前列腺癌疫苗Provenge(普列威)。尽管下一波治疗性癌症疫苗的目标是通过常见的临床终点(如肿瘤进展)来证明疗效,但其技术的新颖性引发了新的监管问题,也将带来新的审批政策。
癌症疫苗显著降低癌症转移或死亡风险达
eMedClub
2022年12月13日,由默沙东与Moderna联合开发的个体化癌症疫苗mRNA-4157/V940与PD-1抑制剂K药(帕博利珠单抗)的组合疗法,在临床2b期试验当中显示,该研究达到五年无复发生存率(RFS)主要终点,与Keytruda单药治疗相比,组合疗法可以显著降低III、IV期黑色素瘤患者在肿瘤完全切除后的复发或死亡风险达44%!
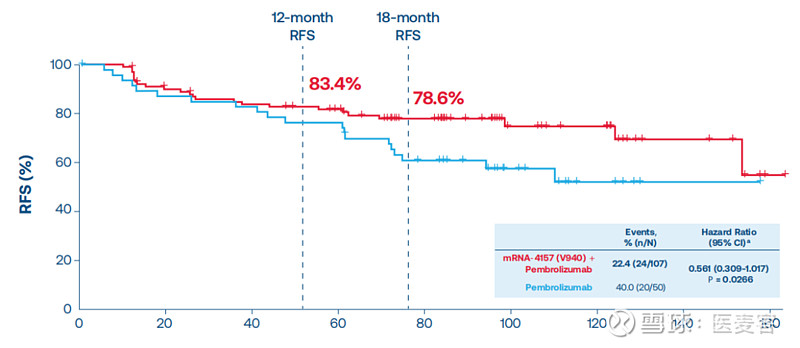
▲ mRNA-4157联合帕博利珠单抗可将复发或死亡风险降低44%
2023年12月14日,Moderna和默沙东宣布2b期临床试验KEYNOTE-942/mRNA-4157-P201的3年随访积极结果。在三年期内,mRNA-4157联合PD-1疗法K药使用可使皮肤癌黑色素瘤患者的复发风险降低49%(HR=0.510,95% CI:0.288-0.906;单侧p=0.0095),并改善远处转移生存期(DMFS),使患者的远处转移或死亡风险降低62%(HR=0.384,95% CI:0.172-0.858;单侧p=0.0077)。
根据如上这个KEYNOTE-942数据,美国FDA和欧洲药品管理局(EMA)分别授予mRNA-4157与帕博利珠单抗组合突破性疗法认定(BTD)和PRIME资格。在黑色素瘤适应症外,Moderna还针对mRNA-4157用于非小细胞肺癌启动了3期临床研究,用于膀胱癌、肾细胞癌启动了2期临床研究。
2023年底,Moderna首席执行官Stéphane Bancel接受采访时曾表示,“Moderna针对黑色素瘤的mRNA癌症疫苗可能在两年内上市,这将是抗击这种最严重形式的皮肤癌的里程碑式一步。”Stephane Bancel表示,“我们认为,在一些国家,这款mRNA癌症疫苗可以在2025年前获得加速批准上市。”
今年2月,《柳叶刀》文献报道了mRNA-4157在美国和澳大利亚进行的多机构的2b期研究结果,与K药(PD-1抑制剂,ICIs)单药治疗相比,mRNA-4157治疗联合K药,显著延长了术后高危黑色素瘤患者的无复发生存期,并显示出可控的安全性。
个体化癌症疫苗是如何制造出和应用?
eMedClub
个体化癌症疫苗的目的是通过根据患者个体化肿瘤突变类别设计的疫苗,可帮助患者产生相对应的抗肿瘤反应,进而提升癌症患者的免疫能力。癌症疫苗的制造和应用步骤简化如下:①肿瘤样本采集 → ②基因组测序→ ③新抗原预测和筛选→ ④疫苗设计和生产→ ⑤质量控制→ ⑥患者接种→ ⑦监测与评估。

▲ 个体化新抗原癌症疫苗的制造和应用流程
Moderna公司的技术平台对患者的肿瘤和健康组织进行测序,并通过使用一种专有算法,识别出免疫原性肿瘤特异性新抗原。其算法能够基于人体外测定数据,高准确度的预测和筛选具有TIL反应性的新生抗原,mRNA-4157就是在此算法下诞生。

▲ 新生抗原的筛选算法概览
新生抗原构成了疫苗构建的基础,而由此产生的蛋白质在个体之间可能存在很大差异。mRNA-4157是一种基于mRNA的新型研究型个体化新抗原疗法(INT),由编码多达34种新抗原的合成mRNA组成,这种mRNA是根据患者肿瘤DNA序列的独特突变特征设计和生产的。

▲ Moderna个体化癌症疫苗设计
对于mRNA-4157来说,AI决定个体化疫苗应该如何制定来攻击癌症。该疫苗在给药到体内后,算法衍生、RNA编码的新抗原序列被内源性翻译并进行天然细胞抗原加工和呈递,这是适应性免疫的关键步骤。
Moderna的治疗学和肿瘤学发展负责人Kyle Holen在世界疫苗大会的场外告诉记者,“由于AI是该项目的核心组成部分,Moderna预计作为mRNA-4157审评的一部分,FDA 将需要审查其算法。Holen接着说,我们必须把我们的算法放在硬盘上,装在'装甲车'里,然后运到FDA。”
众所周知,AI算法在吸收新信息的过程中不断进化。但是为了保护基于AI疫苗的临床试验的完整性,Moderna不得不在研究之前“锁定”算法,以避免任何可能导致结果混乱的变化,Holen补充说。
所有这些都提出了一个新的监管问题:在疫苗被认为是一个全新的产品之前,AI算法允许多大的改变?Holen说,“我们不知道,没人知道。这里是无人区,因为没人做过这种事。”
FDA对于癌症疫苗的新技术打算这样管
eMedClub
Moderna与美国FDA就mRNA-4157疫苗项目进行沟通,探讨了更换基因组测序的供应商和调整抗原数量范围的影响,这些变更将被认为是对项目的重大修改。然而,目前尚未明确这些调整是否需要提交新的补充申请,或是在首次获得批准后,针对任何重大变更提交全新的新药申请。
考虑到癌症疫苗可能需要频繁更新,要求每次更新都经过全面的审评或进行大型随机临床试验似乎不切实际。因此,FDA的Peter Marks博士提出,美国FDA正在考虑的平台技术认定(platform technology designation)可能针对该问题提供了解决方案,目的是为了让使用相同平台技术开发的产品享受到更简化的审评流程。
虽然FDA提出“平台技术认定”的概念已有一段时间,但Marks博士指出,该概念尚未得到充分应用。他强调,mRNA技术的应用将迫使FDA积极探索并扩大这一理念的应用范围,以适应新兴技术的发展。
结语
eMedClub
在近十来年针对癌症的研究中,人们发现不同病人身上的同种癌症具有大相径庭的药物应答、细胞毒性以及预后,因此为不同的病人裁剪特定的癌症治疗方案成为一种极具潜力的手段。继PD-1/PD-L1和CAR-T疗法之后,个体化癌症疫苗逐渐成为肿瘤免疫治疗新的发展方向。未来,除了mRNA-4157,mRNA-5671、BioNTech与基因泰克(Genentech)的autogene cevumeran(RG6180)等mRNA癌症疫苗在抗击实体瘤上均展现了有力前景。这些个体化的癌症疫苗有望获批消息让大家感到兴奋。
个体化新抗原癌症疫苗兴起之下也显现了些问题。如前面提到的测序供应商变更,抗原数量范围调整这样的疫苗生产制造上的变化是否会影响抗癌效果?另外,如mRNA癌症疫苗是否专注于对抗组织中的癌细胞而不伤害健康组织?需要靶向的最佳抗原是什么?疫苗产品的最佳佐剂是什么?哪种免疫检查点抑制剂(ICIs)能最好地提高癌症疫苗的疗效?
为紧抓行业当下面临的机遇,推动行业共同发展。医麦客将于2024年6月14-15日在南京举办2024 IBI EXPO生物创新药产业大会,并召开“第三届核酸药物开发论坛”,探讨“人工智能加速mRNA癌症疫苗开发”这一热议话题。本次会议将邀请该领域的先锋与领袖,聚焦最新研究动态与进展,深度探讨和展望核酸药物开发的未来发展趋势。
//
2024 IBI EXPO 日程一览


扫码
限时领取
免费门票

参考资料:
[1] 'We're open for business': FDA's Peter Marks says agency ready to review novel cancer vaccines despite unknowns ,from 网页链接
声明及版权说明
声明:本文旨在于传递行业发展信息、探究生物医药前沿进展。文章内容仅代表作者观点,并不代表医麦客立场,亦不构成任何价值判断、投资建议或医疗指导,如有需求请咨询专业人士投资或前往正规医院就诊。
版权说明:本文来自医麦客内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台,转载授权请在文章下方留言获取。

点点“分享”、“点赞”和“在看”,给我充点儿电吧