
2023年12月21日/医麦客新闻 eMedClub News/--2023年12月19日,UNIQURE宣布了AMT-130基因疗法治疗亨廷顿舞蹈症(HD)的最新I/II中期数据,可稳定亨廷顿病患者的症状。该临床试验正在美国和欧洲进行,招募了39名患者并进行长达30个月的随访。AMT-130受试者在运动技能、功能独立性和综合评分的评估中观察到改善的趋势。并且,AMT-130在低剂量和高剂量下仍然具有良好的耐受性和可控的安全性,神经元退化和疾病进展的测量指标NfL(神经丝轻链蛋白)均进一步下降。未来将继续跟踪这些患者,并期待明年启动监管互动。

亨廷顿舞蹈症(HD)又称大舞蹈病,是一种神经退行性疾病,症状通常表现为短暂不受控地装鬼脸、点头、手指跳动,随病情加重甚至出现吞咽困难等症状。它是由HTT基因中胞嘧啶-腺嘌呤-鸟嘌呤(CAG)三核苷酸序列的扩增引起的,由此产生超长的突变HTT蛋白会损害脑细胞,并逐渐破坏神经元。据EMA称,亨廷顿氏病影响美国和欧洲约 70,000 人,成为罕见病领域最大的临床未满足需求之一。人的神经系统与免疫系统的性能是亨廷顿舞蹈症等神经退行性疾病难治的部分原因,目前尚没有可用于治疗该疾病、延缓其发作或减缓患者衰退进展的疗法。

▲ 亨廷顿氏病(图片来源:trypanophobia.wordpress)
因此,降低亨廷顿蛋白(HTT)成为减缓或停止亨廷顿氏病神经退行性病变的重要治疗思路。uniQure的基因治疗产品候选药物AMT-130利用其专有的miQURE™沉默技术,由携带人工微RNA(micro-RNA, miRNA)的AAV5载体组成,该载体专门用于沉默亨廷顿基因,并抑制突变HTT蛋白的产生。AMT-130是通过神经外科手术进行患者给药,将在全身麻醉的患者颅骨上钻2-6个小孔,使用微型导管将其注入大脑的两个特定区域(尾状体和纹状体),相当于在大脑建立一个小工厂,并持续生产基因“解毒剂”,阻止亨廷顿蛋白的生产。AMT-130临床前研究显示,单剂AMT-130治疗可改善脑细胞功能、逆转亨廷顿病神经病理学的变化、并且可以实现海马体体积损失的部分逆转。

▲ 给药方式(图片来源:QURE官网)

基因疗法专场论坛
基因疗法的最新临床进展
AAV基因治疗药物在神经领域的最新进展
靶向不同组织的高效性和靶向性的新型AAV载体开发
高分泌型AAV载体基因疗法的应用
LNP体内递送基因编辑技术的研发
新型基因编辑技术的研发进展
高特异性CRISPR/Cas12j基因编辑工具研究进展
变形式碱基编辑系统提高安全性与编辑效率
新型碱基编辑技术在体内基因治疗中的应用
即刻预约,
享“早鸟”福利!
合作、演讲,同步招募中
孤注一掷,迎来“积极”数据
eMedClub
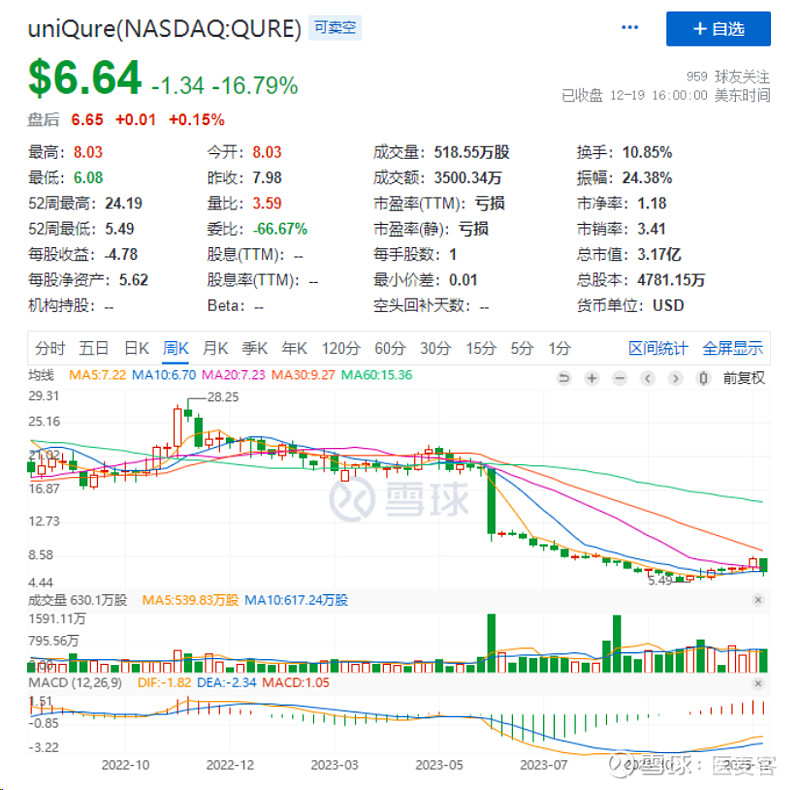
早在今年中旬,uniQure公布了其治疗亨廷顿病的临床I/II期试验的中期数据。公司的研发总裁Ricardo Dolmetsch 博士表示,对在美国进行的AMT-130临床I/II期试验中期结果感到满意。然而市场根本不买账,一天股票跌了40%。近期,uniQure又公布了该实验截止到2023年9月30日的更新数据,虽未能救市,但也未引起上次的大振幅。
探索性功效数据
eMedClub
将每个剂量组中接受治疗的患者临床和功能测量值与基线测量值进行比较,并与对照患者(最长12个月)和非同期标准匹配的自然史组进行比较。该队列包括31名符合uniQure临床试验纳入标准(总功能容量、诊断分类水平和最小纹状体体积)的患者。
➤低剂量组30个月和高剂量组18个月的最新临床数据显示,与非同期标准匹配的自然史相比,存在潜在的剂量依赖性临床益处的持续证据。
➤对于接受高剂量的患者,与治疗前基线测量相比,在18个月时,通过亨廷顿病评级量表(cuhdrs)测量的神经功能及其每个单独组成部分得到维持或改善。
➤对于接受低剂量治疗的患者,与治疗前基线测量相比,通过总运动评分(TMS)和总功能能力(TFC)测量的神经功能在30个月时得以维持。亨廷顿病Total Functional Capacity(TFC)是评价HD患者日常各种生活能力的测量工具,包括独立生活、社交、自我照顾等方面的评估。
➤与自然史队列的预期下降率相比,AMT-130在亨廷顿病评级量表(cuhdrs)、总运动评分(TMS)和总功能能力(TFC)中显示出有利的趋势。
生物标记和体积成像数据
eMedClub
➤参与神经轴突伸长的蛋白NfL(神经丝轻链蛋白),在脑脊液( CSF )中越高,说明大脑损伤越严重。低剂量组的平均NfL在第30个月仍比基线低6.6%。高剂量组的NfL也进一步下降,在第18个月时接近基线,并且没有观察到进一步的增加。所有接受AMT-130治疗的患者都经历了与手术操作相关的NfL的短暂增加,在手术后约一个月达到峰值,此后下降。这些短暂的增加并非为剂量依赖性。
➤突变亨廷顿蛋白(mHTT):鉴于AMT-130直接在脑深部给药,脑脊液中mHTT的药效学不被认为是mHTT在靶脑区域的实质性代表。
➤总脑容量:在外科手术后,用AMT-130治疗的患者总脑容量也未见明显变化,这是积极的信号。
安全性和耐受性
eMedClub
AMT-130总体耐受良好,在6x1012的低剂量载体基因组和6x1013的高剂量载体基因组下都具有可控的安全性。治疗组中最常见的不良事件与手术过程有关。低剂量组、高剂量组、对照组分别有4起、6起、1起与AMT-130无关的严重不良事件(SAE )。而在高剂量队列中有四起与AMT-130相关的严重不良事件(中枢神经系统炎症(n=3)和严重头痛(1)。有症状的中枢神经系统炎症患者用糖皮质激素药物治疗后得到改善。此外,6名高剂量患者接受了围手术期类固醇治疗,同时服用AMT-130以降低炎症风险。
虽然uniQure此款基因疗法的数据并未被市场看好,但uniQure仍从新数据中看到希望,开始在第三个队列中招募患者,以进一步研究两种剂量与围手术期免疫抑制的结合,重点是评估近期安全性。该队列中最多将有12名患者接受治疗,所有患者都将使用当前已建立的立体定向神经外科输送程序接受AMT-130给药。明年第一季度,uniQure计划启动监管互动,以讨论美国和欧洲的数据以及AMT-130持续开发的潜在策略。随后,uniQure预计将展示AMT-130正在进行的I/II期研究的另一项临床更新,包括美国和欧洲试验中接受治疗的患者的额外随访数据。
“屡战屡败”的亨廷顿症为何成香饽饽
eMedClub
uniQure是基因疗法的领军企业,其最有名的战绩莫过于在旗下的血友病B基因疗法Hemgenix于去年11月获FDA批准上市,并在今年2月获欧盟批准上市,这也是全球首款获批上市的血友病B基因疗法。AMT-130能否复制Hemgenix的辉煌,仍未可知。对于这类神经退行性疾病,或许以目前的技术手段来看疾病发展“不退则进”,安全性是首要考虑的。
2022年8月8日,uniQure在其第二季度财报中披露,在一项针对亨廷顿症的1/2期试验中,14例接受高剂量AMT-130治疗组中有3例患者出现了严重副作用。包括脑部肿胀和脑压升高等。但是仅仅是高剂量组出现副作用,低剂量并没有问题。
除了uniQure,不少公司/机构都在研究亨廷顿氏病的基因治疗方法,并研发了全新的治疗路径。拜耳的全资子公司Asklepios其研发的产品BV-101是一种新型的、专门设计的腺相关病毒(AAV)基因治疗载体,可以直接递送目的基因CYP46A1至患者的大脑内,在解决患病神经元的代谢功能障碍的同时有助于突变的亨廷顿蛋白的清除,旨在恢复胆固醇代谢,减少突变亨廷顿蛋白并改善神经元功能,而不会影响细胞中正常亨廷顿蛋白(Htt)的水平。在2022年8月23日,Asklepios宣布通过其子公司BrainVectis在法国进行其针对亨廷顿病(HD)的新型基因疗法BV-101的1/2期临床试验。

回看国内,本导基因旗下的BD112体内基因编辑疗法在今年8月17日获得了欧盟委员会(EC)授予的孤儿药资格认定,该药拟用于治疗亨廷顿舞蹈症。BD112是一款基于原创性VLP递送技术的体内基因编辑创新疗法。VLP可以实现高效、瞬时的CRISPR基因编辑递送。

而小核酸也此疾病中的探索更久。Ionis和罗氏在2013年就以治疗HD的反义寡核苷酸(ASO)——Tominersen 展开合作,这款ASO候选药物和AMT-130原理相似,通过减少所有形式的亨廷顿蛋白(HTT)包括其突变变体(mHTT)的产生治疗HD。2021年3月,由于出现了安全性警告信号,在数据监察委员会的要求下,罗氏终止了Tominersen治疗HD的一项3期临床研究(GENERATION HD1)。随着后续更多数据的审查,罗氏于去年又宣布重启Tominersen,正在结合失败的临床经验设计新的2期临床试验,在疾病负担较轻的年轻成年患者群体中探索不同剂量Tominersen的疗效。今年9月27日,Ionis宣布与罗氏就两个未公开的早期新型RNA靶向项目达成协议,用于治疗阿尔茨海默病(AD)和亨廷顿病(HD)。

在2021年3年,Wave公布了二款ASO药物WVE-001、WVE-002的试验数据,令人失望的是这两个试验受试者的mHTT水平均未出现显著变化。在安全性方面,两款候选药物整体耐受性良好,但也有一小部分参与者出现了严重的副作用。最终,WAVE停止了这两项药物的研发。在两项药物均折戟后,WAVE汲取了教训。研究者发现患者大脑和神经系统不同部位的ASO药物水平并未达到期待值,这或许是PRECISION-HD失败的关键原因。第三款ASO药物WVE-003在分子结构上做了改进,并增加了在动物模型中提前测试ASO药物的步骤。在去年9月20日,WAVE宣布的SELECT-HD临床试验更新结果显示:在接受30或60毫克的队列中,单次给药后85天后观察到脑脊液(CSF)中mHTT较基线平均减少22%(中位减少30%),而wtHTT则被保留下来,与等位基因选择性一致;在安全性方面,30mg、60mg、90mg剂量组整体耐受性良好,未观察到严重不良事件。
亨廷顿病的药品研发之路可谓艰险曲折,然而研究者百折不挠的创新精神让越来越多药品产生了积极的临床数据。而亨廷顿病患者人群在罕见病中较为庞大,尚未有延缓的治疗方法上市,且相对于血友病A,基因疗法企业布局的数量也较少,差异化路线+较大市场缺口既是FDA容易获批的原因,也是市场化之路高歌猛进的王牌,这或许正是屡战屡败的亨廷顿症成为香饽饽的重要原因。
结语
eMedClub
亨廷顿病生物创新药研发仅仅是一个缩影,还有艾滋病、癌症、其他罕见等暂未攻克疾病的创新疗法研发,无不是曲折与前进的统一。但我们相信未来终将会有更多的创新疗法将希望带给患者。
参考资料:
1.网页链接
2.各企业官网
声明及版权说明
声明:本文旨在于传递行业发展信息、探究生物医药前沿进展。文章内容仅代表作者观点,并不代表医麦客立场,亦不构成任何价值判断、投资建议或医疗指导,如有需求请咨询专业人士投资或前往正规医院就诊。
版权说明:本文来自医麦客内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台,转载授权请在文章下方留言获取。

点点“分享”、“点赞”和“在看”,给我充点儿电吧~