引言
目前单克隆抗体(mAb)的生产与纯化工艺已日趋成熟,但抗体捕获仍是下游工艺中的关键技术瓶颈。作为最常使用的主流层析材料,蛋白 A 树脂虽然可以实现较高的结合载量,但也是重要的限速步骤,它需要在低流速下才能能实现高于 30 g/L 的结合载量,从而导致产量较低。因此在过去的十年中,制造商们也在不断改进工艺,以提高产能效率、降低生产成本,以最终惠及患者。
蛋白 A 树脂是以填充床层析柱形式存在,这种形式具有较高的扩散阻力,需要较长的保留时间,且必须在多个批次中重复使用才能达到经济实惠的目标。但这反过来又催生了大量清洁和验证工作,以及繁琐的层析柱装填工作,耗时耗力。
那么是否有更好的层析材料,可以克服现有挑战,在确保产品质量的同时提升效率、加速产能,真正实现降本增效呢?
事实上,新一代层析材料正在出现。

这是一种新型的带蛋白 A 配体的对流扩散(convecdiff)层析膜,包含高结合凝胶相,具有短扩散路径长度(2~3 um)和大对流孔两大特征,可在较短保留时间下实现稳健和可扩展的高动态载量。此外,大对流孔还可使结垢倾向更低、更易清洁。
研究人员使用这种新型层析膜纯化了一组含Fc分子,仅在12秒保留时间下就达到了高于30 g/L的典型结合载量,并且在200次循环内仍具有稳健的性能和产品质量!这也证明了该种层析膜可作为蛋白A树脂的可行替代品。
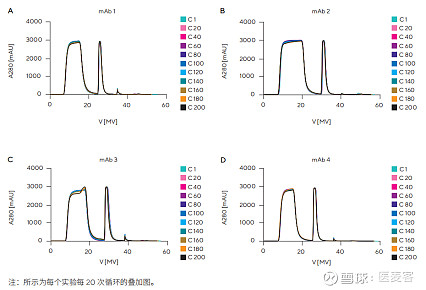
新型层析膜在200次结合和洗脱循环内mAb 1-4(A-D)的紫外吸收曲线叠加图
这一研究中使用的新型层析膜是来自赛多利斯的Sartobind® Rapid A,膜体积(MV)为1.2 mL。
经研究检测,在200次循环应用条件下,Sartobind® Rapid A层析膜的压降变化在0.2bar范围之内,表明该膜未受到严重污染影响。同时,研究人员还分析了产品的关键质量属性(CQA),包括HCP去除率、hcDNA去除率、蛋白A配体浸出和高低分子量种类,结果表明,在200次循环内,HCP和hcDNA去除结果一致。
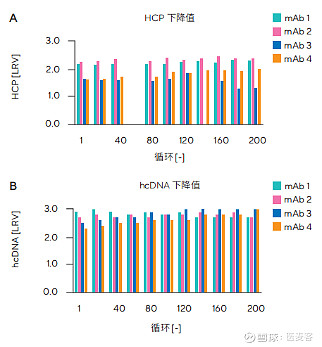
Sartobind® Rapid A在纯化mAb时的HCP和hcDNA去除能力
这项新技术可以说是行业的一大进步,可以消除两大痛点:一是填充床层析存在的失败风险,二是层析柱重复使用存在经济可行性。研究证明,Sartobind® Rapid A的产量高、循环时间短,并且每批使用的单克隆抗体纯化层析材料减少了10倍,可在同一批次中充分重复利用。同时,这一新型层析膜还极大减少了工艺流程中的层析柱操作,可节省大量人力与时间成本,多维度助力抗体生产企业实现降本增效!
想下载完整手册了解详细方法与分析,或直接申领试用,请扫码下方二维码