
2023年3月26日/医麦客新闻 eMedClub News/--2023年3月24日,TIL细胞疗法领军企业IovanceBiotherapeutics宣布,已向FDA完成Lifileucel的生物制品许可申请(BLA)的滚动提交,这意味着全球首款TIL疗法距离上市再进一步。Lifileucel是一款TIL疗法,针对晚期(不可切除或转移性)黑色素瘤。该款细胞疗法的上市之路颇为曲折,其上市申请屡次与FDA未能达成一致,屡次被推迟。

Lifileucel属于过继性免疫疗法的一种,该款疗法旨在利用患者自身的免疫细胞,通过扩增和激活这些细胞,然后将它们重新注入患者体内,以攻击和摧毁肿瘤细胞。
2022年,Iovance披露了Lifileucel治疗晚期黑色素瘤的临床研究(C-144-01)结果。该研究旨在评估lifileucel在晚期(不可切除或转移性)黑色素瘤患者的疗效,这些患者既往接受过抗PD-1/L1治疗。
在注册性队列4(n=87)中,客观缓解率(ORR)为29%,3例完全缓解(CR),22例部分缓解(PR)。中位缓解持续时间(DOR)为10.4个月,中位随访时间为23.5个月。

该研究结果得到了队列2(n=66)研究结果的支持:ORR为35%,5例CR和18例PR。队列2的中位DOR未达到,中位随访时间为36.6个月。队列2和4合并患者(n=153)的ORR为31%,并且在中位研究随访27.6个月时未达到中位DOR。

另外,Lifileucel+Keytruda联合治疗未经免疫治疗的黑色素瘤,ORR为66.7%。
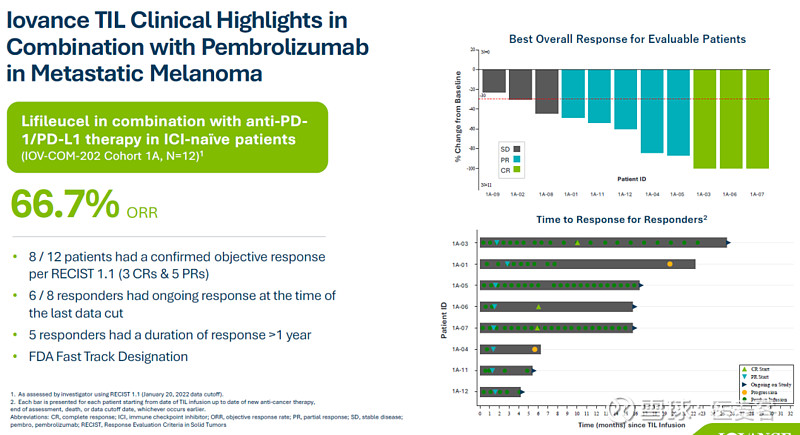
此次lifileucel的BLA提交得到C-144-01临床试验积极临床数据的支持,Iovance正在寻求加速获批上市。Iovance还与FDA就3期TILVANCE-301的注册试验设计达成协议,TILVANCE-301旨在评估lifileucel联合pembrolizumab一线治疗晚期黑色素瘤患者的疗效。该试验旨在支持lifileucel在接受抗PD-1治疗后晚期黑色素瘤患者中的全面批准,并支持注册lifileucel与pembrolizumab联合作为一线治疗晚期黑色素瘤,Iovance正在为TILVANCE-301试验的启动做准备。
Iovance临时总裁兼首席执行官FrederickVogt博士表示:“完成lifileucel的BLA提交是我们为实体瘤患者提供个性化细胞疗法的关键一步。我要感谢参与C-144-01临床试验的患者和医生以及FDA审查团队的承诺和支持,以及我们的内部团队为完成Iovance提交的第一份BLA所做的巨大努力。我们的商业化准备工作仍在进行中,以支持今年晚些时候lifileuce的上市。”
尽管上市之路颇为曲折,Iovance的股价也因此的跌宕起伏,但在不懈努力之下,这款TIL疗法终于完成了BLA滚动提交,也给行业传递了一个积极的信号。
另外,TIL疗法多方位的优势也吸引了全球多家企业的布局,TIL疗法的一项大型随机临床3期试验结果发表于顶级医学期刊《新英格兰医学杂志》。该试验募集了168位转移性黑色素瘤患者,研究结果显示,接受TIL疗法的患者的无进展生存期是对照组的两倍,49%的TIL疗法组患者对治疗产生应答,并有20%接受治疗的病患达成完全缓解。
而在国内,已经有多家企业布局TIL疗法,包括沙砾生物、君赛生物、天科雅、厚无生物、西比曼生物、智瓴生物、劲风生物、原启生物、蓝马医疗、华赛伯曼、循生医学、卡替医疗等,并且已经有多家企业的TIL产品已经获批开展临床。
参考资料:
1.网页链接
声明及版权说明
声明:本文旨在于传递行业发展信息、探究生物医药前沿进展。文章内容仅代表作者观点,并不代表医麦客立场,亦不构成任何价值判断、投资建议或医疗指导,如有需求请咨询专业人士投资或前往正规医院就诊。
版权说明:本文来自医麦客内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台,转载授权请在文章下方留言获取。
——近期热门活动一览——
3月29日,干细胞抗衰老策略与药物临床转化
3月30日,AAV基因疗法从研发到生产全流程解读系列课程第二讲
3月30日,小干扰 RNA 药物开发新型体内自组装递送系统建立与RNA原位共标技术

点点“分享”、“点赞”和“在看”,给我充点儿电吧~