
1
前言
c-MET[亦称为MET酪氨酸蛋白激酶或肝细胞生长因子受体(HGFR)]是一种由MET基因编码的蛋白质。c-MET对胚胎发育、器官生长和伤口愈合至关重要。肝细胞生长因子(HGF)是c-MET受体的配体。
MET通常由上皮来源的细胞表达,但也可在内皮细胞、神经元、肝细胞、造血细胞、黑色素细胞和新生儿心肌细胞中被发现;而HGF则仅来源于间充质细胞。
当HGF与c-MET结合时,它会诱导二聚化,从而导致激活。当这些信号被异常激活时,它会启动和维持肿瘤转化,促进肿瘤细胞增殖和存活,以及肿瘤侵袭和血管生成。肿瘤中c-MET的异常激活与多种癌症的不良预后有关。
事实上,MET的异常表现已在多种恶性肿瘤中被发现,其中包括肾癌、肝癌、胃癌、乳腺癌和脑癌等。正常情况下,只有干细胞和祖细胞能表达MET,从而使这类细胞能进行侵入性生长,以便在胚胎中生成新组织,或者使成人的受损组织再生。
然而,肿瘤干细胞却能拥有应该只有正常干细胞才能表达MET的异常能力,从而促进了肿瘤的生长和转移。c-MET 的过度表达以及其 HGF 配体的共表达所引起的“自分泌”(autocrine)激活,都与肿瘤形成息息相关。
2
MET信号通路与信号转导
基于HGF/c-MET的结构,HGF可以与c-MET结合,因而诱导c-MET同源二聚化和自磷酸化,然后激活GAB1、GRB2、SHC和STAT3。总体而言,c-MET可以参与激活多个下列主要信号通路:
1、RAS通路 — 该通路可以介导由HGF诱导的肿瘤散射和增殖信号,从而导致肿瘤的分支形态发生。HGF可以诱导RAS的持续激活,从而延长MAPK的活性。
2、PI3K通路 — 可直接通过RAS的下游来激活PI3K 通路,或者可通过多功能对接站点来对其直接激活。PI3K通路的激活可以增加肿瘤细胞的活动性,原理为重塑细胞外基质的粘附或细胞骨架重组传感分子(如RAC1和PAK)的募集。被激活的PI3K也可通过AKT途径来加强肿瘤的存活。
3、STAT 通路 — 持续的STAT和MAPK激活是肿瘤分支形态发生的要素,MET也可通过SH2结构域来直接激活STAT3转录因子。
总体而言, MET在癌症发展中的作用主要是通过以下三种机制实现的:
1) 激活关键致癌通路(RAS、PI3K、STAT3、β-catenin等);
2) 促进肿瘤内新血管的生成和生长,以支持其野蛮增长;
3) 促进癌细胞的对外侵袭和转移;癌细胞因MMP蛋白酶的产生而解离,导致癌症向其他身体部位,如骨骼、肝脏、肺部、大脑等部位的远距离扩散。
同时,MET还有其他激活途径。例如,DCP可以通过 MET-JAK1-STAT3信号通路与MET的Y1234/1235结合来诱导细胞增殖,从而导致癌细胞中的c-MET自磷酸化。同时,也可通过磷酸化Y1234/1235来激活c-MET,诱导癌细胞对化疗药物产生耐药。
此外,旁分泌(paracrine)HGF/c-MET亦可通过YAP/HIF-1α途径来促进糖酵解代谢。最后,MET的活性也可以通过c-MET与不同细胞膜受体(如CD44、整合素α6β4、丛蛋白、FAS、IGF-IR、EGFR等)之间的cross-talk来监测。
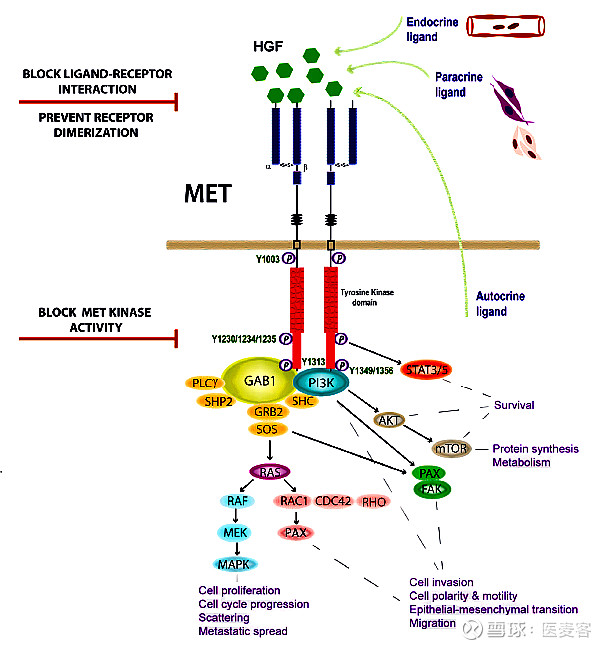
MET信号通路与信号转导说明图 (来源: Feng Y, et al, 2012)
3
c-MET的失调
癌症中的c-MET失调包括点突变、扩增、融合和c-MET蛋白的过度表达等,这些都与多种癌症的不良预后相关。过往的研究表明,MET激活既是一种主要的致癌驱动突变,也是获得性抗靶向药物耐药的驱动因素。总的来说,各种类型的MET失调都能对癌症的产生和恶化造成影响,具体如下:
1、METex14改变(点突变、缺失、插入和复杂突变),可导致MET受体降低降解。从而导致MET信号的激活和肿瘤的产生。
2、MET融合基因是由细胞膜旁调控序列缺乏的METs和不同的N-Terminal partners所组成。有许多基因被发现能与MET融合,例如TPR、TRIM4、ZKSCAN1、PPFIB1、LRRFIP1、EPS15、DCTN1、PTPRZ1、NTRK1、CLIP2、TFG和HLA-DRB1等。
3、MET的扩增是主要致癌因素。在MET扩增过程中,由于MET基因拷贝数增加,MET/CEP7比率亦会随之增加。
4、毁损的MET受体降解亦可以是配体异常MET信号的其中一种机制。
5、过度表达的MET/HGF可以通过上调分泌信号来诱导肿瘤细胞转化。虽然在众多癌症中,MET蛋白的过度表达与不良预后相关,但不幸的是,用其作为抗癌药物疗效的指标并不可靠。有研究人员甚至认为, 多个在3期临床中失败的c-MET抑制药物(如Onartuzumab, Tivantinib 和 Cabozantinib等)就是因为无法正确筛选合适的患者 。
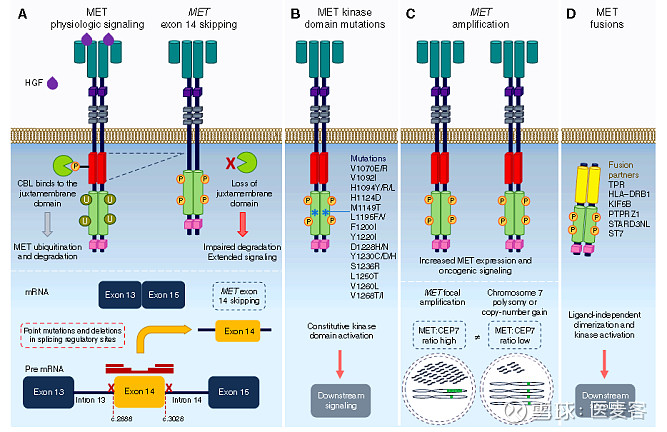
在癌症中各种c-MET失调原因的说明图 (来源: Recondo G, et al, 2020)
4
MET在TKI耐药中的机理作用
耐药机制可能是长期药物暴露后癌细胞选择压力的结果。就c-MET来说,由于MET扩增亚克隆细胞群的存在以及旁分泌和自分泌HGF等的刺激,耐药性可随着时间的推移而出现。这将反过来导致c-MET治疗药物的耐药肿瘤亚克隆的增加。
例如在许多癌症中,尤其是非小细胞肺癌,通常可以观察到由于MET扩增而导致的EGFR-TKIs的耐药性。第一代和第二代EGFR TKIs的耐药性高达50-60%,第三代EGFR TKIs的耐药性也有15-20%。有两个已发表的主要研究想必能帮助大家了解第三代EGFR-TKI奥西替尼(Osimertinib)获得耐药性的机制。
这两个名为FLAURA和AURA2的研究分别为患者提供了一线和二线奥西替尼的治疗。在疾病进展或停药时对患者血浆样本进行二代基因组测序。结果表明MET扩增为最常见的获得性耐药机制;一线治疗患者中有15%的 MET扩增,而二线治疗患者则有19%的 MET扩增。此外,在肿瘤和间质细胞中HGF水平的增加也可导致MET途径的失调,从而导致EGFR-TKIs的耐药。
幸运的是,多个临床前研究表明,抗c-MET的药物可以逆转对EGFR-TKI的耐药性并可恢复其敏感性。事实上,EGF和HGF对细胞增殖的协同作用亦已在其它的临床前研究中得到证实。这为联合靶向药物治疗或用双抗来治疗患者 (特别是EGFR-TKIs耐药的病人)提供了依据。
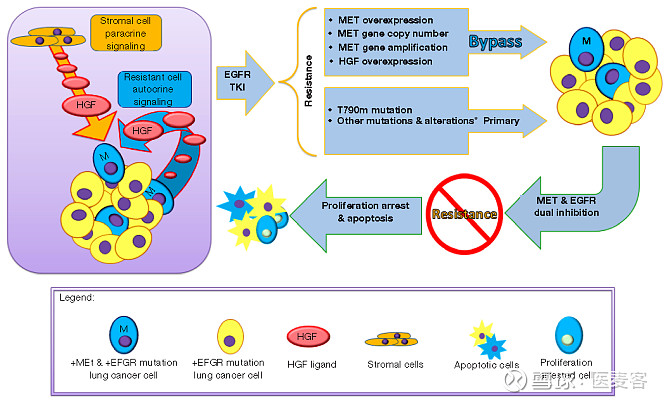
MET 在 EGFR-TKI耐药中的可能机理说明图 (来源:Ko B, et al, 2017)
5
抑制HGF/c-MET轴的抗体药物开发
一般来说,只有存在MET基因改变的患者在接受抗c-MET药物后才会有客观反应;而对于存在野生型MET的患者而言,靶向HGF/MET信号通路通常对癌细胞生长影响不大。
据近期报道,抑制c-MET的药物对有高水平MET扩增或METex14跳跃突变的患者相当有效。目前已有多种抗c-MET药物正在研发中,本文的重点将主要集中在抗体和生物制剂上。
a.Onartuzumab (罗氏/基因泰克公司)
Onartuzumab是一款有趣的全人源化单臂/单价的特殊c-MET单抗。它可阻断HGF-α链与c-MET配体的结合。Onartuzumab使用旋钮入孔(knobs-into-holes)技术,优先组装重链和Fc链。
这个特殊设计的原因在于基因泰克的科学家们担心,以二价抗体为结构的药物说不定会模拟HGF所激动的二聚作用。这样不单不能阻止MET的活动,反而会造成MET通路的激活。为了解决这一问题,他们开发了一个特殊的单臂/单价的c-MET单抗,确保该药仅以一对一的方式与受体结合,从而阻断MET通路的活动。
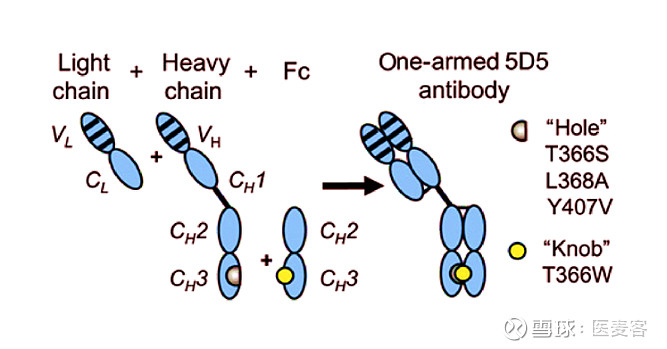
Onartuzumab 单臂/单价c-MET单抗设计说明图 (来源:Merchant, et al, 2013)
基因泰克公司一共对Onartuzumab进行了18个临床试验,其中包括乳腺癌、结直肠癌和胶质母细胞瘤的二期临床和非小细胞肺癌和胃癌的3期临床等。然而,大多数临床试验的结果都令人失望。2015年后该公司再没有启动新的临床计划,Onartuzumab的研发现已陷入停滞。
例如,在一项以治疗非小细胞肺癌患者的随机研究(GO27820)中, 评估Onartuzumab联合一线铂类化疗与单独化疗的疗效比对时,主要研究终点中位PFS在两组中并无分别,都是只有4.9个月。而对于MET表达较高的患者而言, Onartuzumab组的中位PFS为5.0个月,而对照组则为5.2个月,结果也无分别。
另一个针对非小细胞肺癌患者的II期试验(GO27281)中, Onartuzumab联合铂类/培美曲塞/贝伐单抗治疗再次没有达到其主要研究终点,其中位PFS为5.0个月,而对照组则为6.8个月。在MET表达较高的患者中,Onartuzumab的中位PFS为4.8个月,而对照组为6.9个月。
Onartuzumab联合EGFR-TKI的临床数据也同样不尽如人意。在一项2期临床试验中,120名已被其它药物治疗过的非小细胞肺癌患者被随机分为两组,一组接受Onartuzumab联合Erlotinib治疗,另一组则接受Erlotinib单药治疗。结果表明,与对照组相比,Onartuzumab联合组在总体人群中的PFS和OS均没有改善。然而,在MET阳性的亚组患者中,治疗组的PFS和OS 则有所延长。
因此,其后基因泰克公司开展了一个499例MET阳性的非小细胞肺癌患者的3期随机临床试验。其中一组患者接受Onartuzumab联合Erlotinib治疗,另一组患者仅接受Erlotinib单药治疗。结果显示,Onartuzumab联合组的患者与对照组相比表现不佳:ORR(8.4%对9.6%),PFS(2.7 vs 2.6个月)和OS(6.8 vs 9.1个月)都没有改善。Onartuzumab的研发再遭滑铁卢,基因泰克公司因而放弃后续研发。
当然,总会有很多事后孔明来对这个大家寄予厚望的3期临床为何失败来作盖棺定论。综合各方观点如下:
首先,存在生物标志物如何定义患者为MET阳性或阴性的问题。不幸的是,在该研究中用以定义MET 阴/阳性的IHC assay抗体, 与Onartuzumab的关联性甚差;因此,其所选定的患者未必能从Onartuzumab的治疗中受益。
其次,MET阴/阳性的决定是由患者最初诊断时所进行的活检组织中所作出,但真正入组的病人则是已经接受过其它一线或二线药物治疗的患者。在其后的治疗过程中,患者的MET状态可能已经改变。
最后,为这3期临床铺垫的原本2期临床数据其实并不稳妥。Onartuzumab联合用药组中存有EGFR 变异患者有20%,而Erlotinib单药组则只有7%。这个差异对疗效的影响难以评估。当然,之后其它c-MET药物的临床数据亦不出色,表明仅靠单药抑制MET通路本身可能不是一种最为有效的治疗策略。
b.Emibetuzumab (礼来公司)
Emibetuzumab是一种人源化的c-MET IgG4单抗,可阻断HGF和c-MET的结合,导致c-MET的内化和降解,并防止信号传递。礼来已经为该抗体进行了几次临床试验,其中大多数是针对非小细胞肺癌的。遗憾的是,由于没有强烈的疗效信号,2014年后礼来已没有再启动新的临床研究,该药物的开发似乎已被放弃。
例如,在一项2期临床试验上,礼来尝试评估Emibetuzumab + Erlotinib比Emibetuzumab单药对MET阳性的非小细胞肺癌患者的疗效。该试验共入组111名患者,其中28名患者接受Emibetuzumab单药治疗,83名患者接受Emibetuzumab联合Erlotinib治疗。
结果显示,在MET有表达 (≥10%细胞具有IHC≥2+) 的患者中,联合治疗组的ORR为3.0%,而单药治疗则为4.3%。在MET高表达 (≥60%细胞具有IHC≥2+) 的患者中, 联合治疗组的PFS(3.3个月比1.6个月)和OS(9.2个月比8.2个月)虽然略高,但ORR(3.8% 比4.8%)则低于单药;当然,这种微小差距也很难在统计上有意义。
此外,在一个反向设计的2期临床上,礼来评估了Emibetuzumab + Erlotinib比Erlotinib在治疗具有EGFR突变的晚期非小细胞肺癌患者中的疗效。该临床共入组141名患者,其中一半接受联合治疗,另一半接受Erlotinib单药。
结果显示,在总体人群中,联合组在主要研究终点PFS上与单药组(9.5个月vs 9.3个月)并无明显差异,临床算是失败。其后,在一个探索性的分析上,MET高表达(MET IHC3+)的患者亚组在联合用药上好像比单药延长了PFS(20.7 vs 5.4个月);不过这类事后分析一般样本量不高,所以甚难确定其真正意义。
总体而言,由于没有强烈的疗效信号,礼来选择不再进一步开发该药。
c.Rilotumumab (安进公司)
Rilotumumab是一种完全人源化的IgG2单体,可与HGF-β链绑定从而抑制HGF与c-MET的结合。安进已经为该药进行了17个临床试验。其中,在肾细胞癌、恶性胶质瘤、结直肠癌、间皮瘤、卵巢癌和前列腺癌中进行过2期临床,而在非小细胞肺癌和胃癌中进行过3期临床。
然而,显示出的疗效数据都非常一般。例如,在一项1/2期临床试验上评估了Rilotumumab联合Erlotinib治疗非小细胞肺癌患者的有效性上,在所有接受治疗的45位患者中,ORR为8.8%, PFS中位数为2.6个月,mOS为6.6个月。此外,对于33位野生型EGFR患者亚群而言,中位PFS为2.6个月,mOS为7.0个月,效果也没有多大差别。
基于这些令人失望的结果,安进公司在2014年后再没有对其启动新的临床研究。
d.Ficlatuzumab (Aveo公司)
Ficlatuzumab是一种针对HGF的高亲和力人源化IgG1单抗,通过阻断HGF/cMET结合来抑制HGF诱导的c-MET信号通路。
一项2期随机临床试验评估了Ficlatuzumab + Gefitinib联合治疗与Gefitinib单药在非小细胞肺癌患者中疗效的比较。虽然在总体人群中,与Gefitinib单药相比,联合治疗并未明显改善ORR(40% 对 38%)、PFS(5.6 对 4.7 个月)和OS(24.7 对 21.8 个月);但是,在有着EGFR突变和低c-MET表达的患者亚群中,接受联合治疗的患者与单药对比,ORR差异为41%比22%,中位PFS对比为11个月比5.5个月,两者均有相当改善。
总体而言,Ficlatuzumab联合Gefitinib在具有EGFR突变和c-MET低表达的小细胞肺癌患者中具有不错的疗效,值得进一步探索。
Aveo公司对该药共进行了约10项临床试验,其中一项为针对胰腺癌的1期临床研究,以及针对非小细胞肺癌、头颈癌和急性髓系白血病(AML)的多个2期临床研究。目前,该抗体是所有同类药物在临床开发阶段中最为积极的药物。
以下是正在研发的主要cMET/HGF抗体的总结,供读者参考。多个1期临床新药目前并无公开数据,所以无法评论。
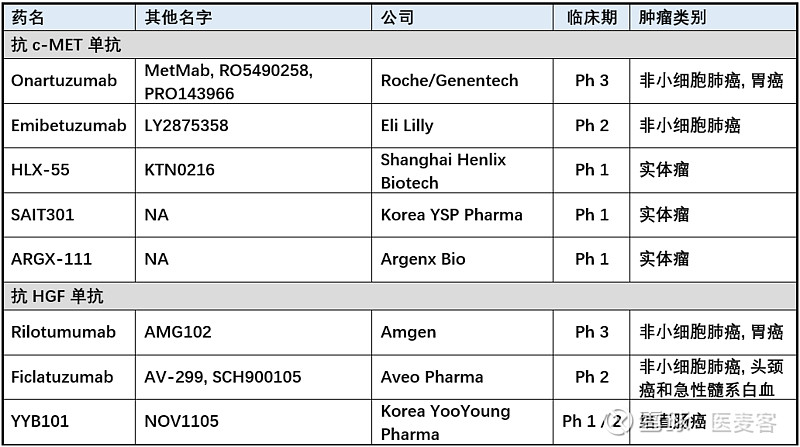
6
小分子c-MET抑制剂的研发
目前,有几款小分子c-MET抑制剂已经上市或正在研发之中。不过,Tivantinib 和Cabozantinib都曾有在3期临床失败的记录 。这类药物最成功之处似乎展现在具有METex14变异的非小细胞肺癌患者亚群中,例如FDA近期批准了Tepotinib和Capmatinib的上市使用就是很好的例子。由于篇幅所限,加上本文重点为抗体与生物制剂的评论,在此将不再对小分子药物作进一步阐述。
然而,为完整起见,下面提供一份主要c-MET小分子药物汇总表,供读者参考:
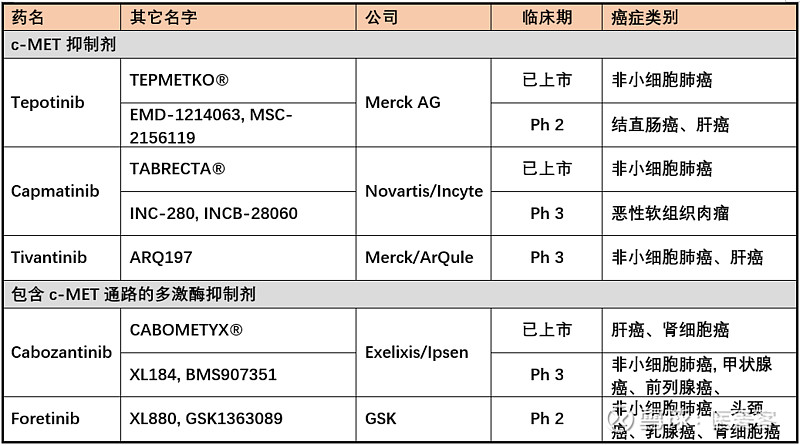
7
免疫疗法
在如今IO疗法当红之际,我们当然不可错过免疫疗法在MET变异患者中的可能角色。
一项回顾性的研究分析了在非小细胞肺癌患者中,免疫疗法对不同致癌基因病人的疗效;当中包括了36例MET变异的患者(13例MET扩增,23例METex14跳跃突变),他们都在不同阶段的治疗过程中接受过抗PD1或PDL1的抗体药物。在这些亚组分析中,患者们的ORR为16%,中位PFS为3.4个月,OS为18.4个月。疗效看来一般,不过OS数据还算不错。
另一项回顾性研究涵盖了147名患者,以评估METex14肺癌患者的PD-L1表达、肿瘤突变负荷(TMB)和免疫治疗在这些患者中的临床活性。其中,PD-L1阳性(PD-L1≥ 1%)的发生率为63%,而在具有METex14变异的患者中,其TMB水平则相对较低。在24名接受过抗PD1/PDL1治疗的患者中,ORR为17%,平均OS为18.2个月。然而,21名可评估患者的PFS中位数仅为1.9个月。与之前另一回顾分析类似,PFS相对较差,但OS还算可以。
总体而言,这两个回顾性研究显示,IO单药在治疗具有MET改变的非小细胞肺癌患者的临床表现并不特别出色。因此, IO与其他药物联用可能比单独使用抗PD1/PDL1的治疗效果更好。期待未来能有更多的临床研究可以提供数据以便参考。
8
未来可能发展的研发方向
虽然近年来已有多个抗c-MET药物的3期临床以失败告终,但具有MET基因变异的癌症患者亚组,尤其是MET扩增或METex14跳跃突变,似乎对MET抑制剂反应不错。此外,寻找合适的生物标记物以便更好地选择患者,或者使用联合治疗或双抗,都是未来发展的一个可行方向。对于后者,一个很好的范例即为强生公司的Amivantamab,一款EGFR x cMET双特异性抗体。(编辑按:本文著者Mark Chiu博士曾领导研发Amivantamab)
Amivantamab双抗可通过结合EGFR和MET而阻断配体结合,促进受体降解,并在具有EGFR突变(EGFRm)的非小细胞肺癌患者中触发ADCC。一项1期临床试验评估了Amivantamab在治疗具有EGFR突变的晚期非小细胞肺癌患者中的有效性,其中期数据在2019年的ASCO大会上公布。
该试验一共入组116例患者,其中97%携带EGFR突变。在88名可评估的患者中,28%获得PR。此外,在47名对第三代EGFR-TKI耐药的患者中,21%也获得PR (其中4名为具有C797S突变,1名为MET扩增,5名为没有可识别的EGFR/MET基因改变)。在20例EGFR 20ins患者中,30%也达到PR。
以上数据最令人印象深刻的是,该药对第三代EGFR-TKI(包括C797S、MET扩增和外显子20ins)耐药的患者都有临床疗效。总体而言,Amivantamab在携带EGFR突变或对第三代EGFR-TKI耐药的非小细胞肺癌患者中都具有不错的疗效。因为数据积极,以致FDA在2021年5月仅凭这个1期临床数据就批准了该药上市。
随着Amivantamab的成功,其他EGFR x cMET双抗也陆续在开发中。其中包括:LY3164530(礼来)、MCLA-129(Merus)、CKD-702(韩国CKD制药)和EMB01(岸迈生物),它们目前都处于1期或1/2期的临床开发阶段。
就国内而言,除了岸迈生物,贝达药业也从Merus公司获得了MCLA-129在中国的开发和销售权益,并在近日开展了国内的1/2期临床试验。
至于临床前期药物,德国默克公司和韩国三星公司也拥有类似的临床前管线。而三星拥有的更是一 款EGFR x cMET x HER3三特异抗体。我们拭目以待,看看这些药物在未来能否跑出与Amivantamab相当甚至更好的疗效。
此外,艾伯维公司也有一款c-MET ADC药物Telisotuzumab Vedotin(ABBV-399)正处于临床阶段。在一项1期临床试验中,16名MET阳性的非小细胞肺癌患者采用了这款ADC药物的治疗。结果显示,PR为18.8%,中位PFS为5.7个月,中位应答持续时间为4.8个月。安全性也算不错。艾伯维目前已为该药进行了6个临床试验,其中大多为非小细胞肺癌。在2021年12月,艾伯维更打算用该ADC药物与多西紫杉醇进行一个600例非小细胞肺癌病人的头对头3期临床试验。
期望未来会有更多基于c-MET的ADC药物进入临床,造福病人。
9
TAVOTEK在c-MET生物制剂研发的方向
随着 c-MET/HGF 通路上有着更多的药物上市,拓创生物目前也有多个研发计划。 公司瞄准c-MET驱动肿瘤的多个发展方向。 由于通过配体阻断c-MET 并不特别有效,因此研判需要额外的通路机制作为协助治疗策略。 其中一个方向是瞄准与其关联家族受体相关的c-MET驱动肿瘤。在这个方向上,对这些肿瘤组织的杀伤将需要识别不同表达水平的c-MET和在肿瘤微环境中的其他受体。
此外,这些新药分子亦可利用免疫细胞激活和增殖来靶向并杀伤肿瘤组织。拓创生物还非常热衷于开发其他给药模式,例如通过将 ADC、ITC 甚至 mRNA 的有效载荷来更具体地输送药物到肿瘤微环境中来提高疗效。最后,使用c-MET作为肿瘤特异性标记,将肿瘤组织定位与其他肿瘤抗原联系起来,期望以这种创新的构思在未来能带来更多更有效的新药分子。
10
总结
目前已有很好的证据表明HGF/c-MET通路在多个肿瘤发展过程中所起的重要作用。HGF/c-MET通路在癌症发生中的基因组特征亦已充分得到证实。近年亦有多个抗HGF/c-MET药物上市或在临床试验中。
然而,尽管HGF/c-MET靶向治疗在多种癌症的临床前数据表现非常积极,但仍有多个令人失望的3期临床试验降低了医药界对靶向c-MET通路的期待。
不同癌症中c-MET激活的各种机制,包括HGF/c-MET过度表达、MET基因改变(如突变、扩增、易位或转录障碍)和受损的MET降解,都可以在未来提供一系列良好的潜在生物标记物,从而更好地选择患者亚群。
此外,探索联合用药治疗,包括IO或其它关联通路药物的共用,都是可行之道。最后,多靶点的双特异或多特异抗体,甚或ADC或其它的有效载荷 (Payload),都可能在未来对治疗c-MET相关肿瘤上打开一条新路。我们将拭目以待,未来可期。
参考资料:
Bylicki O, Paleiron N, Assié JB, Chouaïd C. Targeting the MET-Signaling Pathway in Non-Small-Cell Lung Cancer: Evidence to Date. Onco Targets Ther. 2020; 13:5691-5706. (doi: 10.2147/OTT.S219959)
Feng Y, Thiagarajan PS, Ma PC. MET signaling: novel targeted inhibition and its clinical development in lung cancer. J Thorac Oncol. 2012; 7(2):459-67. (doi: 10.1097/JTO.0b013e3182417e44)
Ko B, He T, Gadgeel S, Halmos B. MET/HGF pathway activation as a paradigm of resistance to targeted therapies. Ann Transl Med. 2017; 5(1):4. (doi: 10.21037/atm.2016.12.09)
Mazieres J, Drilon A, Lusque A, et al. Immune checkpoint inhibitors for patients with advanced lung cancer and oncogenic driver alterations: results from the IMMUNOTARGET registry. Ann Oncol. 2019; 30:1321–1328. (doi:10.1093/annonc/mdz167)
Merchant M, Ma X, Maun HR, et al. Monovalent antibody design and mechanism of action of onartuzumab, a MET antagonist with anti-tumor activity as a therapeutic agent. Proc Natl Acad Sci U S A. 2013; 110(32):E2987-96. (doi: 10.1073/pnas.1302725110).
Moosavi F, Giovannetti E, Peters GJ, Firuzi O. Combination of HGF/MET-targeting agents and other therapeutic strategies in cancer. Crit Rev Oncol Hematol. 2021; 160:103234. (doi: 10.1016/j.critrevonc.2021.103234)
Neijssen J, Cardoso RMF, Chevalier KM, Wiegman L, Valerius T, Anderson GM, Moores SL, Schuurman J, Parren PWHI, Strohl WR, Chiu ML. Discovery of amivantamab (JNJ-61186372), a bispecific antibody targeting EGFR and MET. J Biol Chem. 2021; 296:100641. (doi: 10.1016/j.jbc.2021.100641)
Park KC, Richardson DR. The c-MET oncoprotein: Function, mechanisms of degradation and its targeting by novel anti-cancer agents. Biochim Biophys Acta Gen Subj. 2020; 1864(10):129650. (doi: 10.1016/j.bbagen.2020.129650)
Recondo G, Che J, Jänne PA, Awad MM. Targeting MET Dysregulation in Cancer. Cancer Discov. 2020; 10(7):922-934. (doi: 10.1158/2159-8290.CD-19-1446)
Sabari JK, Leonardi GC, Shu CA, et al. PD-L1 expression, tumor mutational burden, and response to immunotherapy in patients with MET exon 14 altered lung cancers. Ann Oncol. 2018; 29:2085–2091. (doi:10.1093/annonc/mdy334)
Syed YY. Amivantamab: First Approval. Drugs. 2021; 81(11):1349-1353. (doi: 10.1007/s40265-021-01561-7)
Zambelli A, Biamonti G, Amato A. HGF/c-MET Signalling in the Tumor Microenvironment. Adv Exp Med Biol. 2021; 1270:31-44. (doi:10.1007/978-3-030-47189-7_2)