

本文由医麦客原创,欢迎分享,转载须授权
2020年8月27日/医麦客新闻 eMedClub News/--日前,Sutro Biopharma宣布,根据该公司与德国默克的医疗保健部门达成的合作和许可协议,Sutro已经实现了临床供应里程碑,Sutro公司有权获得来自德国默克的付款。
该里程碑付款基于2014年双方达成的合作协议,Sutro公司将提供候选产品 M1231的GMP临床试验产品,实现 M1231 的1期临床试验测试,从而触发了该里程碑付款。值得一提的是,M1231是一款双特异性抗体偶联物(bispecific antibody drug conjugate )。


双特异性抗体偶联物
M1231是一款同时靶向MUC1-EGFR的双特异性抗体偶联物(ADC),用于治疗实体肿瘤。M1231基于Sutro公司的XpressCF®和XpressCF+™技术平台开发,同时依赖于德国默克的strand-exchange工程结构域(SEED)平台生产的双特异性抗样分子,此外M1231还利用了Sutro公司专有的连接子。
Sutro首席科学官Trevor Hallam博士说:“M1231是第一个同时靶向MUC1和EGFR的双特异性ADC,同时结合我们XpressCF+™技术以及德国默克SEED平台的力量,Sutro开发了独特的下一代ADC药物,因其能够选择性靶向两种不同肿瘤抗原的机制,有潜力扩大治疗范围。”
根据早先达成的协议,Sutro公司将生产M1231以供应早期临床试验,德国默克将负责该候选产品的临床开发和商业化,以及该药物的灌装和完成。这意味着,该产品下一步就是向临床试验迈步。
进一步的财务细节暂时未予披露。

专注于蛋白偶联物
Sutro Biopharma,Inc.位于南旧金山,是一家临床阶段的药物发现,开发和制造公司。Sutro使用精确的蛋白质工程和合理的设计,正在推进下一代肿瘤治疗学。
Sutro公司利用专有和集成的无细胞蛋白质合成平台XpressCF®和特定位置的偶联平台XpressCF +™开发了Sutro的前两个内部研发管线STRO-001和STRO-002。
▲ XpressCF®技术平台(图片来源:sutrobio)
Sutro公司的XpressCF®平台是一种无细胞(cell-free)蛋白生产技术,不需要反复调整新的细胞系,避免了传统蛋白生产的一些局限性,同时能够在8-10小时内以g/L的产量生产单一蛋白质。XpressCF®平台可以提供定制的治疗性蛋白质的设计、制造和开发,同时还支持非天然氨基酸序列的插入。
XpressCF+™允许定制治疗性蛋白质,包括20种天然氨基酸,以及非天然氨基酸合成的蛋白质。使用XpressCF+™开发的含有非天然氨基酸的蛋白质可以在特定位点与一种或多种化学物质偶联,使蛋白-药物偶联同源。
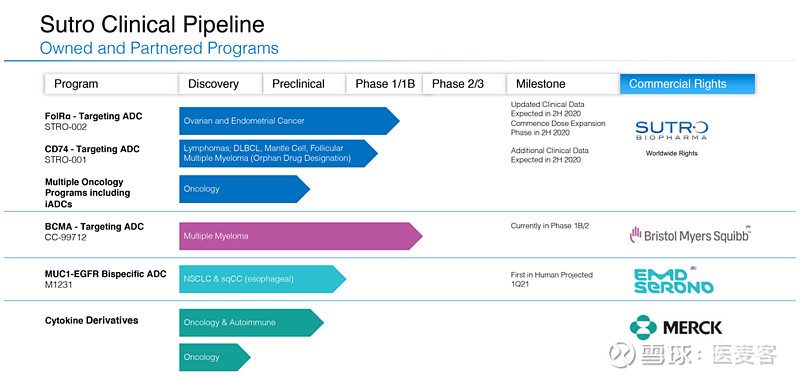
▲ Sutro公司的研发管线(图片来源:sutrobio)
STRO-001是靶向CD74的ADC,目前正在对包括多发性骨髓瘤和非霍奇金淋巴瘤在内的晚期B细胞恶性肿瘤患者进行1期临床试验中进行研究。STRO-001于2018年10月被FDA授予多发性骨髓瘤孤儿药称号。
STRO-002是靶向叶酸受体α(FolRα)的ADC,目前正在进行针对卵巢癌和子宫内膜癌患者的1期临床试验。
CC-99712是一款靶向BCMA的ADC,由Sutro公司与BMS合作开发,正在招募多发性骨髓瘤患者参加1期临床试验。
迄今为止,Sutro公司已经设计了多款肿瘤免疫疗法、ADC、疫苗记忆双特异性抗体等,选择的靶点都是经过临床验证的、但治疗效果欠佳的靶点。除了开发内部管线以外,Sutro还与合作伙伴(例如德国默克、BMS等)共同开发更优的肿瘤药物,以更有效的杀伤肿瘤细胞,同时不损害健康细胞。
目前看来,该公司的研发重点集中在ADC药物上,事实上,从2019年以来,ADC的发展迅猛,2019年FDA批准3款,2020年至今FDA批准2款。

ADC药物快速发展
目前,FDA一共批准了10款ADC上市。此外,还有数十家制药公司正在进行ADC疗法的临床试验,其中包括了阿斯利康、葛兰素史克(GSK)、阿斯特拉斯制药(Astellas Pharma)、西雅图遗传学公司(Seattle Genetics)等制药巨头,其中罗氏和第一三共公司都在针对不同的癌症开发不同的ADC药物。
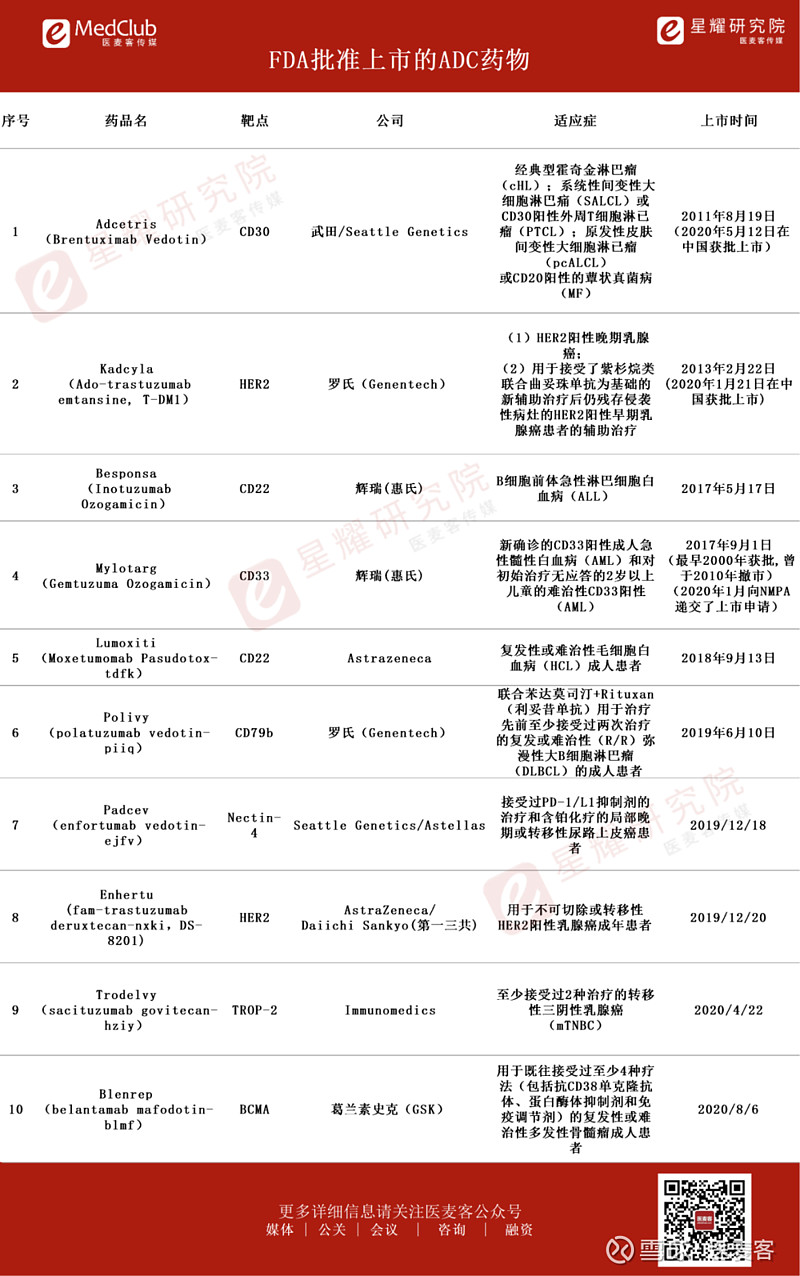
相较于国外热火朝天的市场,国内ADC研发领域也不落下风,虽无ADC药物获批上市。日前,荣昌生物已经向中国药监局提交旗下ADC候选产品的上市申请,并被纳入优先审评审批程序。
截至目前,国内已经申报约数十款ADC新药,但靶点相对集中,大部分靶向HER2,其余分别分布在EGFR、Trop2、c-MET、CD20、CD30。就当前各药企的ADC获批进度来看,处于临床I期的居多,百奥泰的BAT8001处于临床III期,而其他药企大多临床申报中或已获批临床。
参考资料:
1.网页链接
2.网页链接

医麦客近期热门报道
★CRISPR巨头公司Editas的候选疗法获得FDA授予罕见儿科疾病称号,镰状细胞病基因疗法赛道已开丨医麦猛爆料
★百奥泰递交港股上市申请,又一家“A+H”上市公司丨医麦猛爆料

 点击“阅读原文”,免费看直播!
点击“阅读原文”,免费看直播!