1.截至2022年12月31 日止年度的產品收入達人民幣4,139.1百萬元,較截至2021年12月31日止 年度的人民幣4,001.1百萬元增長3.4%。
营收只能算持平吧,看之前的数据,pd1大概在20亿左右,意味着其他药品的营收已经和pd1持平
2.毛利率下降很多。截至2022年12月31日止年度,產品銷售的毛利率為78.9%,較截至2021年 12月31日止年度的88.7%下降9.8%。2022年,主要產品的生產效率進一步 改善,而毛利率的變化主要是由於新合作產品入賬的毛利率較低,毛利率 相對較低的生物類似藥產品貢獻比例增加,以及達伯舒®(信迪利單抗注射 液)的單價下降所致。
说的没毛病,营收有一大部分是生物类似药提供,换句话说,营收的质量在下降
3.研究與開發(「研發」)開支由截至2021年12月31日止年度的人民幣2,118.7 百萬元增加人民幣546.0百萬元至截至2022年12月31日止年度的人民幣 2,664.7百萬元。
4.销售推广费率并没有下降,当然今年的营收也没有增加,下半年有所下降,需要继续观察。研究與開發(「研發」)開支由截至2021年12月31日止年度的人民幣2,118.7 百萬元增加人民幣546.0百萬元至截至2022年12月31日止年度的人民幣 2,664.7百萬元。
5.商業化產品組合由六款產品擴充至八款產品,礼来引进的两个,算凑数的吧。RET不知道能否卖的好?
nsclc感觉意思不大啊。RET基因在非小细胞肺癌中是一种罕见靶点。RET融合变异阳性在中国人中的发生率约1.6%,但由于中国肺癌患者的基数较大,每年新发RET阳性肺癌患者可达1.1万人。
甲状腺应该有看头一些。RET基因变异被认为是甲状腺癌等多个瘤种形成发展的重要因素。研究显示,几乎所有遗传性MTC和约50%的散发性MTC均存在RET突变,约10%-20%的甲状腺乳头状癌(PTC)患者存在RET融合,并有19.4%的RAIR PTC存在RET/PTC重排。
6.三 項 新 藥 上 市 申 請(「 N D A 」实际就两个pcsk9、bcma-cart,BCR-ABL之前已经有条件获批。
7.四款候選產品关键临床(外加一款:IBI-112在中國中重度斑塊型銀屑病患者的3期臨床研究(CLEAR)於2023年2 月啟動)
IBI-362两个三期、KRASG12C、ROS1/TRK、
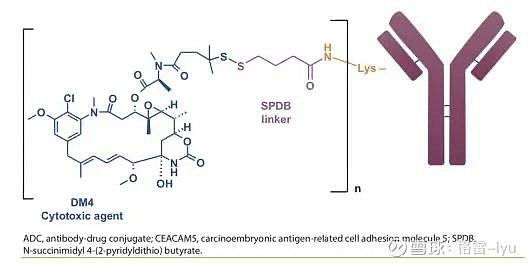
CECAM5-ADC,赛诺菲(Sanofi)引进ImmunoGen的另一款新型抗体偶联药(ADC),是目前针对CEACAM5靶点研究进展最快的同类首创药物。由人源化单克隆抗体(SAR408377)和DM4通过ImmunoGen开发的可切割链接子(SPDB)偶联而成。
III期CARMEN-LC03试验(NCT04154956)招募大约450例非小细胞肺癌成年患者,ECOG评分为1或0,在接受铂类化疗和免疫检查点抑制剂(ICI)治疗后,疾病出现了进展。此外,患者必须在至少50%的肿瘤细胞中表现出CEACAM5的表达,强度至少为2+,才能被纳入研究。参加开放标签试验的患者将被随机分配接受SAR408701单药治疗或标准护理治疗多西紫杉醇。治疗的剂量分别为每2周100毫克/平方米静脉注射或每3周75毫克/平方米静脉注射。该研究的共同主要终点是无进展生存期(PFS)和生存期(OS)。次要终点包括客观缓解率(ORR)、健康相关的生活质量、安全性和中位持续缓解时间(DOR)。该试验预计完成日期为2024年8月。
前期的数据
截至2020年1月,在该试验的非鳞状非小细胞肺癌队列中,有92例患者以最大耐受剂量(MTD,每2周一次,每次100mg /m^2,IV)接受治疗。其中28例为CEACAM5中度表达者【1%-50%的肿瘤细胞上免疫组化(IHC)≥2+】,64例为高表达者(IHC≥2+在≥50%的肿瘤细胞上)。先前治疗线的中位数为3。
CEACAM5中度表达者的总客观缓解率(ORR)为7.1%(95%,置信区间:1.98%-22.65%),所有患者均部分缓解(PR),53.6%的患者疾病稳定(SD),35.7%的患者病情进展(PD);疾病控制率(DCR)为60.7%。
CEACAM5高表达者的ORR为20.3%(95%,置信区间:12.27%-31.71%),所有患者都出现PR,SD为43.8%,PD为32.8%;DCR为64.1%。
在整个非鳞状非小细胞肺癌队列中,最常见的治疗相关不良反应(TEAEs)包括:气喘(38.0%)、角膜病/角膜炎(38.0%)、周围神经病变(26.1%)、呼吸困难(23.9%)和腹泻(22.8%)。
8.其他
2023年年底在中國就Tigulixostat申請IND開展臨床,並啟動3期 臨床研究。
2023年年底,我們預期讀出高濃度IBI-302治療nAMD患者的2期臨床試驗 數據
於2023年下半年,我們計劃讀出IBI-311治療TAO患者的2期臨床研究數據, 並啟動IBI-311治療TAO患者的3期研究。
总体感觉,IL2感觉有点悬啊,cd47也是。唉,自己搞的靶点目前还没看花结果的。