一片药能在人体内起效的关键的不仅仅是化合物,化合物最终在体内的溶出度如何,制剂工艺影响非常大!这也是国家在仿制药申请过程中,一致性评价需要严查人体BE- PK试验的原因。药成分相同(化合物CAS号一样,核磁图谱一样),但是服用到人体内的溶出状况可能千差万别。
观点:合成目标化合物不等于能做API生意;利托那韦原料药API工艺难点在控制晶型;需重视制剂厂商的稀缺性
药学学科下,二级学科再分 药物化学、药物分析、药物制剂、药理学、药代动力学、临床药理学。每个专业解决制药的不同流程。这一篇说一说晶型。虽然我研究药物化学,但趁机学习一下药物分析和药物制剂的内容。
一、合成目标化合物不等于能做API生意
有些朋友可能对中间体、化合物、原料药以及制剂的概念混杂。
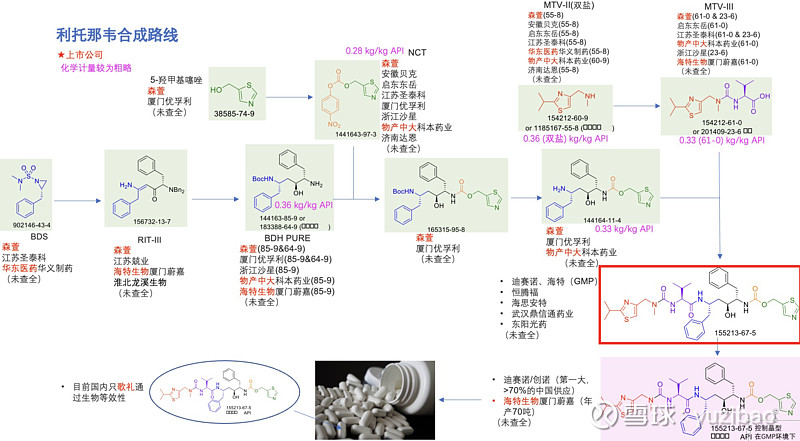
以利托那韦为例,下图绿色的都算是中间体,最终得到红色圈圈利托那韦化合物,对应CAS号 155213-67-5,不过在这一步骤,如果没有控制晶型,就只能算化工产品,化工产品是卖不上价格,竞争者无数。控制晶型且在GMP环境下生产,才是原料药API,去药监局备案,才能稳定地卖上价格。
下面的图,某厂商合成了红圈框,顶多只能说符合目标化合物,但是成不了原料药API。森萱有所有中间体片段,有其壁垒性。如果后期能解决晶型控制的问题,生产API,价值进一步上去了。
目前供应利托那韦API的主要是迪赛诺,控制晶型并通过了GMP审计(不是仅仅在GMP环境下生产,是需通过审计)。
赛诺的晶型控制可能很强,网上他的专利很多都和晶型有关。
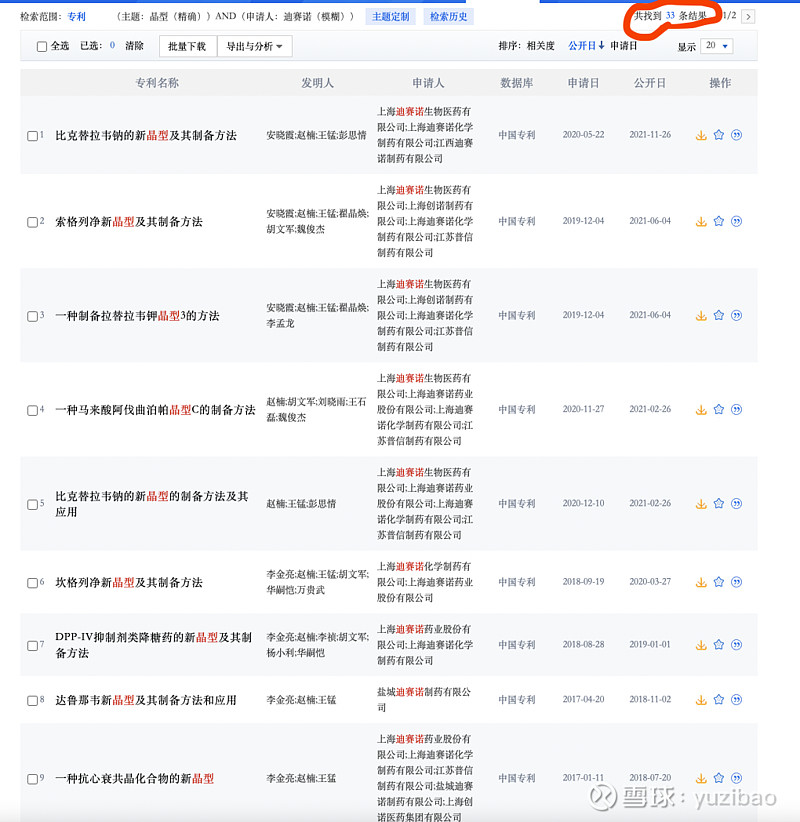
二、利托那韦原料药API工艺难点在控制晶型
控制晶型是为了口服生物利用度一致性。通俗点说,晶型是化合物原子堆积排列的方式。
对于仿制药物而言,晶型技术往往是原研企业的核心技术机密,是原研产品的内控指标。要实现有效仿制必须攻克晶型专利技术壁垒,可以换个晶型,你只有有本事做到BE等效/通过一致性评价,NMPA/FDA不会管你,如果不评价,就会出现仿制药质量疗效不如原研药的现象。
所以,不是说化学成分一样就一样了。还得考虑制剂工艺。
药物多晶型按稳定性分稳定型、亚稳、无定型。从物理化学角度,不稳定的晶型在热、外力的环境下,会变成更稳定的晶型。
稳定晶型成药性
- 如果稳定晶型用来成药,并且不影响口服药的吸收和分布是最完美的。
- 不幸,很多药的稳定晶型口服生物利用度非常差,过于稳定不溶解,甚至有出现“安全无效”的情况。类似金针菇“see you tomorrow”。
雅培首次上市利托那韦是以胶囊形式上市(1996年),在当年的固体制剂工艺下,片剂口服是没有生物利用度的,本身溶解性很差,很多BCS IV类的药物有类似特征。所以利托那韦刚开始用的是胶囊剂和口服液,API是亚稳定晶型Form I。
但不知道为什么,部分制剂生产工厂出现API不溶解问题,后来发现是由于原料药厂商生产不出Form I晶型的原料药,历史上有名的“消失的晶型”,生产出来的全都是Form II稳定晶型,而且像会传染似的,只要有一点儿Form II 晶种,原液都以Form II稳定晶型析出。Form II稳定晶型的原料药在后续湿法制剂时,非常难溶解,更糟糕的是,析出Form II晶型有很多残留溶剂和杂质。
三、利托那韦片剂没有想象的那么容易,需重视制剂企业稀缺性
已经上市的利托那韦胶囊,发现“转晶”,生物利用度暴跌,利托那韦胶囊在1998年撤市,损失超过2.5万亿美金。
在那以后,人们对晶型的控制愈加关注。
因为Form I的胶囊剂容易“转晶”,后来在2010年推出了片剂,使用Meltrex® technology技术制备成热稳定的片剂。这项核心技术降低了利托那韦胶囊制剂中发生转晶的风险,又保证了口服生物利用度。
所以,利托那韦开发的核心难点:
(1)API的晶型控制
(2)能获得生物等效性的片剂工艺。
以上两者缺一不可。中国要真的成为制药大国,不光盯着原料药中间体这些上游环节。学习完利托那韦片开发,就开始理解为什么化工行业和制药行业附加价值差异这么大。可重复的工艺控制,夯实的制药工程研究,才能创造更高价值。
如果在国内查利托那韦上市,能查到的口服液和胶囊剂,这类产品有较大的风险发生“转晶”,不是稳定制剂,意义不大。能查到歌礼药业有片剂制剂,并且通过了仿制药一致性评价。目前不知道国内有多少公司能搞定片剂的制备,控制“转晶”,又能复刻原研药艾伯维的口服生物利用度。希望东阳光药能做到,不过他21年4月就完成了BE试验,过了小半年还没提交申请,不知是数据不好还是还在补充材料。看到歌礼药业为了补充自己的丙肝组合,从19年就奋发做BE,做了3次才通过,估计制剂工艺不太好摸索。
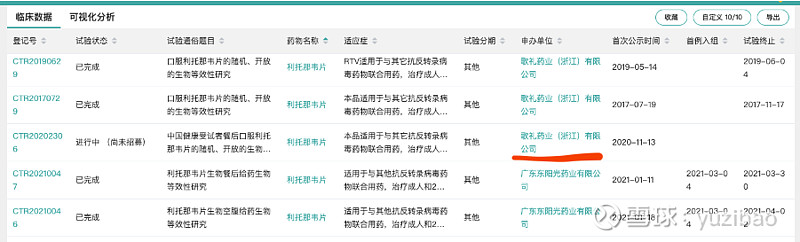
能查到的美国上市利托那韦仿制药企业有6家仿制药片剂,欧盟只有2家。


这样看来,最近歌礼制药涨也不是没有道理,市值比较小,弹性是足够的。但不知道为何周四周五跌下来,难道是大家看到满天飞的利托那韦化合物供应,认为制剂就能很快攻破吗?还是想的有点天真了。在原研药艾伯维紧缺的情况下,其他公司想开展一致性评价看是难度不小吧。
$森萱医药(BJ830946)$ $歌礼制药-B(01672)$ $精华制药(SZ002349)$
参考资料:
《晶型药物》. 吕扬,杜冠华.
我国化学药物晶型研究现状与进展_杨世颖
Chemburkar S R ,Bauer J , Deming K , et al. Dealing with the Impact of Ritonavir Polymorphs onthe Late Stages of Bulk Drug Process Development[J]. Org.proc.res.dev, 2000,4(5):413-417.