港股终于又迎来了一家生物医药公司。
今天,专注肿瘤免疫治疗创新药研发及商业化的生物公司思路迪医药(3D Medicines Inc)成功登陆港交所。
其母公司思路迪是一家肿瘤精准医疗公司,旗下有思路迪医药和思路迪诊断,两者在2018年完成分拆。思路迪医药在IPO前获得多轮融资,其中不乏高瓴资本、倚锋资本、中信建投投资海德资本等知名投资机构。
思路迪医药拥有1款核心单品PD-L1单抗恩维达,以及11款候选药物产品,包括恩维达在内的大部分产品来自于其他公司授权,覆盖肿瘤免疫单药治疗、具有可与管线产品联用的作用机制的创新候选药物及疼痛管理资产,但公司尚未实现盈利。
自2018年以来,港股上市成为未盈利生物医药公司“补血”的重要一步。港股自去年以来的暴跌对这些公司股价造成了巨大冲击,定价扭曲和流动性不足,生物科技公司市值一直在煎熬。消极情绪到底后,近期港股有所回升,同时可以注意到,12月伊始,在港交所有IPO新动态的生物医药公司除思路迪医药之外,还有:双抗药物研发生产公司友芝友生物已向港交所递交IPO申请,绿叶制药控股子公司博安生物通过港交所上市聆讯,等等。
思路迪医药是2022年港股第五家上市的生物医药企业,今年前四家港股IPO的公司为乐普生物、瑞科生物、百奥赛图、艾美疫苗。思路迪医药CEO为前FDA新药审评专家龚兆龙博士,合作方包括康宁杰瑞、先声药业、SELLAS、Aravive等,能在分拆后四年内完成上市,也是对其临床开发能力、资源部署整合以及商业化优势的印证。
三顾港交所终成功
这是思路迪医药第三次递交港股招股书。在此之前,公司曾于2021年6月30日及2021年12月31日分别向港交所递交招股书,但均因未能在6个月内通过港交所聆讯致上述两份招股书失效。
虽然冲刺二级市场历经波折,但在一级市场,思路迪医药一直是投资机构青睐的标的。在递交IPO申请前,公司已完成数轮融资,投资机构涵盖高瓴资本、新天域资本、倚锋资本、中信建投投资、先声药业、泰格医药等多家知名机构,累计融资额达2.3亿美元,约15.5亿元人民币。招股书显示,思路迪医药投后估值已经达到7亿美元。
密集融资下仍然执着于IPO上市的思路迪医药,显然是因为对现金流维持有较大需求。
创新药企的成长之路普遍经历过前期“烧钱”研发,等到产品面世再“回血”的路径。招股书显示,思路迪医药在2019年、2020年研发投入分别为2.3亿元、2.64亿元。此外,2021年2月,思路迪医药研发生产基地在徐州正式开工,此项自建的GMP车间占地约80000㎡,总投资25亿元。
2020年、2021年和2022年前5个月,思路迪的营业收入分别为0、0.60亿、1.61亿元人民币;相应的净亏损分别为6.35亿、14.62亿和2.93亿元人民币。在今年5月底,集团剩余的现金及现金等价物6.6亿元。
不过,和今年在港股IPO上市的大部分生物科技公司一样,思路迪医药的融资额并不大,根据招股价,公司最多募资4.29亿港元。据招股书,此次IPO募集资金主要用于产品和候选药物的研发、监管备案及商业化;用于业务开发活动,扩大药物管线及组合,潜在收购高价值及独特的创新资产等。
观察思路迪医药的管线药物,几乎全部为自其他公司取得授权,其自有研发药物尚停留在早期临床或临床前阶段。盈利尚需时间的思路迪医药此次能登陆港交所,可能与其核心产品恩沃利单抗,即恩维达的正式获批与商业化进度有关。
恩维达于2021年11月获批,并于2021年12月商业化,这款PD-L1单抗适用于不可切除或转移性微卫星高度不稳定(MSI-H)或错配修复基因缺陷型(dMMR)的成人晚期实体瘤患者的治疗,给药途径为皮下注射,而大多数竞争者的给药途径为静脉滴注。2022年4月,恩维达写入3部2022版CSCO指南。官方数据显示,截止2022年5月31日,该品种商业化以来销售收入为2.21亿元人民币。
CEO是前FDA新药审评专家,
“BLA申报”是强项
值得注意的是,恩维达不属于思路迪医药独有。恩维达最开始是康宁杰瑞制药自主研发的产品,内部代号为KN035,思路迪医药于2016年开始参与共同研发,之后这款PD-L1在大陆地区的推广权交给了先声药业,而先声药业也是思路迪医药的股东之一。
根据销售计划,康宁杰瑞在按一定比例加成后,会以出厂价将药品销售给先声药业,后者在完成商业化销售后,从收入端提取一定的销售分成,剩下的税前利润才由思路迪和康宁杰瑞来平分。
虽然三家创新药公司共享一款PD-L1会让思路迪医药获得的收益打折扣,但是可以从这项合作中看到思路迪医药资源部署整合优势,以及商业化能力。
据华人抗体协会的资料,恩维达——彼时还是KN035的IND申请是国内首家在没有临床数据的情况下,直接向FDA申报并获准在美国开展全球首次临床试验的项目。根据康宁杰瑞和思路迪的合作开发协议,康宁杰瑞负责临床样品和上市后药品生产,思路迪主导全球注册、临床开发和商业化。
思路迪医药和康宁杰瑞的合作可称为高效,两家公司在签署合作协议后仅9个月,就使项目在没有临床数据的情况下成功申报在美国开展全球首次临床试验,并在4年内完成了IND的提交到BLA的获批,完成了新药开发整体过程。
恩维达是全球首个获批BLA的皮下注射PD-L1抗体。根据FDA要求,一款药品从研发至上市需要经历临床前试验、新药临床试验申请、临床试验等步骤,最终提交BLA(生物制品许可申请)或NDA。
弗若斯特沙利文研究显示,创新肿瘤药物从IND阶段推进至BLA或NDA阶段一般耗时五至六年。据思路迪医药招股书,“BLA申报”是思路迪医药的强项,公司能够凭借临床团队的试验管理及技术优势在多个国家及地区的临床试验中高效招募患者。
同时,思路迪医药在国际注册的优势和其CEO龚兆龙博士密不可分,龚兆龙拥有10年的FDA新药审评工作经验,也是最早一批回国创业的前FDA评审专家。回国后曾在百济神州等多家新药研发企业担任高管,参与和推动百济神州3个创新药快速进入临床开发及国外权益转让,熟悉药物开发和审评的相关国际法规。
目前来看,思路迪医药的商业化合作布局广阔,其他建立合作关系的国内及跨国知名制药及生物科技公司包括默克、TRACON、SELLAS、Aravive、海和药物、Y-Biologics及Immune Oncia等。具体合作包括与TRACON在美国、加拿大及墨西哥开展恩维达针对软组织肉瘤患者的临床试验,以及恩维达和由默克研发的靶向表皮生长因子受体(EGFR)的单克隆抗体西妥昔单抗将开展联合给药研究。
初步可见肿瘤慢病化生态布局
围绕公司的合作商业化产品,思路迪医药尝试建设肿瘤慢病化的生态矩阵。思路迪医药的招股书中特别说明,癌症治疗慢病化成为肿瘤治疗的未来主要趋势,公司着力组建并正在开发疗法组合,以帮助需要长期治疗的癌症患者。
官网资料显示,根据“癌症治疗慢病化市场中的主要市场参与者”这一定位,公司的布局方式为:肿瘤免疫管线为核心,部署单药/联用肿瘤产品矩阵,包括多适应症抗体新药和肿瘤疫苗;疼痛管理解决方案为辅助,包括肿瘤疼痛、术后牙痛等;未来产品除继续针对多适应症肿瘤免疫疗法,还会布局转移性实体瘤和局部晚期实体瘤管线作为协同。
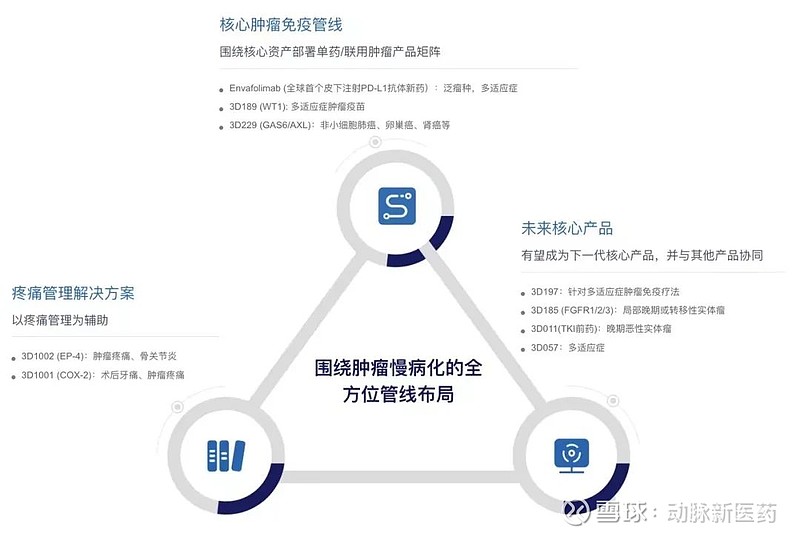
▲思路迪医药管线布局,来源:公司官网
且从目前的核心产品来看,预后、延迟复发、优化给药,是思路迪医药参与中国肿瘤药物市场增长的关键词。
如和SELLAS合作的在研多肽癌症疫苗Galinpepimut-S (3D189),已于今年4月获NMPA批准,用于开展评估该药品在血液肿瘤患者中的安全性和免疫原性的I期临床研究。
3D189为新一代靶向WT1(Wilms肿瘤蛋白)的潜在“first-in-class”肿瘤免疫治疗新药,在过度表达WT1的超过20种癌症(包括肺癌及结直肠癌)中具备靶向治疗潜质,被设计用于预防及推迟复发(通过延长无进展生存期)及有望延长该等患者的生存期。
还有和Aravive合作的一款靶向GAS6-AXL信号通路的抑制剂3D229(又名AVB-500),这款抗卵巢癌新药在去年7月获CDE批准加入国际多中心III期临床试验。
卵巢癌预后差,5年生存率仅40%,且极易复发,约70-80%对铂类治疗敏感的患者经多次复发后最终对铂类化疗耐药。GAS6-AXL信号通路是促进肿瘤生长的重要通路,而AVB-500药物能够强力、有选择性的中和GAS6,靶向抑制肿瘤生长,在治疗铂耐药复发性卵巢癌中,AVB-500展示出良好的安全性和抗肿瘤疗效。
以及恩维达本身,也在今年8月获得了NMPA“新增300mg每两周给药一次”的补充申请批准,新的用法用量的获批基于在日本与美国的数据,将减少药品使用频率,通过给药方案的优化,提供给肿瘤患者更好的治疗选择。
在国内激烈的单抗类药物竞争中,思路迪医药在港股IPO冲刺主打“肿瘤慢病化治疗第一股”。越来越多“第一股”的诞生,表明行业垂直细分机会增多。但是,如何在真正把细分赛道从“概念”到“走通”,可能是企业上市后更艰难的课题。