目前,新冠疫情仍在影响全球多个国家。最新数据显示,截至5月21日,全球累计COVID-19确诊病例已超过500万例。新冠疫苗的成功研发将对控制疫情起到至关重要的作用。

来源:《柳叶刀》
5月22日,顶级医学期刊《柳叶刀》发表了我国军事医学研究院陈薇院士和江苏省疾控中心朱凤才教授团队的新冠疫苗人体试验临床数据结果。研究结果显示,I期临床108名志愿者全部有显著的细胞免疫反应。据悉,这是世界首份新冠疫苗的人体临床数据。
具体来说,该研究(NCT04313127)旨在评估表达SARS-CoV-2棘突糖蛋白的重组5型腺病毒(Ad5)载体COVID-19疫苗的安全性、耐受性和免疫原性。
研究小组在中国武汉进行了Ad5载体COVID-19疫苗的剂量递增、单中心、开放标签、非随机、Ⅰ期试验。年龄在18至60岁之间的健康成人按顺序登记并分配到3个剂量组(5×1010, 1×1011和 1.5×1011 病毒颗粒)中的一个,通过肌内注射接种疫苗。主要结果是疫苗接种后7天的不良事件。在接种疫苗后28天内进行安全性评估。特异性抗体用ELISA检测;疫苗诱导的中和抗体应答通过SARS-CoV-2病毒中和试验和假病毒中和试验检测;T细胞响应用酶联免疫斑点法和流式细胞仪检测。
2020年3月16日至3月27日,研究小组筛选了195位参与者。最终,108位参与者(51%为男性,49%为女性;平均年龄36.3岁)接种了低剂量(n=36)、中等剂量(n=36)或高剂量(n=36)的疫苗。所以被招募进研究的参与者都被纳入了结果分析。
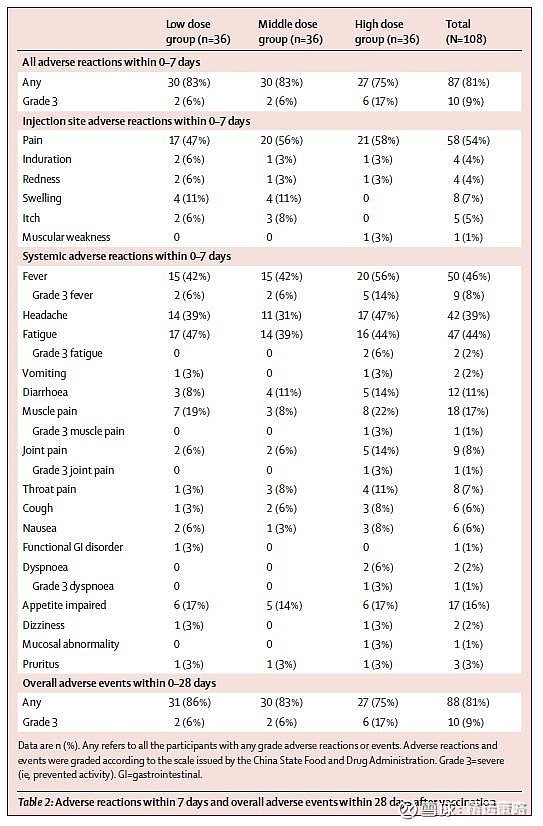
结果显示,低剂量组、中等剂量组均有30名(83%)参与者在接种疫苗后的头7天内报告了至少1项不良反应,而高剂量组有27名(75%)参与者在接种疫苗后的头7天内报告了至少1项不良反应。最常见的注射部位不良反应为疼痛,有58位疫苗接种者报告了该不良反应。最常见的系统性不良反应为发热(50例[46%])、疲劳(47例[44%])、头痛(42例[39%])和肌肉疼痛(18例[17%])。所有剂量组报告的大多数不良反应的严重程度为轻度或中度。疫苗接种后28天内未显示有严重不良事件发生。
表2:疫苗接种后7天内的不良反应和28天内的总体不良反应
此外,在接种后第14天,ELISA抗体和中和抗体显著增加,在接种后第28天达到峰值。在接种后第14天,特异性T细胞反应也达到峰值。
表3:对受体结合域的特异性抗体应答,以及中和活SARS-CoV-2的抗体
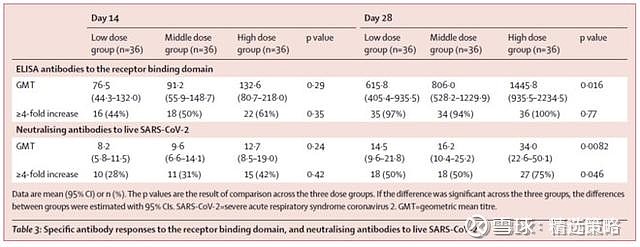
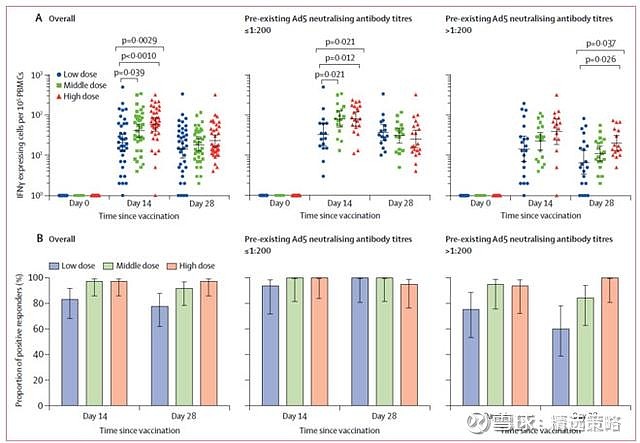
图1 ELISpot检测的特异性T细胞应答
基于以上研究结果,研究团队认为,5型腺病毒载体COVID-19(Ad5-nCoV)疫苗在接种28天后是可耐受的、具有免疫原性的。在健康成年人中,对SARS-CoV-2的体液反应在接种疫苗后第28天达到高峰,并且在接种疫苗后第14天观察到快速的特异性T细胞反应。综合这些结果表明,5型腺病毒载体COVID-19(Ad5-nCoV)疫苗值得进一步研究。
陈薇院士称,这是一个里程碑,但应谨慎解释这些结果,触发这些免疫反应的能力并不一定表明5型腺病毒载体COVID-19(Ad5-nCoV)疫苗将保护人类免受COVID-19的侵害,这一结果显示了开发COVID-19疫苗的希望,但距离所有人都能使用这种疫苗还有很长的路要走。
此外,研究者们还指出,该试验的主要局限性在于其样本量小、持续时间相对较短以及缺乏随机对照组。在所有人都可以使用该试验疫苗之前,需要进一步的研究。目前,一项针对5型腺病毒载体COVID-19(Ad5-nCoV)疫苗的随机、双盲、安慰剂对照II期临床试验已启动,以确定是否能够复制I期研究结果。
相关论文:
[1] Feng-Cai Zhu et al. Safety, tolerability, and immunogenicity of arecombinant adenovirus type-5 vectored COVID-19 vaccine: a dose-escalation,open-label, non-randomised, first-in-human trial. TheLancet (2020).
参考资料:
1# 重磅!陈薇院士新冠疫苗临床试验结果发布:全部产生免疫应答!(来源:健康时报)
yan2020zhi 上面微信你添加下,这里发不了文件,添加申请时请务必备注:ss