
3月27日,和黄医药赛沃替尼片新适应症上市申请获CDE受理。根据和黄医药近期发布的年度报告,推测此次申报适应症为:一线及二线治疗MET外显子14跳跃突变非小细胞肺癌(NSCLC)患者,有望将赛沃替尼片在中国的适应症拓展到一线患者。
赛沃替尼(savolitinib,沃瑞沙)是一种口服的高选择性小分子c-Met抑制剂,最初由和黄医药开发,2011年,和黄医药与阿斯利康达成一项全球许可协议,将共同开发沃瑞沙并促进其商业化。和黄医药与阿斯利康合作负责赛沃替尼的临床开发,在中国由和黄医药主导,在海外则由阿斯利康主导。此外,和黄医药负责赛沃替尼在中国的上市许可、生产和供应,而阿斯利康则负责实现沃瑞沙在中国乃至全球范围内的商业化。赛沃替尼的销售收入由阿斯利康确认。
阅读下文,了解更多新药研发获批信息
3月28日药品受理信息
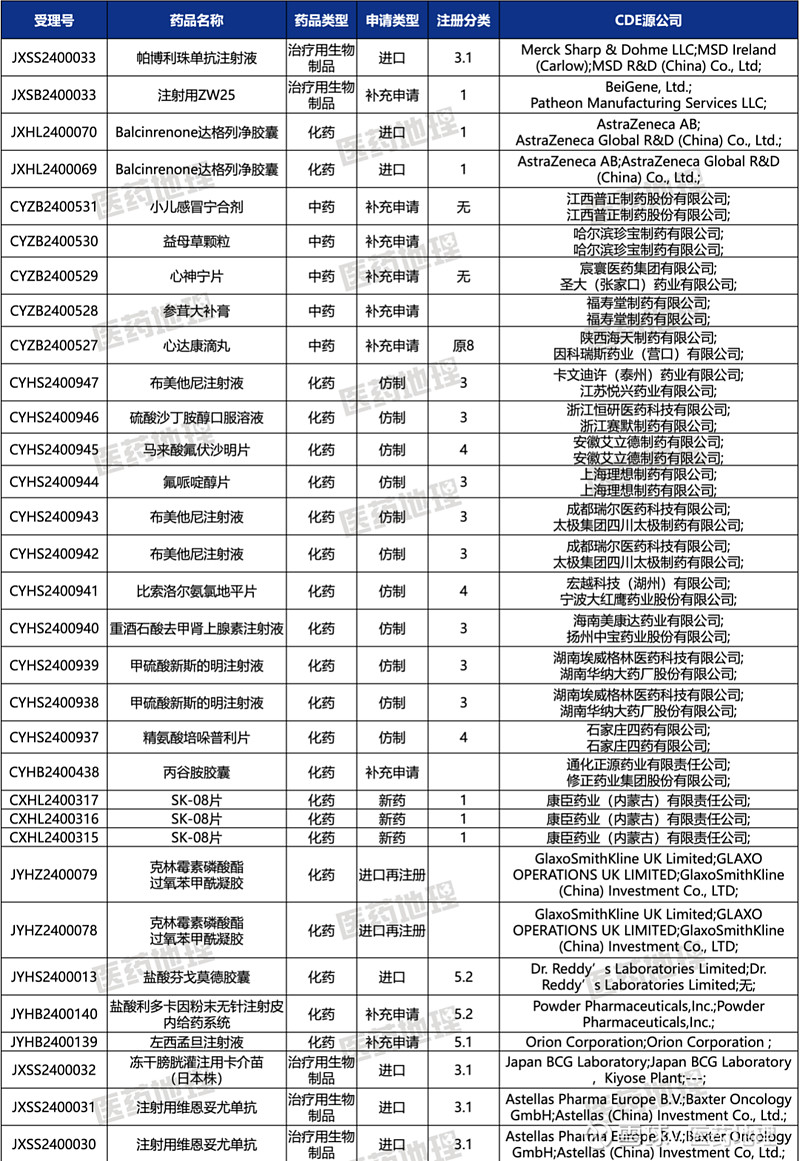
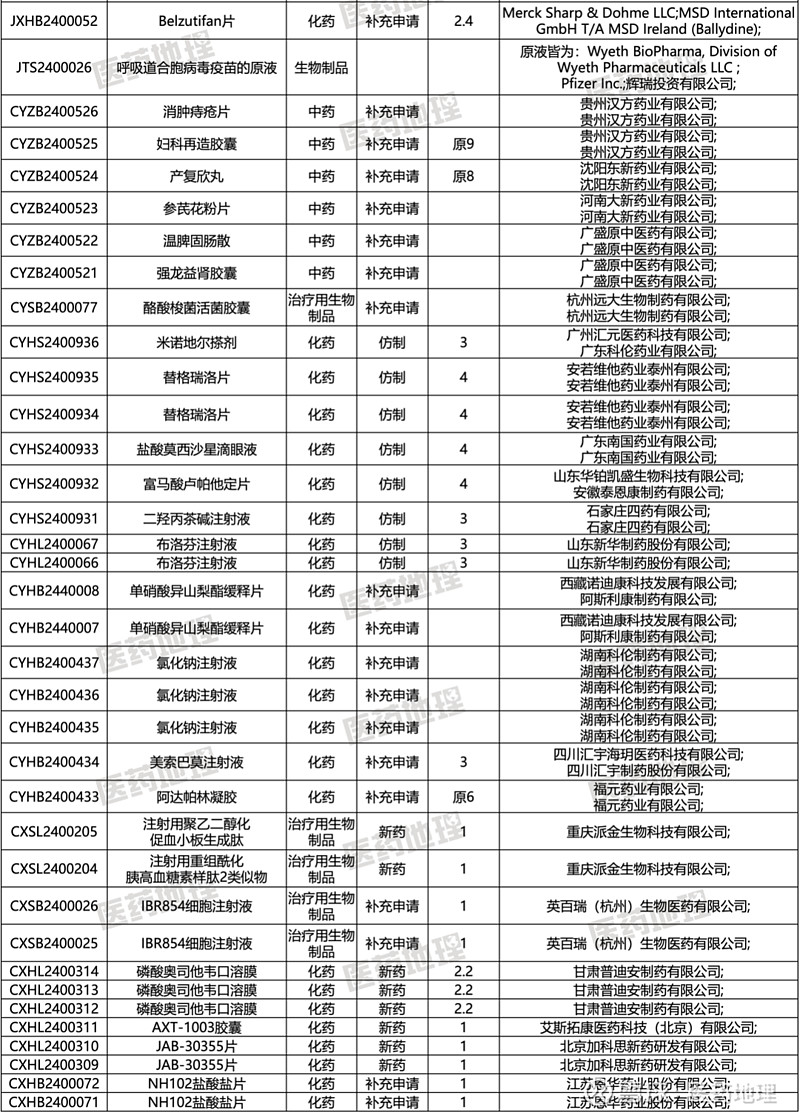
来源:Pharma ONE智能药物大数据分析平台
3月28日,CDE公示了68条药品受理信息(按受理号区分),从“药品类型”上看,“化药”共有46款,“治疗用生物制品”共有10款,“中药”共有11款,。
从“申请类型”上看,“补充申请”共有28款,“新药”共有11款,“仿制”共有19款,“进口”共有7款,“进口再注册”共有2款。
从“注册分类”上看,“1类药品”共有15款,“2.2类药品”共有3款,“2.4类药品”共有1款,“3类药品”共有13款,“3.1类药品”共有4款,“4类药品”共有7款,“5.1类药品”共有1款,“5.2类药品”共有2款。
END
如需获取更多数据洞察信息或公众号内容合作,请联系医药地理小助手微信号:pharmadl001
