
2022年4月26日,华海药业子公司华博生物HB0034注射液的临床试验申请获得NMPA受理。

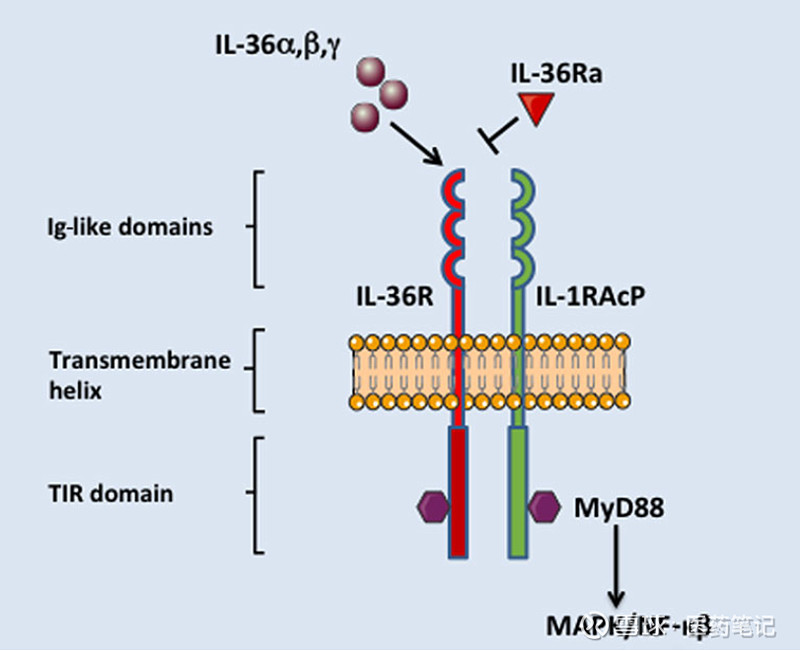
HB0034为IL-36R抗体,也是国内首款申报临床的IL-36R抗体。IL-36Rα 、β、γ结合IL-36R,后者随之与IL-1RAcP形成异源二聚体,进而激活胞内下游信号通路。
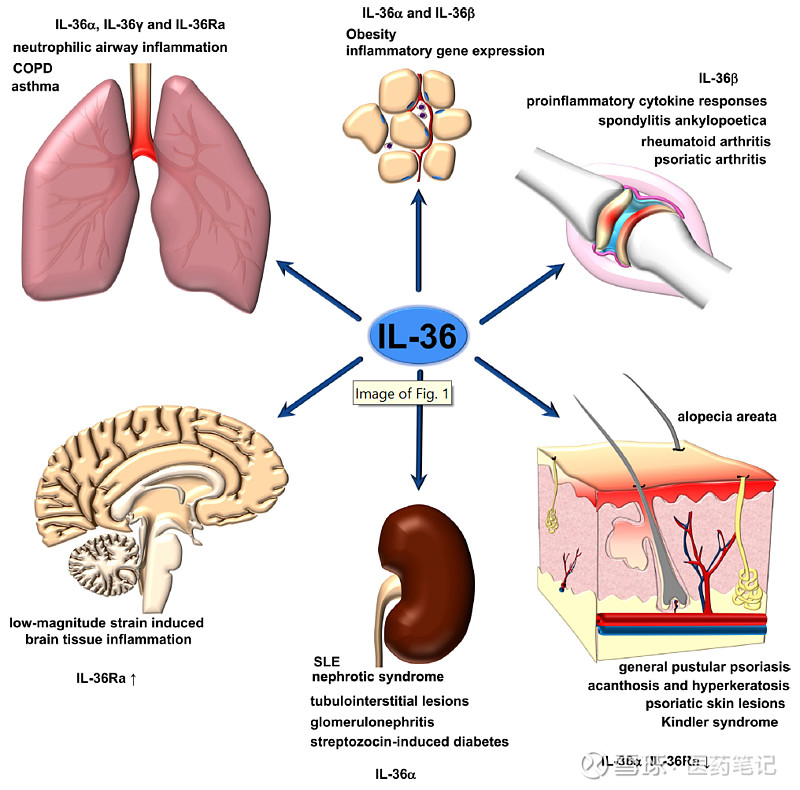
IL-36R参与多种自身免疫病的发病机制。
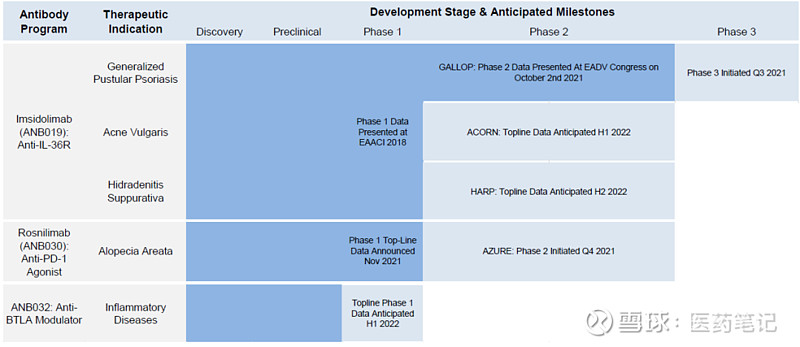
IL-36R抗体Imsidolimab为AnaptysBio自主管线中首个产品,在探索脓疱型银屑病、痤疮、化脓性汗腺炎等三种适应症。
2021年3月8日,AnaptysBio宣布IL-36R抗体Imsidolimab治疗掌跖脓疱病的二期临床失败。

2022年3月14日,AnaptysBio宣布IL-36R抗体Imsidolimab治疗痤疮的二期临床ACORN没有达到疗效的主要终点和次要终点。

2022年3月28日,勃林格殷格翰公布其IL-36R抗体Spesolimab治疗GPP的二期临床数据,12周治疗后84.4%的患者无可见脓疱,81.3%患者皮肤清除或接近清除。

总结
从目前的临床数据来看,IL-36R靶点具有极大临床价值,但IL-36R抗体在不同适应症的临床表现差异较大,目前来看GPP(泛发性脓疱型银屑病)的临床响应较为理想,其他适应症如痤疮、PPP(掌跖脓疱病)等则表现欠佳。