
▎Armstrong
2022年2月11日,礼来宣布第3款新冠中和抗体Bebtelovimab获得FDA的紧急使用授权(EUA)。

2月10日,礼来刚刚与美国政府签订这款中和抗体的60万剂订单,总金额达7.2亿美元(1200美元/剂)。

此前,礼来已经有2款中和抗体获得FDA的EUA,分别为从Abcellera引进的Bamlanlvimab和从君实生物引进的JS-016。Bebtelovimab为Abcellera开发的第2款中和抗体。

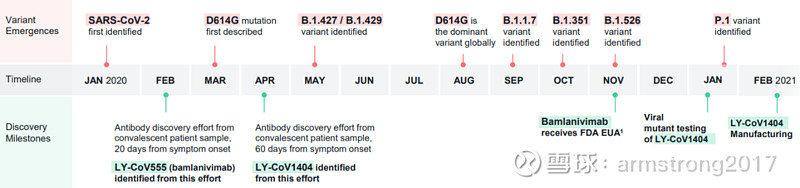
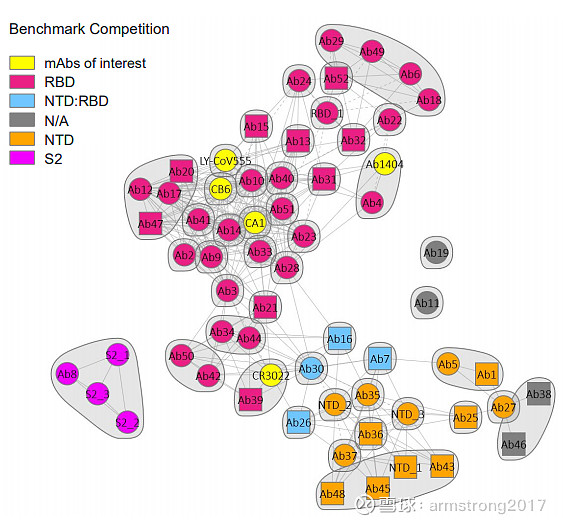
Bebtelovimab为Abcellera合作开发的第2款中和抗体,与Bamlanvimab筛选的时间仅相差两个月,同样来自康复患者样本。
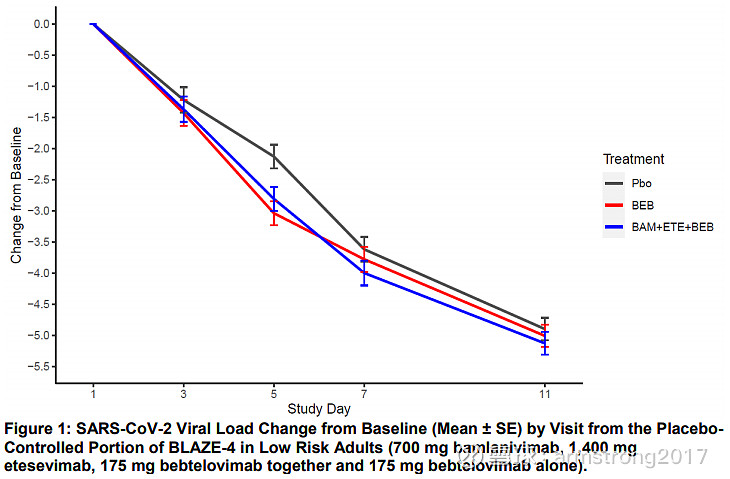
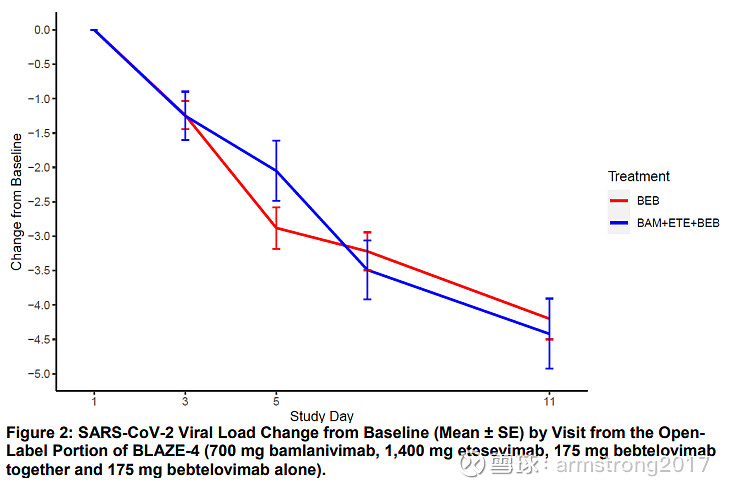
此次获批是基于二期临床数据,对于低风险和高风险患者,175mg Bebtelovimab在降低病毒滴度方面的效果都与Bamlanvimab+Etesevimab+Bebtelovimab三者联合相当。
Bebtelovimab加速获批的重要原因是其为一款广谱中和抗体,对目前所有已知的关键突变株都保持了强大的中和活性,包括Omicron突变株。
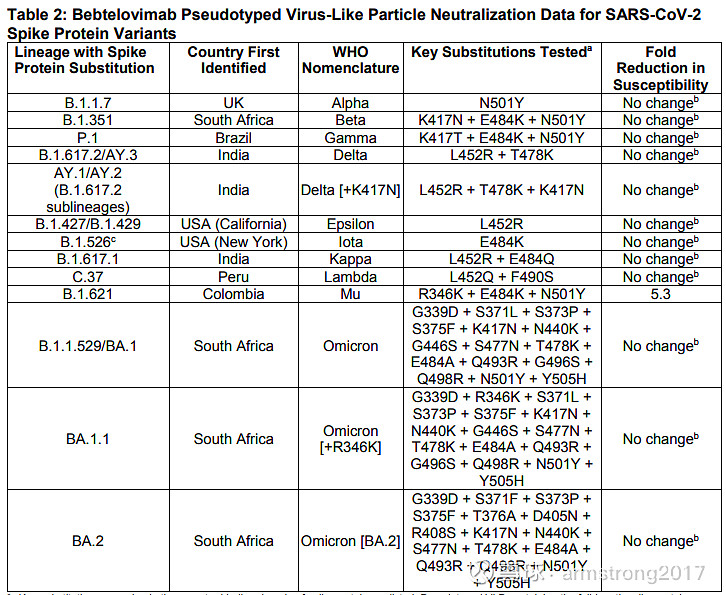
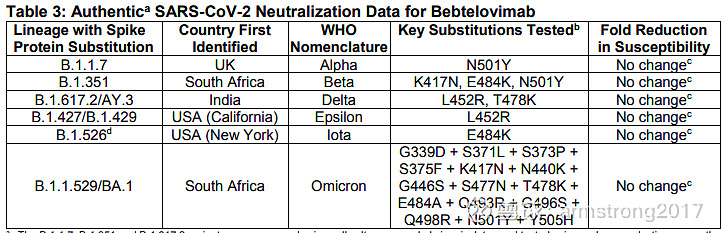
Bebtelovimab对Omicron的中和活性超过所有其他已上市的新冠中和抗体。
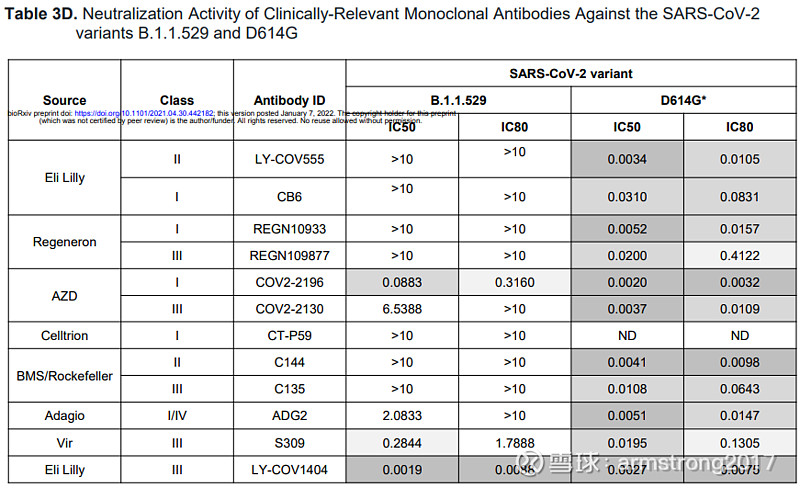
2022年1月,FDA已经限制再生元与礼来中和抗体的使用,因其对Omicron突变株无效。Bebtelovimab成功接替了Bamlanvimab(Abcellera)和Etesevimab(君实生物),且剂量更低仅175mg,而后两款中和抗体的剂量为700mg。
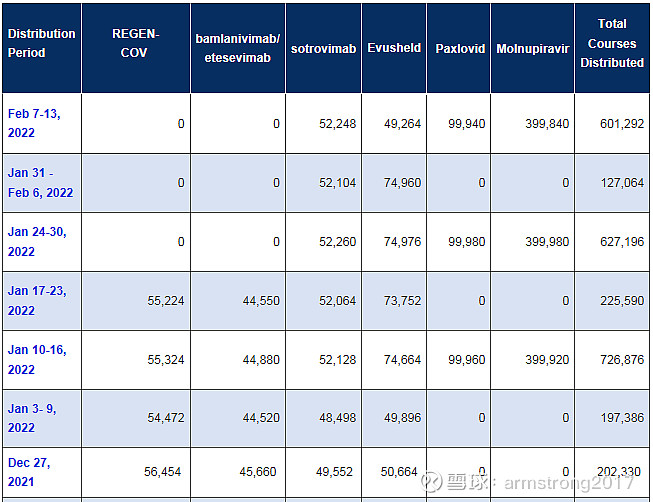
总结
2021年,再生元中和抗体销售额76亿美元,礼来中和抗体销售额22亿美元。随着Omicron突变株的流行,新冠治疗药物集中在礼来新一代中和抗体、Vir Bio、阿斯利康的中和抗体,以及辉瑞、默沙东的新冠口服药。辉瑞已经与凯莱英签订57亿元人民币的CDMO订单,昨日又与博腾股份签订43亿元人民币的CDMO订单,2022年Paxlovid的计划产能高达1.2亿疗程。