2020年2月12日“医耘沙龙”第十期PROTAC靶向蛋白降解平台药物研发报告及投资机会探讨于线上举行。本次沙龙邀请了华医资本合伙人曹锋博士和嘉兴优博创始人曹小冬博士对PROTAC靶向蛋白降解平台药物研发进行了深度探讨,近百位投资人参与了本次线上沙龙。下文是关于PROTAC靶向蛋白降解平台药物的深度行研分享。
核心要点:
首先,看好PROTAC靶向蛋白降解领域。疾病治疗领域的空间广阔,市场巨大,未来可期。
其次,PROTAC技术处于快速成长期,适合早期赛道投资。目前的突破点还是首选一些经过验证的靶点,降低变量,证明PROTAC的可行性,未来有望直接靶向“不可成药”靶点。
最后,投资标的选择标准主要为以下两个:
团队组成:因为涉及三联体的设计、合成和验证,所以需要资深化学、药学专家的加盟;另外,需要有对泛素蛋白酶系统研究深度了解的科学家。
技术:自身有专利或者授权专利,不与现有国际专利形成冲突;有独特的平台技术,来解决目前PROTAC平台遇到的问题;差异化的管线品种(对适应症和靶点的选择)。
什么是泛素-蛋白酶体系统?
泛素-蛋白酶体系统是人体内天然的蛋白质降解途径。众所周知,蛋白质是生命活动的主要承担者,因此维护机体蛋白的平衡非常重要。这样的动态平衡不仅包括蛋白质的生成,也包括多余或异常蛋白质的降解。
真核细胞内蛋白质的降解途径主要有三种:泛素化途径、胱天蛋白酶(caspase)途径以及溶酶体途径。
本文探讨的PROTAC技术和泛素-蛋白酶体系统 ( ubiquitin-proteasome system,UPS)相关。
通过泛素-蛋白酶体系统降解蛋白可分为以下几个步骤:E1泛素激活酶在其C端激活Ub,Ub与E2泛素结合酶结合,然后通过E3泛素连接酶将Ub转移至底物蛋白。最后,在经过多轮泛素化后,底物蛋白会被蛋白酶体识别并降解【1】。另外,泛素化过程也是可逆的,去泛素化酶可以将泛素从泛素链上去除。
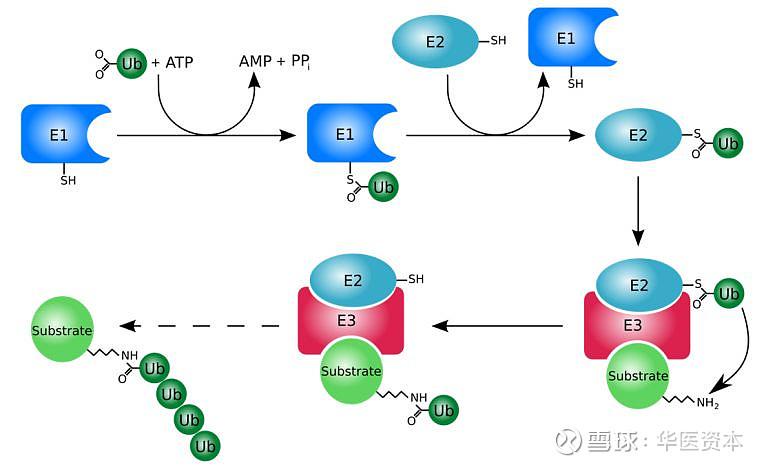
图片来源:公开资料
Aaron Ciechanover, Avram Hershko和Irwin Rose三人由于发现了该机制,于2004年被授予了诺贝尔化学奖。基于这个发现,有无科学家想到利用类似原理来降解想要降解的蛋白质呢?在2001年,Crews和Deshaies实验室报告了第一个基于蛋白降解的PROTAC(Proteolysis Targeting Chimera)分子,命名为Protac-1。
那么PROTAC具体是什么样子呢?(下图)
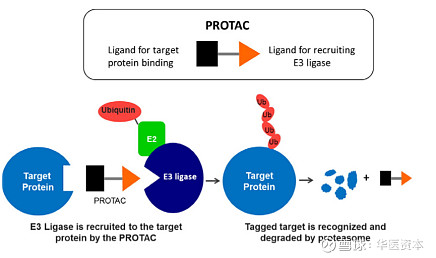
图片来源:公开资料
PROTAC就是靶向蛋白降解的小分子联合体,联合体分子包括三部分:左边是结合目标蛋白的配体;右边是可以招募E3泛素连接酶的配体;中间则通过合适的连接器(linker)连接【2】。
泛素-蛋白酶体系统对于制药领域的影响?
蛋白质异常会导致人体疾病的发生,然而传统的小分子和抗体药物只能靶向大约20%的蛋白,这中间还存在着大量的需求,也就是“未成药靶点”。
这些“未成药靶点”有可能成为PROTAC作用的靶点,PROTAC极大的扩大了作用于蛋白的成药范围。
PROTAC分子在体内的过程就是:PROTAC的两端分别识别靶蛋白和E3泛素连接酶并形成靶蛋白-PROTAC-E3的三元复合物, 接着在靶蛋白被泛素化后,会通过泛素-蛋白酶体的途径被降解。值得一提的是,完成上述过程后,PROTAC分子会被释放出来参与下一个蛋白的降解过程,因此这里的PROTAC分子扮演的更类似于一个酶催化的角色。
泛素-蛋白酶体系统的发展历史
PROTAC技术开发已有20年的历史。
第一代PROTACs是基于肽段基序作为 E3 泛素连接酶的配体。虽然此时的PROTAC分子提供了概念验证,但是由于细胞渗透性较差,降解活性仅在微摩尔级水平【3】。
第二代PROTACs的标志是利用小分子作为 E3 泛素连接酶部分,因为小分子更容易被人体吸收,也更容易成药。值得注意的是,2019年已有2个药物进入临床I期。
在下图中,华医资本研究院根据文献中的历史沿革做了简单的汇总,对PROTAC历史感兴趣的读者可以回看该文献,里面会有更详细的描述。

图片来源:文献【3】,华医资本汇总
与此同时,在海外该技术也获得了资本的热捧和众多跨国制药公司的青睐。相信在不久的将来,中国研发PROTAC的公司也会迎来越来越多的融资。
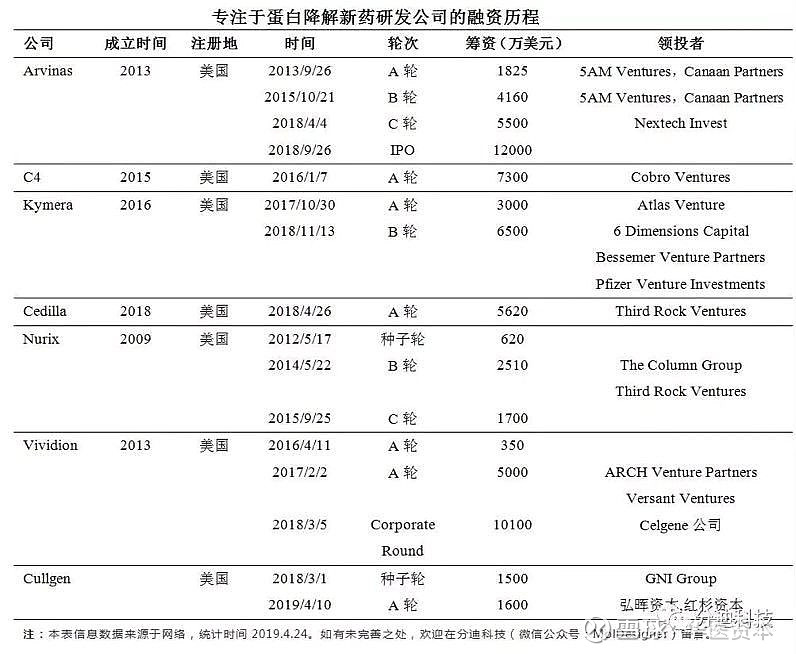
图片来源:分迪科技汇总
目前的PROTAC技术发展怎么样了?
在前文说到,目前基于PROTAC技术的药物已经有2个进入I期临床,已经是不小的进步。然而总体来说,PROTAC的挑战也是巨大的,虽然经历了20年的研发,整个PROTAC平台的药物研发还属于早期阶段。
我们先来说说PROTAC的优势。
其一,PROTAC技术可靶向未成药蛋白。由于PROTAC平台的药物是依赖于靶蛋白-PROTAC降解剂-E3形成的三元复合物来实现靶蛋白降解,而不是依赖于分子与靶蛋白活性中心的共价结合。因此对亲和力的要求更低一些,只需要和靶蛋白结合的时间足够完成泛素化标记即可。
其二,克服现有药物的耐药性。耐药性产生的一个主要原因是靶蛋白结合口袋区域的氨基酸残基发生突变。PROTAC分子可以选择不靶向口袋区,因此能克服现在点突变带来的耐药性。
其三,选择性和安全性更佳。目前已有多项研究证明,基于多靶点抑制剂设计的PROTAC分子能与多个靶蛋白结合,但是降解的蛋白只是其中少数几个。
其四,安全性更佳。这有两个原因:1. 选择性更佳,因此脱靶更少,毒性少;2. PROTAC分子是可以循环利用的,因此需要的剂量低,理论上也更安全。
Arvinas公司(目前两个药物进入临床的)的创始人Crew(PROTAC技术的引领者)等人也曾于2017年发表论文【4】描绘了PROTAC平台的优势,不过华医研究院认为对于目前来说,Crews教授描绘的优势还是有些理想化,想要发挥PROTAC的全部功效,还需要时日。
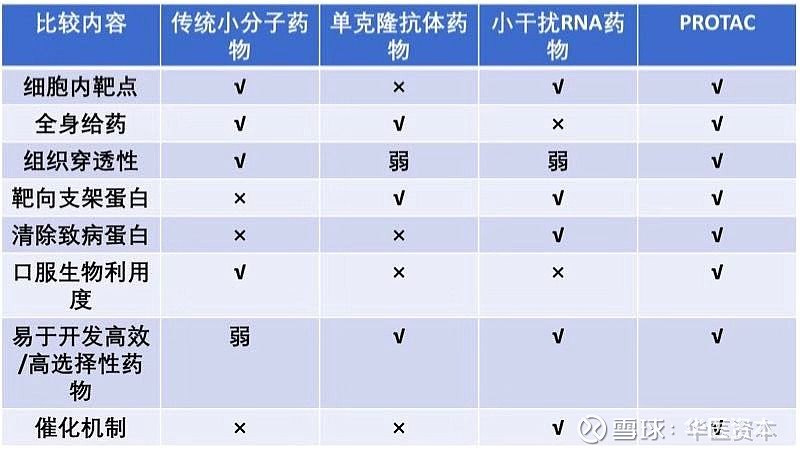
图片内容来源:文献【4】
值得注意的是PROTAC违反了药物化学领域的信条类药五原则(rule of five),药效学与药代动力学分离,且在药物的特异性、结合能力和特异性上也与和传统小分子的模式不同。因此既往的经验往往不能成为PROTAC成药的帮助,因此挑战也是巨大的,主要面临如下挑战:
1. PROTAC是三部分组成,其分子量偏大,口服吸收和透明性都比较差,PK/PD也是问题。
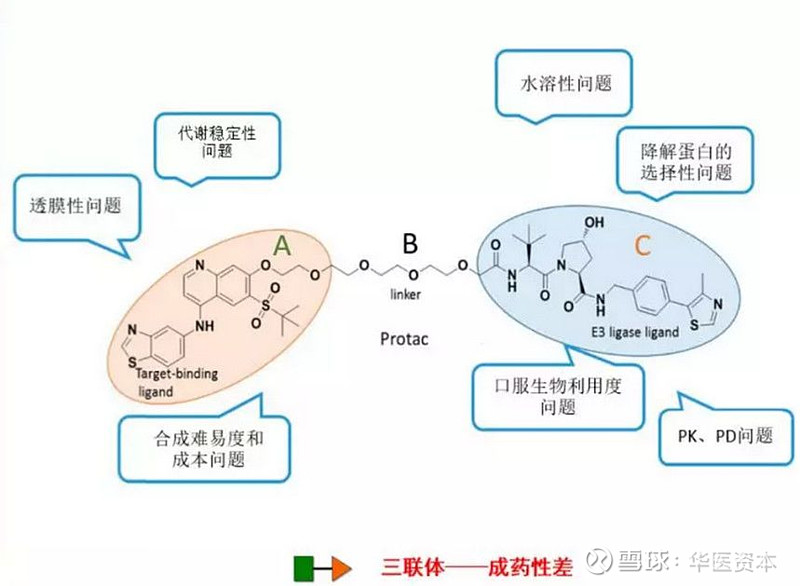
图片来源:公开资料
2. 如何理性设计PROTAC,有效形成三元复合物,并有效激活降解系统。
蛋白降解并不仅仅取决于二元目标蛋白与配体的亲和力,而是取决于三联体的活性,而PROTAC的连接的构象和位点,连接链的长度和组成的修饰以及浓度等都会对三联体的活性产生影响,因此调控起来更加有难度。
就PROTAC浓度举例,PROTAC发挥药效必须与靶蛋白和E3酶形成有效的三元复合物,然后有实验显示【3】,当浓度高时,药物分子会与靶蛋白或E3酶分别形成二元复合物(hook effect)。
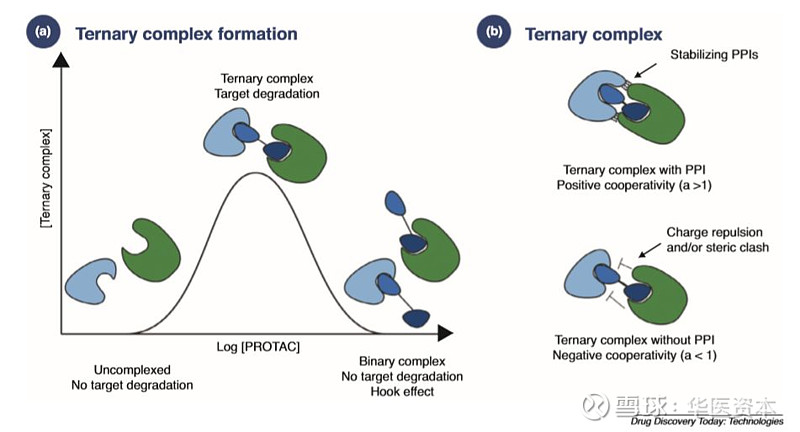
图片来源:文献【3】
另外,目前来看,E3和不同靶标蛋白的协同性不同,还没有显示出一般性规律。这就需要科学家不断设计差异化的PROTAC,以期获得高效降解的三元复合物。
3. 毒性及其检测
前文提到目前已有多项研究证明,基于多靶点抑制剂设计的PROTAC分子能与多个靶蛋白结合,但是降解的蛋白只是其中少数几个。然而目前整体来看,安全性还未得到完全的证实。而能靶向E3酶CRBN的度胺类药物(沙利度胺、来那度胺、泊马度胺)在上世纪五六十年代引起“海豹儿”的事故,还一直让人心有余悸。另外,不同于传统靶向蛋白活性的小分子,彻底降解蛋白的PROTAC会不会带来更严重的毒性,仍然需要时间来验证。
4. E3连接酶的小分子配体数量不够
目前人体内已被发现的 E3 连接酶有600 多种,但目前在已报道的 PROTAC 中涉及的E3 连 接 酶 常 用 的 只 有 MDM2 ( mouse doubleminute 2 homologue) 、cIAP1( cellular inhibitor ofapoptosis protein 1) 、CRBN( cereblon) 、VHL( vonHippel-Lindau) 等【5】,原因主要在于缺乏具有高亲和性、特异性的 E3 连接酶的小分子配体。
PROTACs技术会朝着什么方向继续发展?
耶鲁大学的Craig Crews教授(前文提到Arvinas的创始人)在2019年2月发表在DrugDiscovery Today:Technologies上的1篇综述【5】讨论了这一问题。
总体来说,会往以下这4个方向发展:优化PROTACs的设计、合成与评价,扩大可用E3泛素连接酶的范围,选择和验证靶点以及最终靶向无成药性的蛋白,也可以理解为克服前面提到的挑战。
目前的临床进展?
到目前为止已有 30 种以上与疾病发生发展至关重要的蛋白质进行了 PROTAC 的研究与报道,其中许多 PROTAC 显示出纳摩尔级别的降解效率。靶蛋白主要包括核受体,如 ER、AR、RAR;蛋白激酶,如 Akt、BCR-ABL、c-ABL、BTK、CDK9等;转录调节蛋白,如 BRD4、Sirt2、TRIM24、Smad3等。
走的最快的是AR和ER受体,Arvinas就这两个靶点的PROTAC治疗方法进入临床I期。
靶向AR的ARV-110于2019年3月26日正式开展I期临床试验,启动患者给药,用于治疗转移性去势抵抗性前列腺癌(mCRPC)患者。ARV-471也于2019年第三季度开始启动1期临床实验。ARV-471是一款口服雌激素受体(ER)PROTAC蛋白降解剂,用于治疗局部晚期或转移性ER+/HER2-乳腺癌患者。
2019年10月,Arvinas分享了两项1期临床试验的部分结果。ARV-110的3个剂量爬升组(35 mg,3名患者;70 mg,4名患者;140 mg,3名患者)中,没有观察到限制剂量的毒性反应(DLT),也没有观察到2级、3级、或4级的相关副作用,安全性佳。此外,在ARV-471(30mg)疗法中,也观察到了和剂量呈比例的暴露。
接下来,ARV-110会继续增加给药剂量。除了继续研究安全性和PK外,ARV-110的一期临床试验还将通过对患者前列腺特异性抗原(PSA)水平和RECIST的疗效展开进一步研究。
总体而言,这样的数据对于靶向蛋白降解领域来说,是另一个令人振奋的里程碑,在初步证明其安全性后,具体的疗效如何值得期待。
目前有多少公司在做PROTAC这个方向?
国外:布局PROTACs技术的初创公司中,研发进展最快的是Arvinas(目前两个临床I期药物)、C4 Therapeutics、Kymera Therapeutics(靶向IRAK4的蛋白降解剂预计在2020年上半年开展临床试验)等,除此之外还有Captor therapeutics、nutrix、Cellida、Vividion等。这些公司几乎都受到资本市场的追捧。
而大公司多以和小型Bio-Tech公司合作为主,包括基因泰克、辉瑞、阿斯利康、默沙东、安进、吉利德、勃林格殷格翰、葛兰素史克、新基、礼来、艾伯维、强生等等。
国内:布局PROTACs技术的初创公司有嘉兴优博、上海睿因(Cullgen)、成都分迪科技、和径医药、海创药业、加科思、科伦药业、石药集团等,都处于研究的早期阶段。
其中嘉兴优博属于PROTAC的第一梯队,拥有差异PROTAC蛋白降解TED平台。目前,嘉兴优博已经有1个药物准备进入临床前研究,预计融资后18个月申报IND。
PROTAC是否值得投资?
PROTAC是个值得关注的适合早期投资者的投资领域。
首先,我们看好PROTAC靶向降解蛋白领域。疾病治疗领域的空间广阔,市场巨大,未来可期。
其次,目前PROTAC技术处于快速成长中,适合早期赛道投资。目前的突破点还是首选一些经过验证的靶点,降低变量,证明PROTAC的可行性,未来有望直接靶向“不可成药”靶点
最后,我们认为投资标的选择标准主要为以下两个:
团队组成:因为涉及三联体的设计、合成和验证,所以需要资深化学、药学专家的加盟;需要有对泛素蛋白酶系统研究深度了解的科学家。
技术:自身有专利或者授权专利,不与现有国际专利形成冲突;有独特的平台技术,来解决目前PROTAC平台遇到的问题;差异化的管线品种(对适应症和靶点的选择)。
参考文献:
【1】PICKART C M.Mechanisms underlying ubiquitination[J]. Annu Rev Biochem, 2001, 70 (70) : 503-533.
【2】Neklesa, T. K., Winkler, J. D., & Crews, C. M. (2017). Targeted protein degradation by PROTACs. Pharmacology and Therapeutics, 174, 138-144.
【3】PROteolysis TArgeting Chimeras (PROTACs) - Past,present and future. Drug Discov Today Technol. 2019 Apr;31:15-27. doi:10.1016/j.ddtec.2019.01.002
【4】Taavi K. Neklesa a,⁎, James D. Winklera, Craig M. Crewsb.Targeted protein degradation by PROTACs. Pharmacology& Therapeutics 174 (2017)138–144
【5】CIECHANOVER A. Proteolysis: from the lysosome to ubiquitin and the proteasome[J].Nat Rev Mol Cell Biol,2005,6( 1) : 79-87.