$沃森生物(SZ300142)$ 今天沃森生物公告了mRNA变异株疫苗RQ3013的Ⅲb实验,我们来做下解读:整体的方案是三针灭活基础上再打一针RQ3013,对照组是智飞的重组蛋白疫苗、康希诺的腺病毒载体疫苗。

1、安全性
原文:IIIb期临床试验的安全性数据显示:试验组和两个对照组不良反应发生率以1级和2级为主,且主要发生在接种疫苗后的7天内;试验组和两个对照组不良反应症状主要为发热、接种部位疼痛、头痛,且以1级和2级为主;未发生与研究疫苗相关的严重不良事件(SAE)。本次IIIb期临床试验的安全性数据表明该疫苗具有良好的安全性。
解读:具体的发热率没有详细说,不过根据经验,应该是高于重组蛋白的发热率的,因为就发热率来说,第一代灭活最低,其次是重组和腺病毒载体,最高的是mRNA。mRNA疫苗的发热率是监管审批重点考虑的问题,考虑到这次疫苗进行了核苷酸化学修饰,理论上发热率应该不会比莫得纳和辉瑞差太多。

2、免疫原性
原文:序贯加强免疫后14天,RQ3013、对照疫苗1和对照疫苗2对Omicron BA.5的真病毒中和抗体阳性率分别为94.63%、67.68%和45.45%,RQ3013显著高于两个对照疫苗组。序贯加强免疫后14天,RQ3013、对照疫苗1和对照疫苗2对Omicron BA.5的真病毒中和抗体GMT(几何平均滴度值)分别为69.14、14.56和12.23,RQ3013 对Omicron BA.5的真病毒中和抗体GMT分别是对照疫苗1、对照疫苗2的4.75倍和5.65倍;序贯加强免疫后28天,RQ3013、对照疫苗1和对照疫苗2对Omicron BA.5的真病毒中和抗体GMT分别为123.2、65.96和55.46。上述数据表明,RQ3013疫苗序贯加强免疫后14天和28天对BA.5的真病毒中和抗体GMT均显著高于两个对照疫苗组,达到免疫原性评价的统计学优效标准。
解读:对BA5的效果来说,显著优于智飞的重组蛋白和康希诺的腺病毒载体疫苗(对照组疫苗),但是整体的水平可能不是太理想。主要是抗原设计的时候,这个疫苗没有把BA5包含进去。这里面李云春在全球健康研讨大会上也提到了,RQ3013对BA5的交叉保护效果比较差。
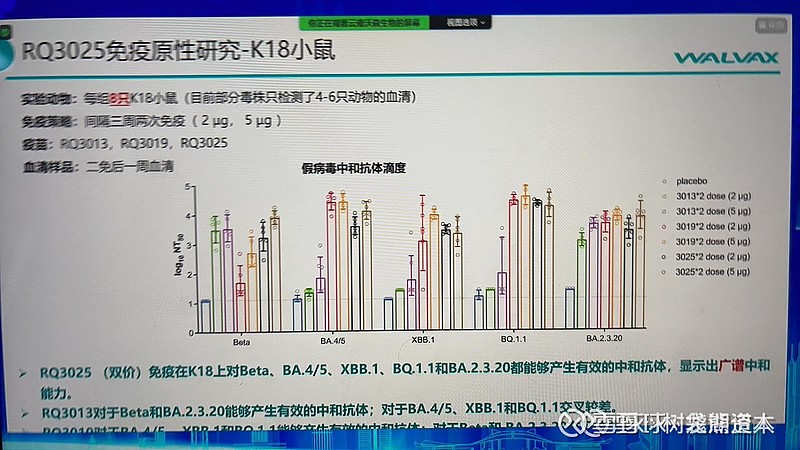
3、对Omicron变异株的保护效力
原文:序贯加强免疫7天后,对任何严重程度的有症状确诊新冠病毒感染所致疾病(COVID-19)的保护效力,RQ3013疫苗组均优效于两个对照疫苗组。
解读:具体的保护率也没说,不过根据经验,实际保护效率应该是优于智飞的重组和康希诺的腺病毒载体疫苗,重症率应该是没有、样本数量也小具体数据不太具备参考价值。
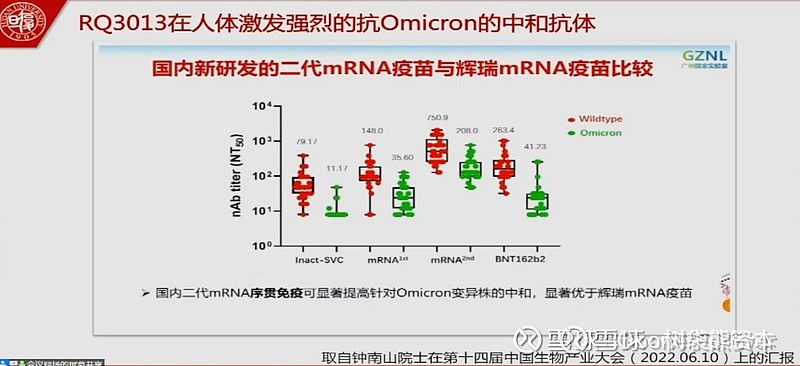
3、RQ3013与BNT2野生株的比较
之前就提到过,RQ3013中和抗体是辉瑞BNT的野生株的4倍左右。
4、下一代广谱mRNA疫苗RQ3025
沃森生物和蓝鹊生物复旦大学合作的下一代广谱mRNA疫苗RQ3025,对当前流行的BA5以及XBB都具有很好的广谱性中和效果。

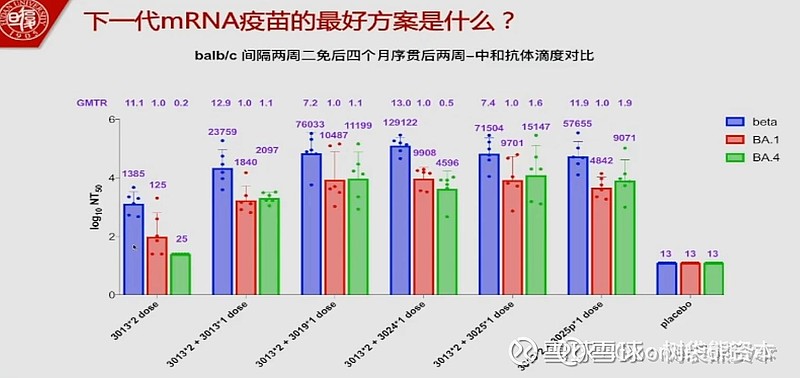
从这个图中可以看出,序贯实验中,RQ3025对BA4的中和效果是RQ3013的7倍左右,所以下一代RQ3025效果是比较突出的(第五个:2针3013+1针3025,2097VS15147),应对当前的BA5和即将到来的XBB是没问题的。
5、结论
总体来看,从非劣效实验来看,相较于智飞的重组蛋白疫苗和康希诺的腺病毒载体疫苗,对BA5来说,RQ3013优势还是比较明显的,具备获批的基本条件。但是,要应对BA5和即将到来的XBB,RQ3013还是不够的。
RQ3013最大的意义是要把技术路线走通,获批后再在RQ3013基础上迅速升级迭代到3025广谱疫苗。类似于神州细胞的重组二价疫苗先批准、四价疫苗再迭代升级,逻辑应该是一样的。
附录:林教授对RQ3013的解读——