$复宏汉霖(02696)$ 作为一家国际化的创新生物制药公司,复宏汉霖致力于为全球病患提供质高价优的创新生物药,产品覆盖肿瘤、自身免疫性疾病、眼科疾病等领域。
8月18日,复宏汉霖公布了2021年上半年度业绩。财报数据显示,上半年复宏汉霖实现营业收入6.336亿元,较去年同期增长474%,主要来自多款产品陆续商业化带来的销售收入、向客户提供的研发服务及授权许可收入。其中,汉利康(利妥昔单抗)获得销售净利润分成2.222亿元(汉利康由江苏复星团队负责销售);另一重磅产品汉曲优(曲妥珠单抗,欧盟商品名:Zercepac)于中国和欧盟实现销售规模稳健增长,共计实现境内收入2.876亿元,境外收入3770万元;自身免疫疾病领域治疗产品汉达远(阿达木单抗)获得销售净利润850万元(汉达远由江苏万邦团队负责销售),并实现授权许可收入220万元。
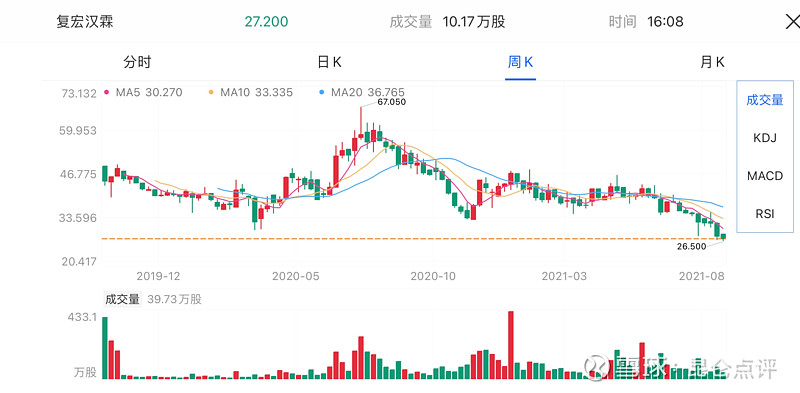
复宏汉霖港股走势图(下图)
在全速推进产品全球商业化的同时,以未满足的临床需求为导向,持续加码创新,2021上半年,复宏汉霖4项临床试验取得重要进展、4个产品于全球范围内获得多项临床试验批准,上半年公司研发开支约为人民币7.393亿元。截至目前,公司已累计在全球范围内获得超过40项临床试验批准,在中国、欧盟、美国、澳大利亚、乌克兰、菲律宾和土耳其等国家和地区开展共计20多项临床试验。
产品介绍
复宏汉霖已有3个产品成功上市,3个产品获得上市注册申请受理,11个产品、8个联合治疗方案在全球范围内开展20多项临床试验。其中,公司首款重磅产品汉利康(利妥昔单抗)为首个获批上市的国产生物类似药。第二款产品汉曲优(曲妥珠单抗,欧盟商品名:Zercepac)为首个中欧双批的国产单抗生物类似药,开辟了中国医药企业参与单抗生物类似药“世界杯”比赛的先河,有望为全球HER2阳性乳腺癌和胃癌患者带来更多的治疗选择。此外,斯鲁利单抗(抗PD-1单抗)、HLX04贝伐珠单抗及HLX01利妥昔单抗类风湿关节炎新适应症的上市注册申请正在审评中。
管线布局:研、产双轨齐头并进
复宏汉霖产品管线(下图)
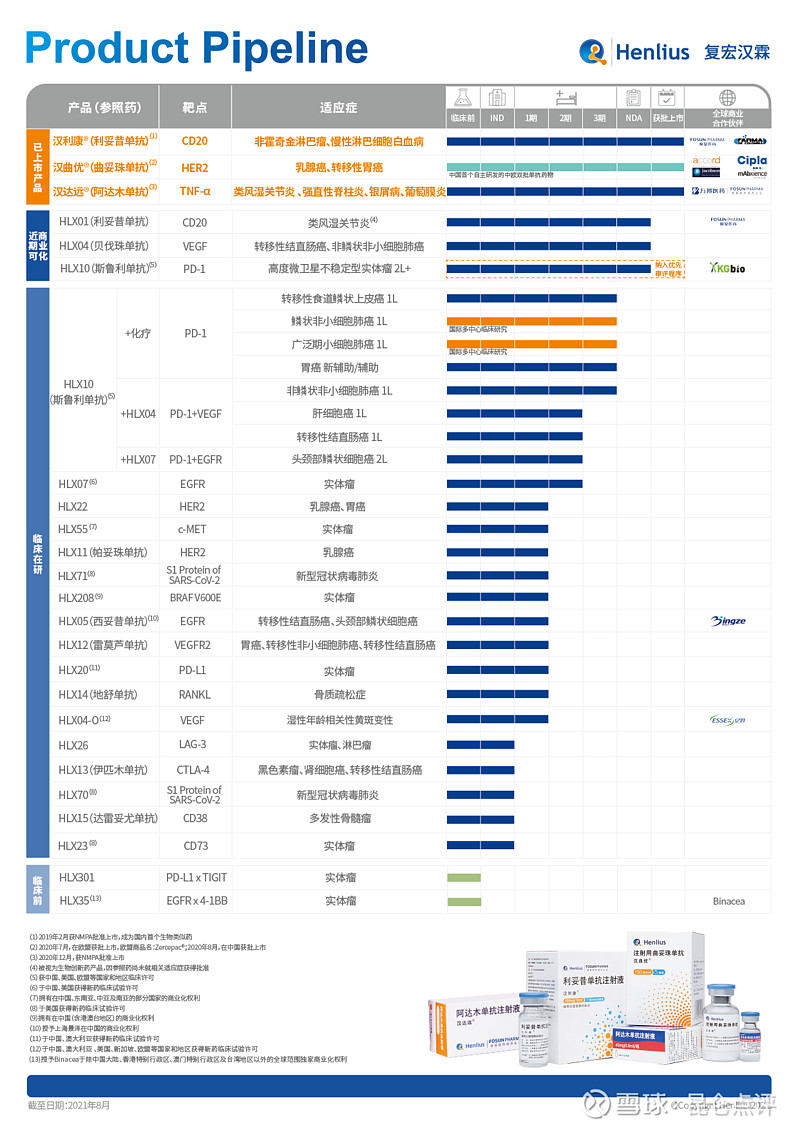
1.汉利康:启动新规格供货,临床应用多方受益
自汉利康上市以来,在安全性及疗效比肩原研药的前提下,凭借合理的价格让过往无法负担原研药的患者可以选择继续治疗,并在新患者的使用比例中超过50%。2020年汉利康在原有的非霍奇金淋巴瘤适应症基础上获国家药监局批准增加滤泡性淋巴瘤和慢性淋巴细胞白血病两项适应症,使得药物涵盖适应症增长至五项,成功扩大患者覆盖群体。在规格方面,汉利康2020年获批500mg/50ml规格,在2021年启动新规格供货,给患者及医生提供更多的选择并有望降低单剂成本。
2.汉曲优:中欧双线布局,渠道推向世界
复宏汉霖对汉曲优(曲妥珠单抗,欧盟商品名:Zercepac)的规划便是面向世界,从一开始的中欧双线布局开始,逐步把药物推向全球,不断取得阶段性成就。汉曲优(曲妥珠单抗,欧盟商品名:Zercepac)为公司抗肿瘤治疗领域的核心产品,于2020年7月和8月相继获得欧盟委员会(EC)与国家药监局(NMPA)批准上市,用于HER2阳性乳腺癌和胃癌的治疗。
在国内方面,目前汉曲优(规格:150mg)已实现中国境内全部省市的招标挂网和医保准入,其中在中国新增60mg规格的补充申请(sNDA)已于近期获得NMPA正式批准上市。值得关注的是,生物类似药和汉曲优分别被纳入2021年新版中国临床肿瘤学会(CSCO)乳腺癌诊疗指南及2021年新版中国临床肿瘤学会(CSCO)胃癌诊疗指南,标志着汉曲优获得了权威医学指南的认可,随着销售网络和队伍的持续扩增,2021下半年汉曲优在中国境内市场的推广有望加快推动,拟于年内遍及全国约390个城市,覆盖DTP药房/医院近4500家。
在海外方面,继Zercepac(规格:150mg)2020年7月在欧盟获批上市后,公司也加快推动该产品不同规格在欧盟的上市进度,2021年4月和6月,60mg及420mg新规格分别获批上市,有望为当地患者提供更多剂型选择和灵活的组合用药方案。复宏汉霖持续联合Accord积极推进Zercepac在欧盟的商业化进程,截止目前,该药已于英国、德国、西班牙、法国、意大利、爱尔兰、匈牙利等近20个欧洲国家和地区上市。2021年7月,Zercepac(规格:150mg)的上市申请进一步获得瑞士药品监督管理局批准。今年1月,复宏汉霖更是和Accord的母公司Intas达成在美国及加拿大地区商业化Zercepac的协议,使得产品渠道全面覆盖欧美主流生物医药市场,逐步走向全球。
3.汉达远:完成主要省市挂网,新增补充适应症
阿达木单抗汉达远是复宏汉霖首款治疗自身免疫疾病的产品,用于类风湿关节炎、强直性脊柱炎和银屑病的治疗。自2020年12月获批上市以来,复宏汉霖积极实现渠道建设,截至目前已完成国内27个省市挂网。今年4月,汉达远治疗非感染性葡萄膜炎适应症的补充申请获批,成功将产品适应症增加至4项。
4.创新斯鲁利单抗:以患者需求为核心,泛癌种治疗适应症即将面世
复宏汉霖将推动第一个创新产品PD-1抑制剂斯鲁利单抗、贝伐珠单抗及利妥昔单抗RA适应症等多款产品陆续上市。斯鲁利单抗为复宏汉霖自主研发的创新型抗PD-1单抗,不同于市面上现有的PD-1产品,斯鲁利率先就高度微卫星不稳定型(MSI-H)实体瘤适应症进行申报,其上市注册申请已于2021年4月获NMPA受理并被纳入优先审评审批程序,有望成为国内首个治疗MSI-H实体瘤的抗PD-1单抗。除MSI-H实体瘤外,该产品另一大特色即是适应症覆盖广泛。目前公司已针对产品的10项免疫疗法在全球多个国家和地区开展了临床试验,全面覆盖肺癌、转移性结直肠癌、胃癌等高发大瘤种,并为产品积累了丰富的国际临床数据。根据复宏汉霖半年报业绩披露,公司计划于2021年下半年就sqNSCLC适应症向NMPA递交NDA。
5.HLX04 &HLX01-RA:差异化开发,进一步扩充公司适应症覆盖
除斯鲁利单抗外,公司HLX04(贝伐珠单抗)和利妥昔单抗类风湿关节炎适应症(HLX01-RA)也有望最快于2021年底或2022年获批上市,成为公司第四/五款获批上市的单抗生物药,覆盖转移性结直肠癌及晚期、转移性或复发性非小细胞肺癌和类风湿关节炎,惠及更多患者群体。基于原研贝伐珠单抗于2020年在中国新增脑胶质瘤(GBM)适应症,公司计划于该产品上市后启动新增该适应症的sNDA。
6.积极扩充管线,布局新一代潜力靶点
围绕LAG-3、CD38、CD73等多个免疫热门靶点,复宏汉霖已同步开展前瞻性布局,加速推动靶点产品全部进入临床研究阶段。纵观公司的产品管线,包括HLX301(PD-L1×TIGIT)、HLX35(EGFR×4-1BB)在内的双抗及ADC等多款产品的临床前研究也正在积极推进。
从患者需求出发,复宏汉霖2021上半年在创新研发上不断精进,加速扩充创新潜力靶点、双靶点抗体平台、抗体偶联药物(ADC)产品,持续完善创新管线。
2021年5月,复宏汉霖自润新生物引进创新产品BRAF V600E抑制剂,加速公司多元化创新的重要战略布局,增强产品靶点和种类多样性。目前该产品处于临床I期,早期临床研究结果显示,产品副作用低且展现出初步疗效,并有潜力与公司自有管线中抗EGFR/PD-1单抗产品产生协同效应。
公司团队介绍
公司首席执行官总裁张文杰先生先后担任拜耳制药工程全球市场部副总、拜耳先灵医药亚太总部业务发展部负责人、美国安进公司中国区总经理,2019年3月加入复宏汉霖,在医药行业拥有逾25年的商业运营经验。其他管理层人员均具有硕士及以上学历,具有超过15年以上的医药行业从业经验。
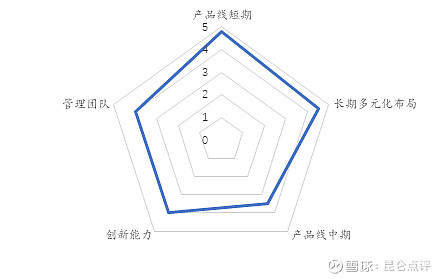
公司总体竞争力