
OncoC4的两位创始人在讲述产品开发计划时,着重强调了ONC-392作为单药开发的潜力。
作为一个研究历史已超过20年的“老”靶点,CTLA-4的风头一度被PD-1/L1覆盖。但随着肿瘤双免治疗时代到来,CTLA-4抗体的研发和交易热度,又开始不断攀升。
与此同时,二代CTLA-4抗体开始从幕后走向台前。它们能否让CTLA-4抗体重回肿瘤免疫的主角位置?
重塑CTLA-4单药开发前景
日前,CTLA-4抗体收获一项交易大单:BioNTech宣布与OncoC4(昂科免疫)达成协议,合作开发后者的新一代CTLA-4抗体ONC-392。根据协议,BioNTech将为此支付2亿美元预付款,未来还有里程碑付款和双位数比例的销售提成。
BioNTech在新闻稿中提到,其将与OncoC4合作开发ONC-392单药或与PD-1/PD-L1抗体联用方案,同时BioNTech还表示将独立负责ONC-392与抗PD-1药物以外产品的组合疗法开发。
研发客就此采访了OncoC4创始人刘阳教授和郑盼教授。在讲述产品开发计划时,他们着重强调ONC-392作为单药开发的潜力。
高昂的交易费用、单药开发的策略,似乎都暗示CTLA-4重新崛起的苗头。
据公司新闻稿,ONC-392单药治疗PD-1/PD-L1抑制剂耐药的转移性非小细胞肺癌,已于去年4月获FDA快速通道认证。除此以外,从Clinicaltrial.gov上查找到的信息,ONC-392还在卵巢癌、胰腺癌、三阴性乳腺等多种不同肿瘤患者队列中探索单药使用效果。

OncoC4创始人 刘阳(左)和郑盼
刘阳和郑盼告诉研发客OncoC4公司名称的来历:Onco是“肿瘤”的英文缩写,同时公司一直针对CD24和CTLA-4两个靶点开发新药,就选取它们的共同部分C4作为后缀。其中C4还隐含突破创新的含义。C4是一种炸药的名称,寓意OncoC4研发的产品也能摧毁肿瘤,成为重磅炸弹。
提起CTLA-4抗体,单药治疗方案开发可能是制药界的一大痛处。根据已有的临床数据,CTLA-4抗体抗肿瘤作用显著,但用药安全窗口甚窄。
因此,相关产品的研发经历也颇为坎坷。全球迄今获批的CTLA-4单抗仅有两款,包括2011年获批的BMS的Yervoy(ipilimumab)和2022年获批的阿斯利康的替西木单抗(tremelimumab)。其中,仅Yervoy治疗晚期黑色素瘤一项获批单药使用适应症,其他适应症均需两药甚至多药联用。也正因此,在PD-1抑制剂获批之后,CTLA-4抗体更多被视为联合用药的搭配角色。
而ONC-392敢于碰触这样的“硬骨头”,正是基于刘阳和郑盼团队在基础研究方面的新发现。
他们带头挑战了CTLA-4的传统疗效机理,认为CTLA-4起效并非类似PD-1那样直接松开其与T细胞表面配体结合的免疫“刹车”。另外,该团队也利用实验数据,否定了CTLA-4疗效与副作用间的线性关系。
他们在发表的论文中提到,CTLA-4抗体发挥作用,是通过强ADCC(抗体依赖的细胞介导效应)来清除肿瘤局部高表达CTLA-4的Treg细胞,从而降低Treg对杀伤性T细胞的抑制;而副作用是由于抗体与CTLA-4的结合体在内吞后被溶酶体清除,导致细胞表面CTLA-4大量减少引发自免反应。
由此阐明CTLA-4抗体的疗效和毒性是可以分离的,只要筛选出的抗体既能在细胞外与CTLA-4结合,又能在进入细胞后自动松开二者的捆绑,就能避免CTLA-4被溶酶体降解,降低治疗毒性,这也是ONC-392的设计基础。另一方面,避免CTLA-4降解也能保持肿瘤局部Treg细胞的CTLA-4高表达,增强抗体杀伤调节性T细胞的能力从而提高疗效。
刘阳表示,在肿瘤治疗领域获得这样一举两得的机会,利用同一机理既能提高疗效又能降低毒性,还是比较少见的。“基于这个机理,ONC-392的治疗窗口就能明显扩展,用药剂量和时间也可大幅提升,这都成为CTLA-4单药使用的基础。”
“Treg派”需更多临床数据支持
刘阳团队提出的新作用机理,事实上在二代CTLA-4抗体研发中已有不少跟随者,市场将它们统称为“Treg派”。在CTLA-4抗体合作交易中,类似设计的产品愈发成为焦点。
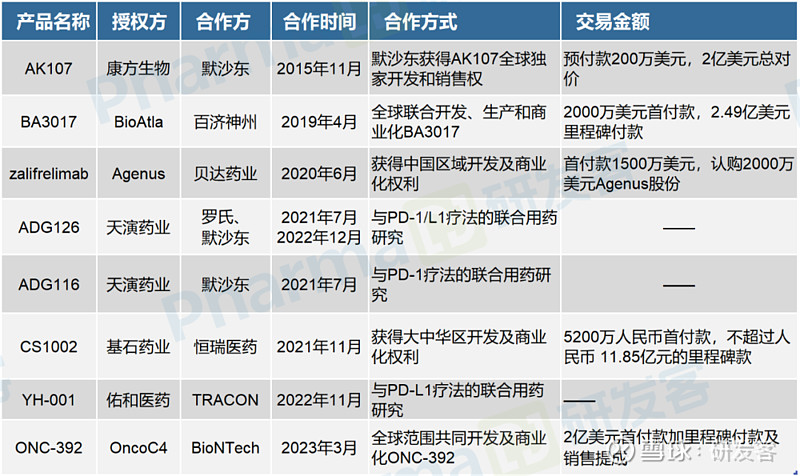
梳理近年产生的与CTLA-4抗体相关的合作或交易可发现,华人科学家创立公司参与的就有近10项,既有产品引进也有对外授权,亦有产品联合用药的合作研究(详见下表)。
(点开看大图)
在这些产品中,康方生物的AK107以及贝达药业引进的zalifrelimab,实际开发时间早于“Treg细胞清除”理论提出时间。而后期开发的天演药业的ADG126和ADG116、佑和医药的YH-001、基石药业的CS1002,在对外公布的作用机理中,都提到与抑制Treg细胞活性有关,这类产品已占据上述交易合作的半壁江山。
作为CTLA-4抗体研发的先驱,BMS也有两款产品BMS-986288 、BMS-986218的机理与清除Treg细胞有关,目前均处于临床研发当中。
但要下定论未来“Treg派”能在CTLA-4抗体市场竞争中取得优势地位,可能为时尚早。目前多数产品尚未从大型临床研究中获得数据,验证产品的安全性及有效性,尤其这类产品最终能否在临床治疗中作为单药使用,仍存在较大不确定性。
有一部分研究者仍然支持CTLA-4靶点原先的作用机理,并在抗体改造中采用“抗体前药”设计,使其仅在肿瘤微环境中条件性激活,从而降低对肿瘤以外组织的影响。BMS另一款正在开发的产品BMS-986249,正是基于该作用机理。
从目前有限的临床研究结果和Ⅱ期研究推荐给药剂量(RP2D)的数据看,ONC-392还是取得了一些突破。
在2021年召开的SITC大会上,OncoC4海报展示了ONC-392单药的Ⅰ期研究结果,在剂量爬坡阶段参与的10名患者中,有一例非小细胞肺癌患者和一例卵巢癌患者出现疾病完全缓解(CR);同时确定了ONC-392单药治疗的RP2D剂量为10mg/kg,每三周一次。
而在2022年召开的SITC大会上,OncoC4又公布了ONC-392与默沙东PD-1抑制剂Keytruda(pembrolizumab)联用的剂量爬坡研究结果。在10名可评估患者中,3人部分缓解(PR),6人疾病稳定(SD),1人疾病进展(PD)。目前已确定的RP2D剂量是6mg/kg的ONC-392与200mg的pembrolizumab联用。
由上可见,ONC-392不论是单药治疗还是联合用药研究中采用的剂量,均高于已上市的CTLA-4抗体ipilimumab。同时,新闻稿中提及ONC-392可在整个研究期间连续给药,目前有患者最长用药时间超过一年,反映出ONC-392对CTLA-4抗体安全性的提升。
从BioNTech与OncoC4的这项交易看,其还可能有利于拓宽CTLA-4抗体在肿瘤免疫治疗中的探索边界,这也是该交易的独特之处。
以往参与CTLA-4抗体合作交易的参与方之一,通常都手握PD-1/L1抑制剂,它们获得CTLA-4抗体后的研究意图也更局限于与PD-1/L1抑制剂开展联用研究。而BioNTech产品线布局的产品类型新颖且涉及面广,包括mRNA肿瘤疫苗、细胞治疗及双抗产品等,未来BioNTech有望启动全新角度的研究探索。
未来这项交易能否帮助CTLA-4带领“Treg派”突出肿瘤免疫产品重围,让CTLA-4抗体成为摧毁肿瘤的“C4炸药”,让我们拭目以待。
采访 | 王星月
编辑 | 姚嘉 yao.jia@PharmaDJ.com
总第1847期
访问研发客网站可浏览更多文章