作者:慧博智能投研
阿尔茨海默病行业深度:治疗现状、竞争格局、市场空间及相关公司深度梳理
我国将逐步迈入老龄化社会,而庞大的老龄人口将对中国的医疗产业提出更高的要求。人口快速老龄化,带来的一个主要疾病就是阿尔茨海默症,患者在认知、记忆、自主行为等能力上会出现持续衰退。国内阿尔茨海默病市场需求旺盛,国内已有至少983万AD患者,随着人口老龄化的发展,国内AD患者数量也将维持增长态势。一方面阿尔兹海默症从病理改变到临床症状出现周期跨度较久,提前诊断和预防逐渐得到重视;另一方面阿尔茨海默病的药物研发已有单抗药物成功上市,血液测试亦将写入指南,AD领域终将实现治疗和诊断领域的双突破。
那么,什么是阿尔茨海默病,有着怎样的发病机制,国内治疗现状如何,有哪些诊断方法以及药物对于治疗阿尔茨海默病是行之有效的,治疗及诊断方面的市场空间有多大,相关公司又有哪些?通过阅读下文我们来逐一了解。
目录
一、阿尔茨海默病概述 1
二、阿尔茨海默病发病状况 6
三、阿尔茨海默病诊断 9
四、阿尔茨海默病药物治疗 13
五、阿尔茨海默病药物研发市场竞争格局 23
六、阿尔茨海默病非药物治疗 25
七、阿尔茨海默病行业市场空间 26
八、相关公司 28
九、参考研报 31
一、阿尔茨海默病概述
1.阿尔茨海默病(AD)
痴呆(dementia)是由于脑功能障碍而产生的获得性和持续性智能障碍综合征,变性病性痴呆是指大脑出现退行性病变的痴呆类型。
阿尔茨海默病(Alzheimer's disease,AD)属于变性病性痴呆,患者数量约占痴呆的60~70%。AD的显著特征是β-淀粉样蛋白和Tau蛋白在大脑中积聚到阻碍正常认知功能,通常表现为记忆、抽象思维、判断、行为和情绪的变化,并最终干扰对身体的物理控制。

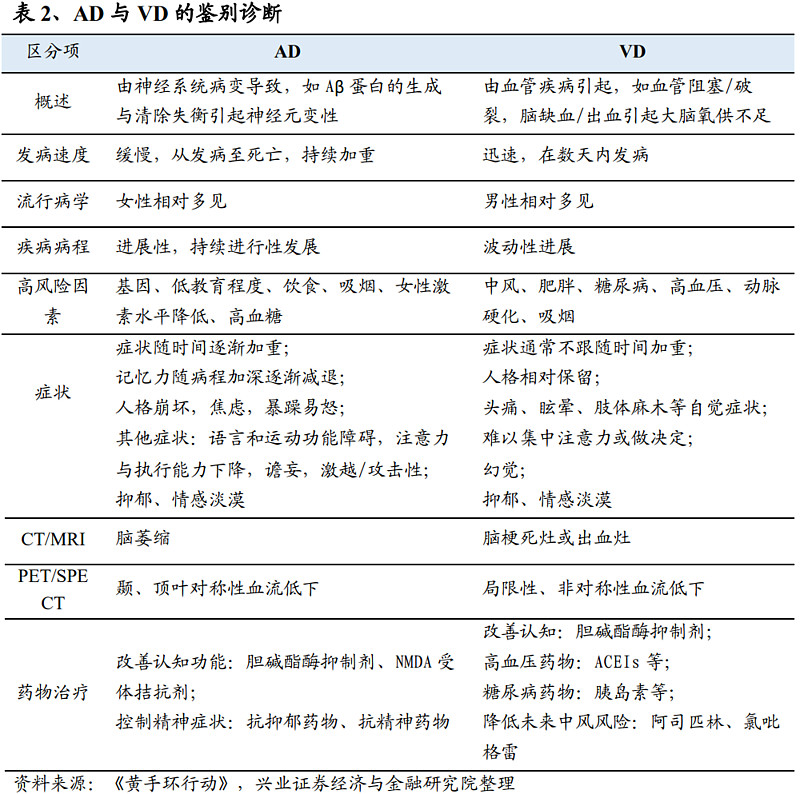
阿尔茨海默病和血管性痴呆的早期症状鉴别比较容易,到晚期鉴别比较困难。二者发病机制不同,AD由神经系统病变导致,而VD与血管疾病引起,此外两类患者在发病速度、流行病学、发展进程、高风险因素、症状和治疗方面仍有所差异。
2.阿尔茨海默病病因
早在1906年,德国精神病学家阿洛伊斯·阿尔茨海默(Alois Alzheimer)就公布了其发现的第一例阿尔茨海默病患者,该病以他的名字命名。但人们只知道AD是一种导致大脑细胞退化的疾病,其特点是思维能力和个人日常活动独立性下降。随着研究的深入,AD被认为是一种多因素疾病:作为AD的病因,主要有2种假说:Aβ假说和Tau蛋白假说。此外,年龄增长、遗传因素、头部受伤、血管疾病、感染和环境因素等多种危险因素也在该疾病中发挥作用。
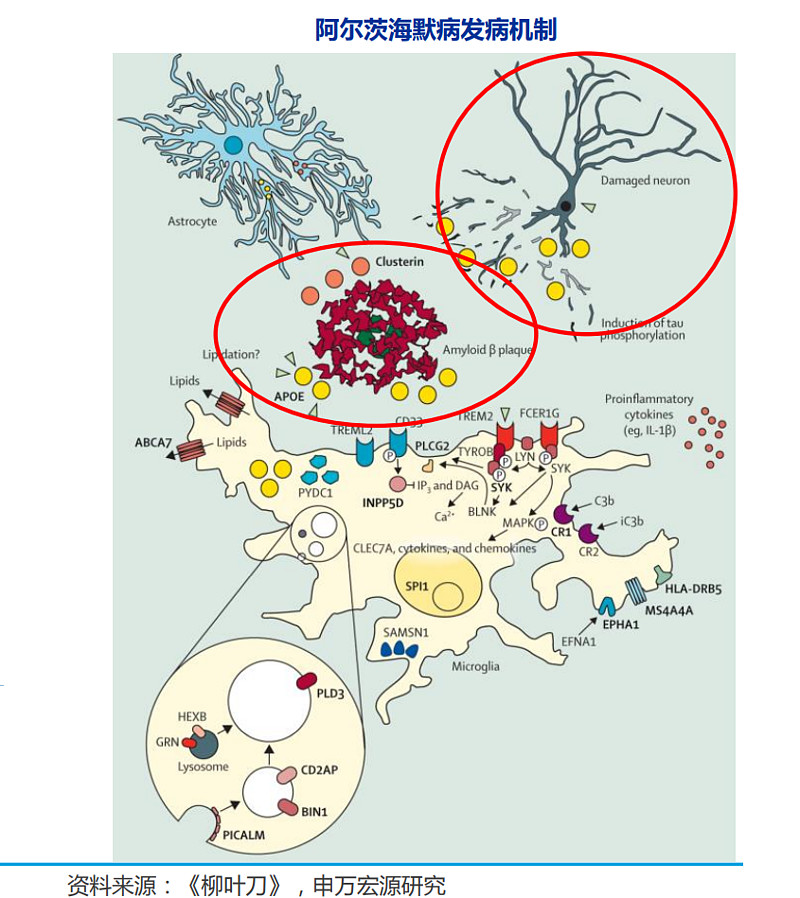
AD患者大脑呈现弥漫性脑萎缩,镜下以淀粉样斑块、神经元纤维缠结、神经元减少为主要病理学特征。
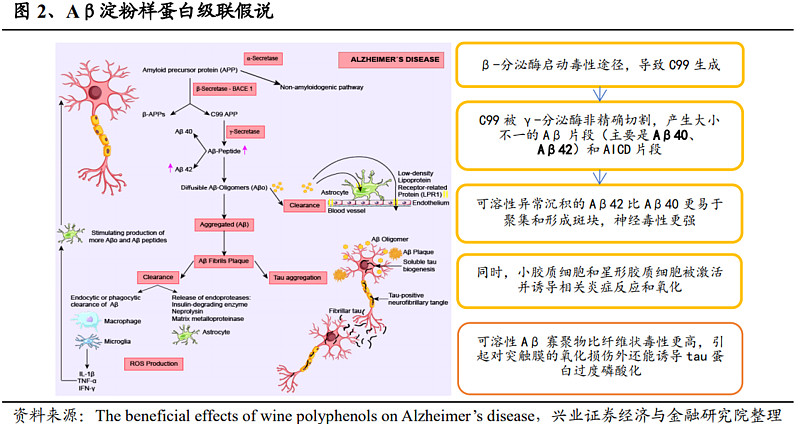
(1)Aβ假说
细胞外β淀粉样蛋白(Aβ蛋白)是由淀粉样前体蛋白(APP)通过分泌酶(包括β和γ分泌酶)裂解产生,在大脑中沉积和积累,导致淀粉样斑块(俗称老年斑)的形成,从而引起大脑中神经元和突触毒性,这种神经元的损伤和死亡会进一步影响患者的记忆和认知。
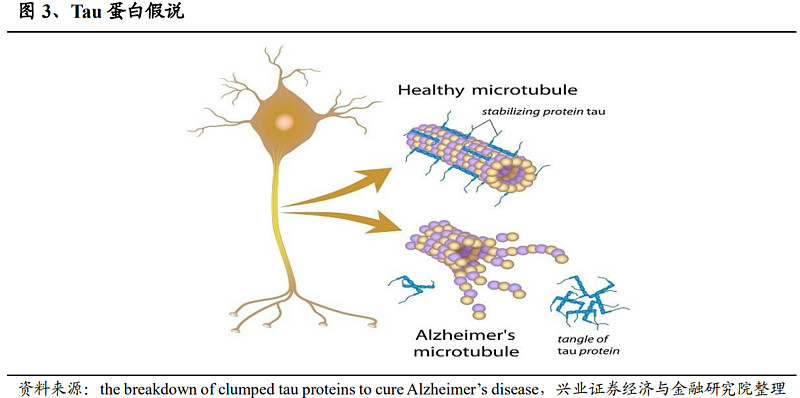
(2)Tau蛋白假说
神经元纤维缠结(Neurofibrillary Tangles ,NFTs)的主要组分为高度磷酸化的Tau蛋白。Tau是一种高度可溶微管相关蛋白,主要在大脑部分表达。胞内异常磷酸化的Tau蛋白,由可溶转变为不可溶同时高度聚集,丧失与微管蛋白结合促进微管稳定的活性,使微管解聚、轴突运转出现障碍,进而导致神经元变性,引起神经细胞的凋亡。
(3)其他假说
其他机制还包括基因突变假说、胆碱能损伤假说、氧化应激假说、神经炎症假说、雌激素缺乏假说、传染病假说、肠道微生物群破坏假说和自噬缺陷假说等,诸如此类的机制也为AD的干预提供了新颖的治疗方案。
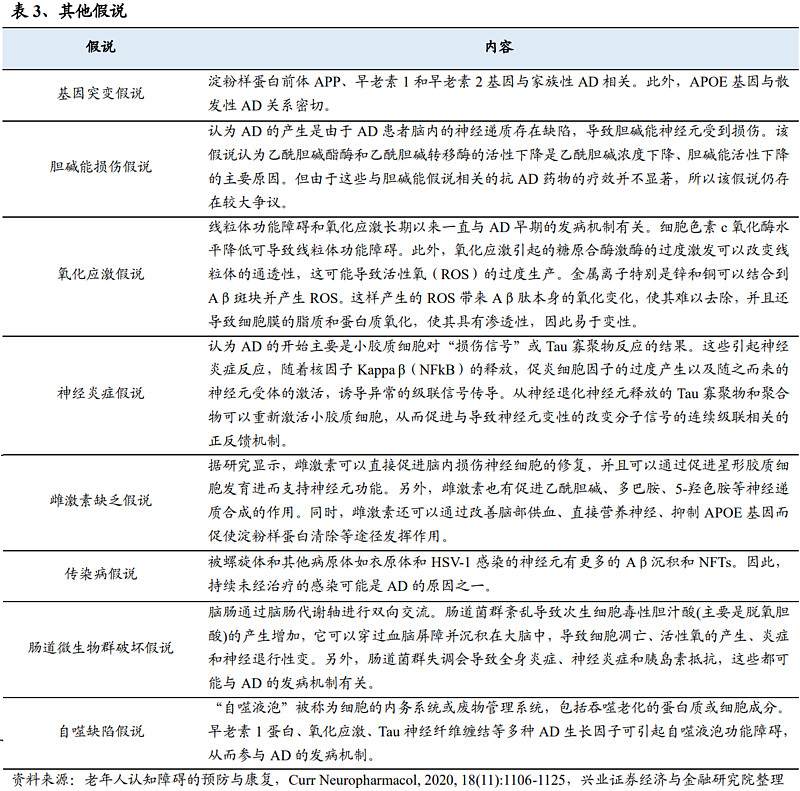
目前主流假说是Aβ蛋白生产和清除失衡,诱导Tau蛋白过度磷酸化、炎症反应、神经元死亡等一系列病理过程。
3.阿尔茨海默病临床分期
AD病程可达12年,早诊断及治疗助于延缓疾病进展。AD的临床表现通常包括多个方面,这些表现会随着病情的进展而逐渐加重。根据AD协会数据,AD连续体存在三个主要阶段,即临床前阿尔茨海默病、阿尔茨海默病引起的轻度认知障碍(MCI)和阿尔茨海默病引起的痴呆(也称为阿尔茨海默病痴呆)。阿尔茨海默病痴呆阶段进一步分为轻度、中度和重度痴呆:
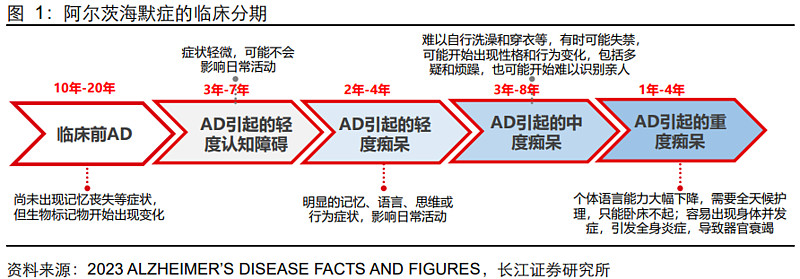
(1)第一阶段(1~3年)轻度痴呆期
具体表现为1)记忆力下降,特别是对最近发生的事情的遗忘明显;2)判断力减弱,患者难以进行事件分析、思考和做出判断,处理复杂问题的能力下降;3)在工作或家务劳动方面表现出漫不经心,无法独立完成购物和财务事务等,社交方面也遇到困难;4)尽管仍然能够完成一些熟悉的日常工作,但对新的事物感到迷茫,情感变得淡漠,偶尔会表现出兴奋或多疑的情绪;5)时间定向能力受损,患者仍能够识别自己所处的地点和人物,但难以准确定位自己在地理空间上,视觉空间能力对复杂结构的理解有困难;6)语言表达词汇减少,命名困难等。
(2)第二阶段(2~10年)中度痴呆期
具体表现为1)记忆严重衰退,对远和近期记忆受到严重影响,简单的空间认知能力下降,时间和地点的辨识困难;2)在问题解决、事物的相似性和差异性辨别方面存在严重障碍;3)需要协助进行户外活动,穿着、个人卫生和外貌维护方面需要协助;4)数学计算能力受损;5)出现各种神经症状,例如失语、失用和失认;6)情感状态由淡漠逐渐转为焦躁和不安,常常不停地走动,可能出现尿失禁等。
(2)第三阶段(8~12年)重度痴呆期
具体表现为患者已完全依赖照顾者,记忆严重受损,仅保留片段性记忆;无法独立进行日常生活,出现大小便失禁,呈现肢体僵硬,体检时出现锥体束征阳性,表现出强握、摸索和吸吮等原始反射。最终陷入昏迷,通常是由于感染等并发症导致的死亡。
二、阿尔茨海默病发病状况
1.全球发病情况
国际阿尔茨海默病协会网站显示,每3.2秒钟全球有1人罹患痴呆。2019年,全球已有5,520万痴呆患者,按照联合国人口预测进度,到2030年,痴呆患者数量预计将攀升至7,800万,2050年将至1.39亿。痴呆是全球残疾损失生命年的主要原因之一,经济负担重。2015年,全球痴呆年总花费8,180亿美元,相当于全球GDP的1.09%。2019年已达1.3万亿美元,根据测算,2030年预计将达2.8万亿美元。

2.国内发病情况
(1)中国AD及痴呆负担高于全球平均水平,老龄化趋势下负担愈重
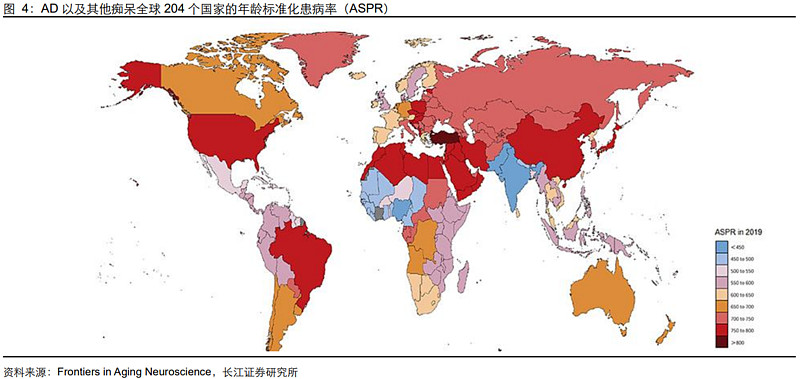
根据弗若斯特沙利文统计,2020年我国共有1,250万AD患者,随着中国人口老龄化,中国AD患者人数正在逐渐增加,预计到2025年,将有1,550万AD患者,2030年进展趋势加速,AD患者将进一步增至1,950万人。根据《中国阿尔茨海默病2022报告》,2019年我国AD年龄标化患病率为788.3/10万人,因AD的死亡顺位在1990年处于第10位,20年后已跃升至第5位,年龄标化死亡率为23.3/10万人。2019年全球AD年龄标化患病率为682.5/10万人,年龄标化死亡率为22.9/10万人。
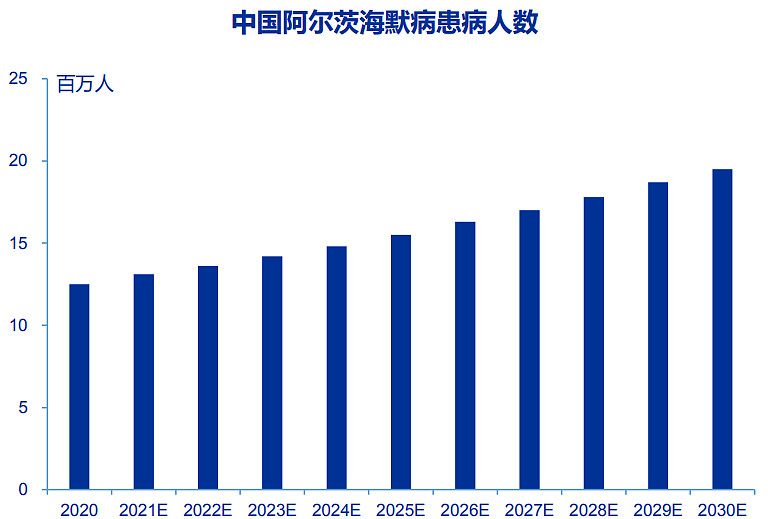
总体而言,我国AD以及其他痴呆的患病率、发病率以及死亡率均高于全球平均水平,在老龄化趋势下,疾病负担将进一步加重。
(2)我国人群AD知晓率较高,但主动就诊率较低
根据一项名为《2022年中国阿尔茨海默病知晓与需求现状调查》的线上问卷调查,20671名成年人调查样本中阿尔茨海默病的总知晓率为95.9%,而主动愿意去医院就诊的比例只有12.9%,其中农村居民和低学历居民主动就诊愿望明显较低。
(3)国内AD患者支付意愿跟水平并不低
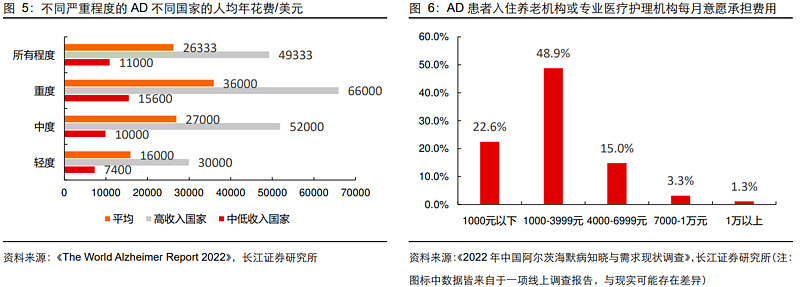
与此同时,国内AD患者支付意愿跟水平并不低。根据《The World Alzheimer Report 2022》,中低收入国家AD人均年花费大概在11000美元,其中轻中度患者花费大概在7400-10000美元之间(折合人民币约为5.4万-7.3万元),包括药物支出和护理支出。另外,根据《2022年中国阿尔茨海默病知晓与需求现状调查》,接近50%的调查对象愿意为入住专业护理机构付出月费用在1000-3999元,年均费用在1.2万-4.8万元之间。
三、阿尔茨海默病诊断
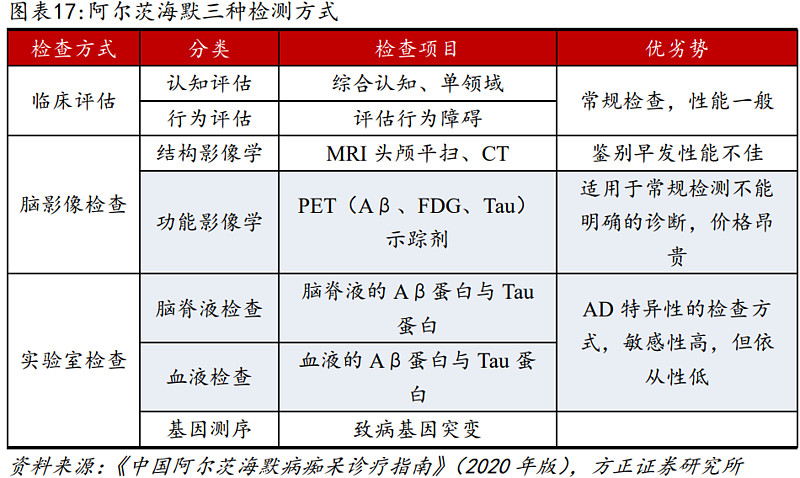
根据《中国阿尔茨海默病痴呆诊疗指南》,目前针对阿尔茨海默的检查主要有临床评估、脑影像学检查和实验室检查三种方式,临床评估作为常规检查,性能一般,目前全球主流诊断方式是脑影像检查技术与实验室检查联合诊断。
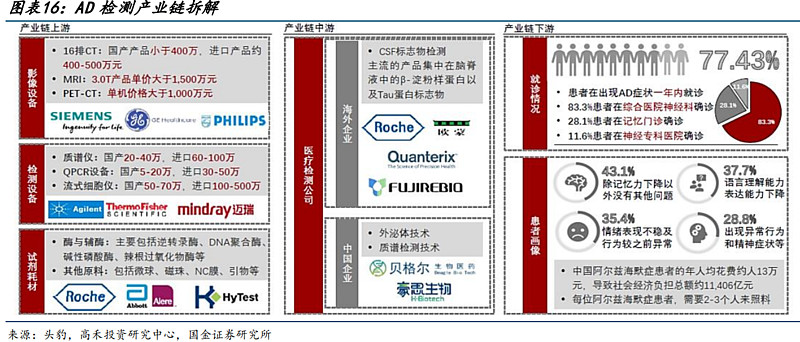
目前AD主要诊断方法为联合诊断。对于有疑似痴呆的患者,首先进行认知功能评估,并且进行常规的CT和MRI等影像学检查。目前用于辅助AD诊断的生物标志物主要分为影像标志物和体液标志物。AD诊断产业链上游包括影像设备、检测设备及试剂耗材供应商,中游为医疗检测公司,下游主体为AD患者。
1.脑影像学检查
脑影像学检查分为结构影像学及功能影像学。根据中国阿尔茨海默病痴呆诊疗指南(2020年版)推荐意见,各个标志物用于鉴别AD性能有差异。

2.AD实验室检查
根据《中国阿尔茨海默病痴呆诊疗指南(2020年版)》数据,AD实验室检查分为脑脊液检查、基因检测以及血液检查。
(1)脑脊液检查
CSF标记物有较高的诊断准确性,如临床前期或MCI阶段,准确诊断最困难,此时CSF生物标志物尤其有价值。在MCI期的敏感度和特异性可达85-90%,可作为AD痴呆期的诊断标志物。

(2)基因测序
许多研究表明,阿尔茨海默症与一些特定的基因变异有关。《2018中国痴呆与认知障碍诊疗指南》指出,有明确痴呆家族史的痴呆患者应进行基因检测以帮助诊断。《阿尔茨海默病源性轻度认知障碍诊疗中国专家共识2021》也指出,有明确痴呆家族史的MCI患者应进行基因检测以帮助诊断。《中国阿尔茨海默病痴呆诊疗指南(2020年版)》认为致病基因突变(APP、PSEN1或PSEN2)有助于识别早发型、家族性AD(1A);易感基因突变(APOE4等位基因)有助于预测家族性AD的风险和脑淀粉样血管病的严重程度。

(3)血液检查
东丽株式会社提到,血液中MicroRNA分析,有可能对鉴别脑血管性痴呆以及预测从轻度认知障碍向痴呆的发展有所帮助。此外2023年7月底,国际临床医生和研究人员委员会在7月16日发布了新修订的阿尔茨海默病诊断指南草案(NIAAA Revised Clinical Guidelines for Alzheimer’s),其中包括在临床设置中使用基于血液生物标志物检测的建议。
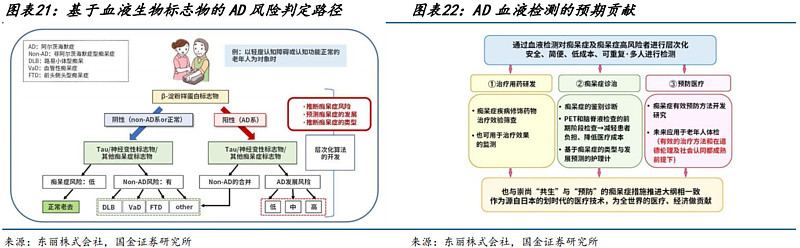
血液与CSF相比易于获取,侵袭性小,是临床试验的理想标本。
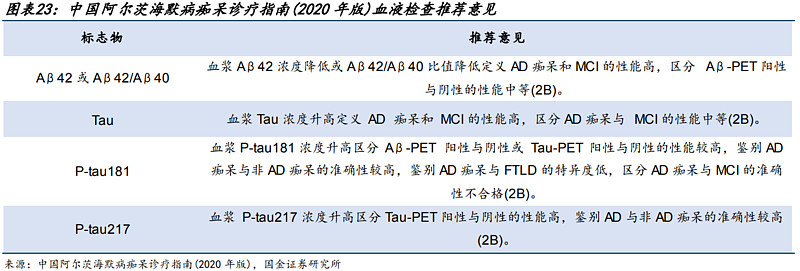
3.AD临床诊断技术对比
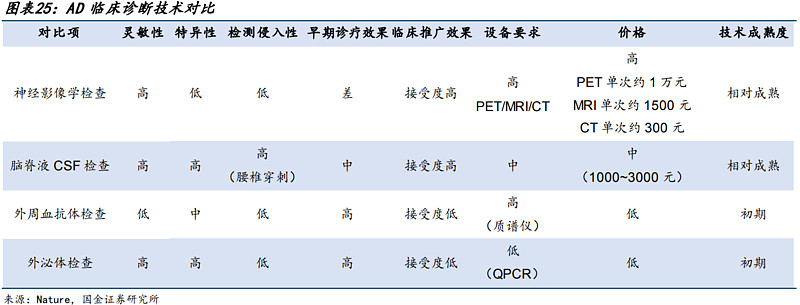
4.国内相关诊断产品
(1)脑影像学检查
截至23年11月8日,国内有两款AD影像学检查相关产品获批,分别为先通医药欧韦宁氟[18F]贝他苯注射液,及北陆药业磁共振成像辅助AI软件——医未脑医生。此外根据东诚药业23年9月15日公告,公司老年痴呆诊断性核素药物18F-APN-1607国内目前正在进行III临床试验,临床病例入组已经过半;关于老年痴呆治疗性药物,公司的参股公司新旭生技的mAb005产品已在美国开展I临床试验。

(2)体液标志物检查
目前中国AD诊断赛道参与厂商数量较少,主要集中在新兴技术研究方向。针对AD血液核心标志物,目前国内上市的主要方法学有:酶联免疫、免疫层析、流式荧光、化学发光以及数字酶联免疫法。预计随产品布局进程推进,将逐步丰富国内AD体液检测市场。

5.AI也可构成临床决策辅助的基础
(1)AI算法可预测2年痴呆风险
英国Llewellyn团队通过对患者在初诊时的家族史、病史、药物史等256种临床病理数据进行整合,发现四种AI模型的诊断性能相近,与CAIDE模型、BDSI模型相比,都能够更加准确地预测未来2年内的AD风险,尤其是基于XGB的AI模型,准确率达92%,AUC达0.92。国内“脑医生”亦可通过MRI图像辅助诊断。
(2)阿尔茨海默病患者的声学改变为人工智能“听声辨痴呆”建立了理论基础
人工智能“听声辨痴呆”的诊断逻辑是大约60-80%阿尔茨海默氏症患者有语言障碍症状;除认知测试外,最常用的阿尔茨海默氏症早期检测测试还包括声学特征,例如停顿、清晰度和声音质量。人工智能的方案是基于Framingham心脏研究(n=1084)进行的受试者神经心理学测试的数字语音记录的自动转录来识别痴呆的不同阶段,将测试中转录的句子编码为定量数据,并使用这些数据和参与者的人口统计特征训练和测试几个模型。结果显示,对照测试数据的平均曲线下面积(AUC)分别达到92.6%、88.0%和74.4%,用于区分正常认知与痴呆、正常或轻度认知障碍(MCI)与痴呆以及正常与MCI。ChatGPT也会给AI诊断带来新的机遇。
四、阿尔茨海默病药物治疗
AD治疗强调尽早诊断、及时治疗、终身管理。临床常用的认知改善药物包括胆碱酯酶抑制剂和谷氨酸受体拮抗剂,使用较多的为多奈哌齐和美金刚。对于中度、中重度的AD患者,1种胆碱酯酶抑制剂加上美金刚能有更好获益。针对伴发的精神行为症状,非药物治疗是首选,必要时联用抗精神病药,常用药物包括利培酮、奥氮平等。
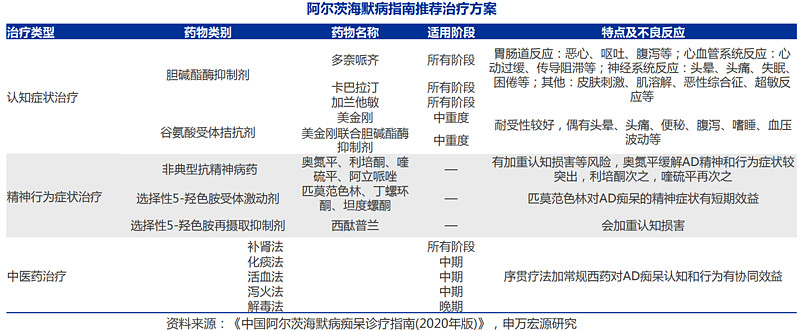
1.已批准药物以胆碱酯酶抑制剂为主
1993年FDA批准全球首个用于治疗中重度AD的药物他克林,但由于其肝毒性太大而后退市,随后的10年内FDA又连续批准了多奈哌齐、利斯的明、加兰他敏与盐酸美金刚这四种新化学实体。其中,除美金刚为NMDA抑制剂外,其余几款产品均为乙酰胆碱酯酶抑制剂(AChEI)。
2.已有药物疗效普遍不足,患者亟需新药
从疗效来看,已上市的几种阿尔茨海默药物只能短期控制症状,难以针对明确病因机制入手延缓疾病进程。根据《阿尔茨海默病患者需求洞察报告》,在接受调查的1000名受访患者中(75.7%接受了药物治疗),其中有近半数接受药物治疗患者反馈了对现有药物治疗效果的不满意。
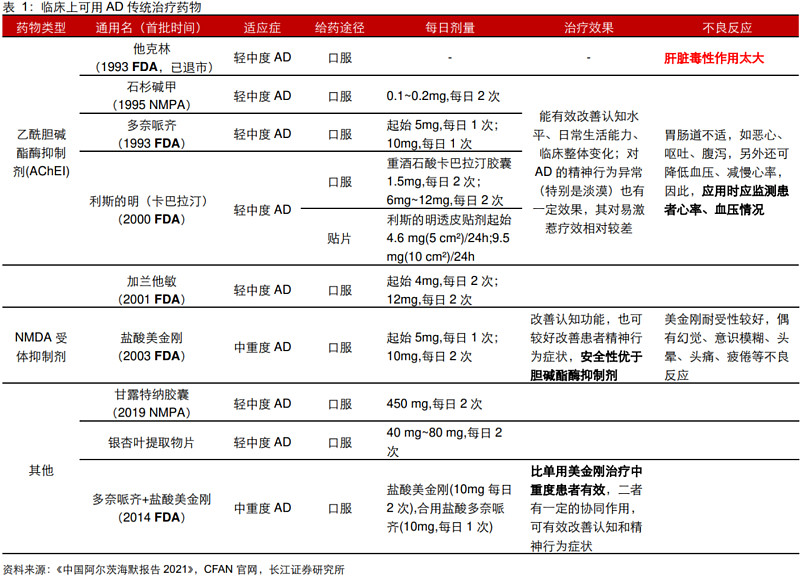
3.Aβ淀粉样蛋白研发最为热门
从研发端来看,目前全球AD药物开发靶点集中在Aβ淀粉样蛋白、Tau蛋白以及胆碱酯酶(及其受体)等靶点,其中Aβ淀粉样蛋白为目前在研项目最多、最为前沿的创新药物靶点。
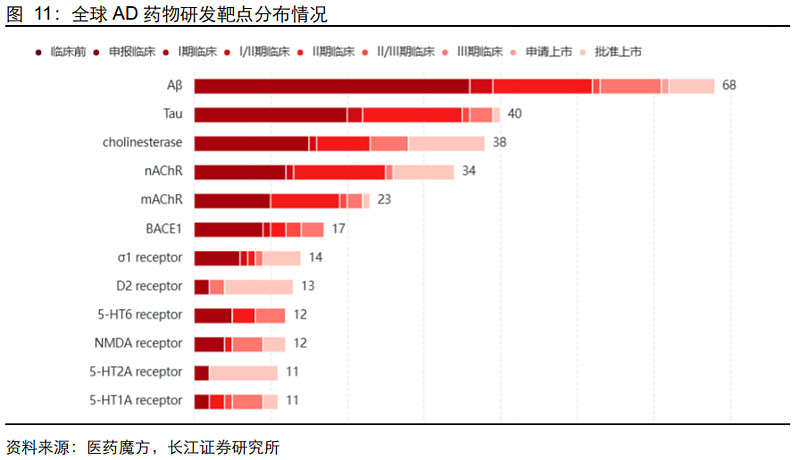
4.研发不断折戟,疗效与安全性常难兼顾
发病机制不明确、发病原因复杂、病程长且持续进展等是AD新药研发的主要困境。据文献报道,AD新药开发失败率高达99.6%,高于癌症药物研发失败率92%。以目前研究最为热门的Aβ淀粉样蛋白级联反应通路以及Tau蛋白两个开发路径为例,近20年来不少国际MNC都纷纷折戟,最常见的失败原因包括没有疗效或疗效不足、毒副作用等。
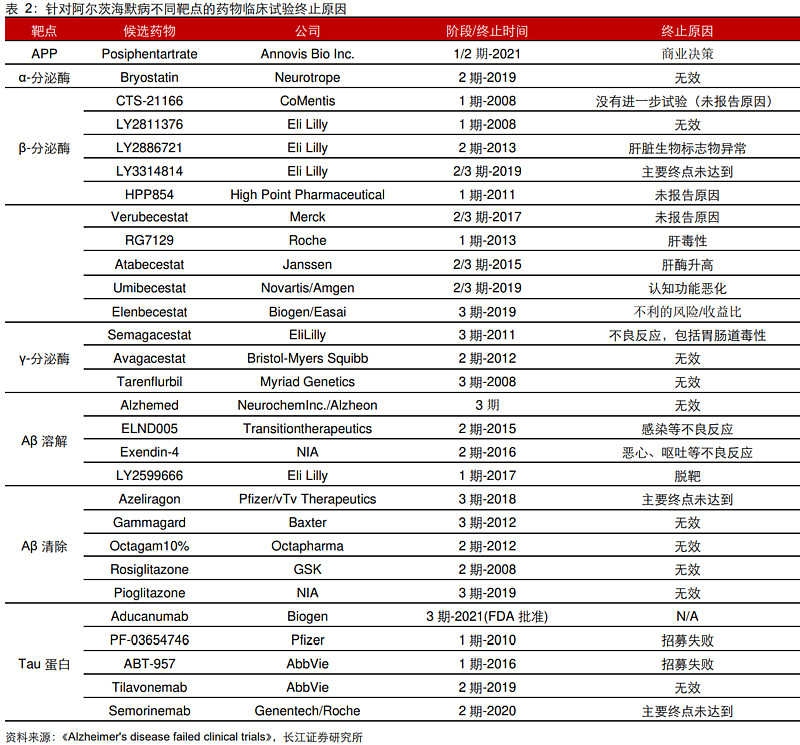
5.海外研究进展:海外捷报频传,Aβ率先打破僵局
(1)Aβ单抗取得突破,获得监管机构认可
自2003年美金刚获批之后,AD疾病领域连续18年没有新化学实体获得FDA的批准。直至2021年,Biogen与卫材药业联合开发的Aβ单抗药物Aducanumab首次获得FDA加速批准,随后Lecanemab、Donanemab相继发布积极III期临床数据并递交上市申请,表明监管机构对于Aβ疗法的逐步认可。针对极具潜力的Aβ单抗,多家MNC药企都有加速布局,例如礼来、罗氏、诺华、辉瑞等。
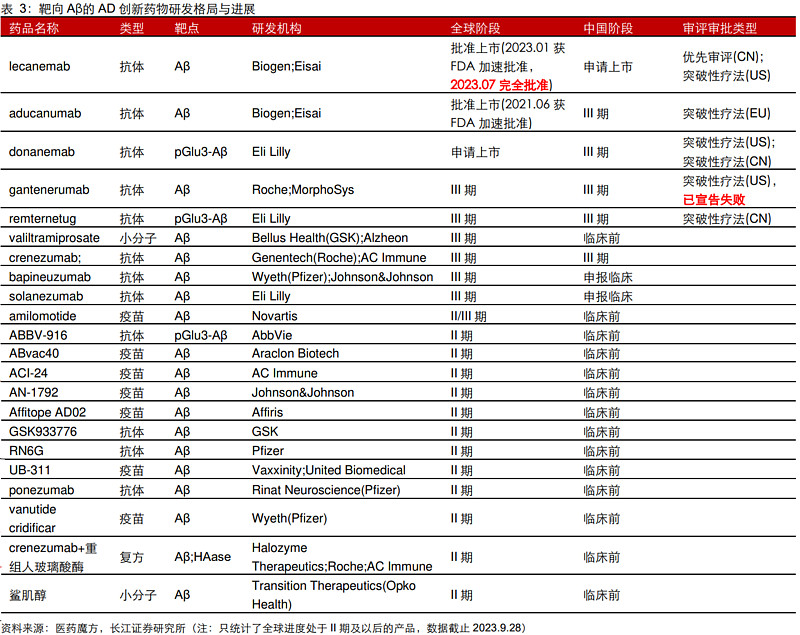
1)Aducanumab:全球首款Aβ单抗,商业化不及预期
Aducanumab(Aduhelm)(阿杜那单抗)是由Biogen和Eisai合作开发的一种靶向Aβ蛋白的单抗药物,在2021年6月获得FDA加速批准上市,是18年来FDA首次批准的AD治疗药物。
作用机制:Aducanumab可选择性地与大脑中的Aβ聚集物、可溶性寡聚体以及不溶性原纤维发生反应,从而减少大脑中淀粉样蛋白的负担;同时,另有文献报道在剩余斑块周围发现有脑巨噬细胞的积累,意味着其吞噬作用可用于去除Aβ斑块,从而减缓神经退行性变和疾病进展。
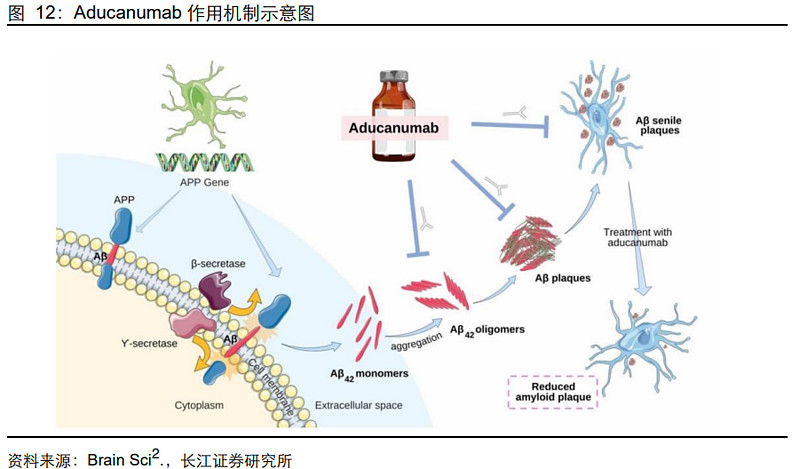
两项III期临床结果有所出入。只有试验EMERGE的高剂量组在临床痴呆总和(CDR-SB)评分以及其他次要终点的实现了相较于安慰剂组的明显改善(P值<0.05),该药物能持续并且显著降低大脑中淀粉样蛋白斑块的含量。但是该疗效备受争议,商业化远不及预期。Aducanumab由于在疗效上具有“不确定性”,美国医保与医助服务中心(CMS)将其医保覆盖范围严格限制为仅用于参加临床试验的患者,拒绝为普通患者支付医保费用,2021年与2022年Aducanumab的全球销售额仅分别为300万和480万美元。2022年4月,Biogen宣布撤回Aducanumab在欧洲的上市申请,并于同年5月宣布决定基本取消Aducanumab的商业化措施。
2)Lecanemab:首个完全获批的Aβ单抗,疗效获得认可
Lecanemab(Leqemb)(中文名为“乐意保”)是Biogen与卫材联合开发的一款Aβ单抗,2023年1月获FDA加速批准用于早期阿尔茨海默病治疗,2023年7月获得完全批准,成为20年来全球首个获得FDA完全批准的AD创新药。
III期临床研究取得阳性结果,且具有高度统计学意义。相关临床试验结果显示:相较于安慰剂组,Lecanemab治疗18个月后认知能力下降减缓了27%。
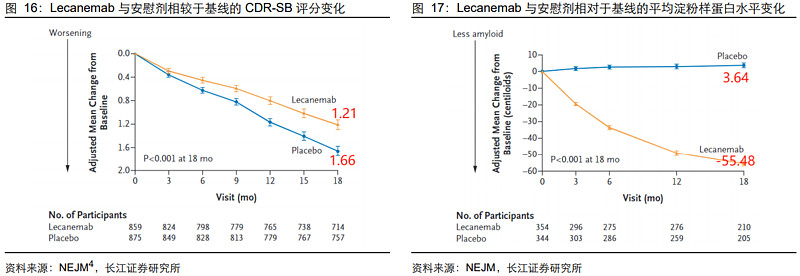
3)Donanemab:疗效再度升级,重新递交上市申请
Donanemab(多奈单抗)是礼来公司研发的靶向N3pG(修饰化β淀粉样蛋白斑块,是Aβ淀粉样蛋白的一种亚型)的单抗药物。2021年10月首次向FDA递交上市申请,不过由于临床证据不足被FDA拒绝,2023年7月礼来再次向FDA递交BLA申请。
相关试验结果显示:无论疾病基线和病理阶段如何,与安慰剂相比Donanemab都能带来认知和功能益处。若与采用与Lecanemab同样的CDR-SB评价体系,Donanemab相比于安慰剂将患者认知能力衰退速度减缓36%。
4)Remternetug:礼来新一代N3pG单抗,值得期待
Remternetug是礼来的又一款靶向N3pG的单抗,目前正在开展治疗早期症状性阿尔茨海默病的国际多中心(含中国)3期临床试验,国内已获得CDE突破性疗法认定。
相关试验结果显示:试验中所有Remternetug剂量组都出现了剂量依赖性的淀粉样蛋白减少,在第169天24例接受治疗的患者中有18人实现了淀粉样蛋白清除。
Aβ单抗药物小结:
Aβ单抗作为阿尔茨海默病领域备受瞩目的创新药物,在临床试验中已经展现出了突破性的疗效,但目前仍缺乏Aβ单抗与传统AD药物(胆碱酯酶抑制剂或NMDA受体抑制剂)的头对头临床研究,尚难以直接对比二者疗效差异。不过可以明确的是,Aβ单抗基于淀粉样蛋白假说,是一种全新的治疗机制,与传统AD药物并无绝对的替代关系,未来甚至也可能探索多种不同机制药物的联用方案。
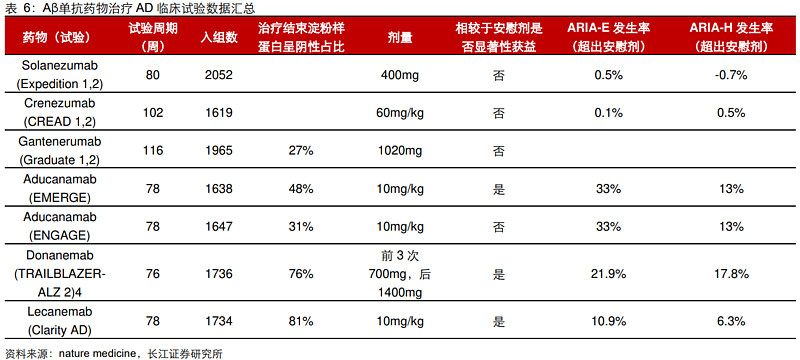
(2)Tau:靶点仍需验证,氢甲硫堇值得关注
Tau蛋白研发同样活跃,但至今没有药物获批。目前全球仍有多款tau蛋白靶向药物处于研发活跃状态,但大多处于早期临床阶段,其中全球进度最快的是Tau Rx Pharmaceuticals公司开发的氢甲硫堇,已经进入到III期临床阶段;而中国区仅有强生的Tau单抗药物posdinema进入到临床阶段。
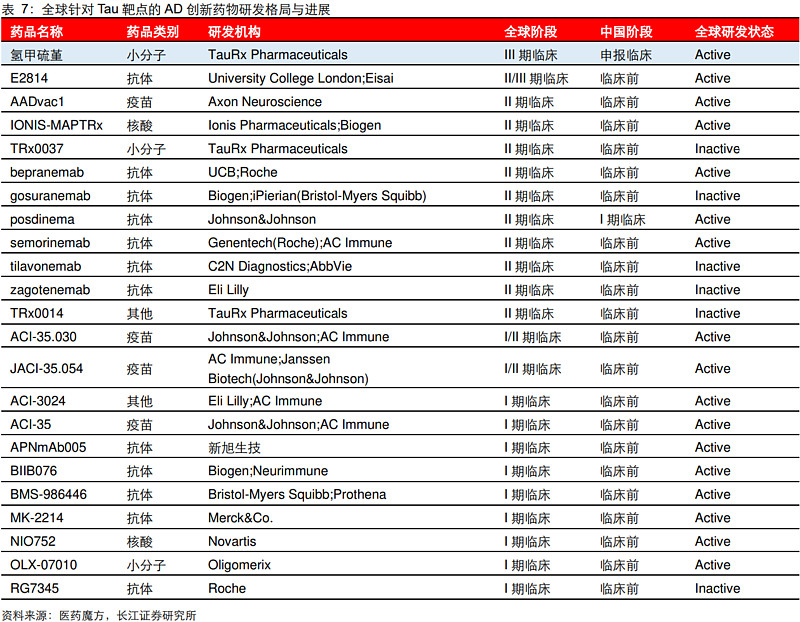
甲磺酸氢甲硫堇(HMTM)是Tau Rx Pharmaceuticals开发的一款口服tau蛋白聚集抑制剂。相关实验结果显示:对早期AD患者显示出认知和功能的持续改善(可超过18个月),对轻中度AD患者显示出认知和功能的稳定。
总体而言,靶向Tau蛋白的HMTM在AD疾病相关生物标记物变化以及初步疗效方面展现出了潜力,但临床证据仍比较缺乏,疗效还需进一步验证。
(3)GLP-1:痴呆发生率降低53%,司美开展III期临床
GLP-1RA在降糖和减重领域的表现已然靓眼,有文献表明GLP-1RA对早期AD亦有潜在疗效。
相比于安慰剂,GLP-1RA(司美格鲁肽或利拉鲁肽)受试者的痴呆发生率降低了53%。目前诺和诺德正在进行两项关于口服司美格鲁肽的III期安慰剂对照试验,以评估对早期AD(轻度认知障碍和轻度痴呆)的疗效,GLP-1靶点在AD领域的潜力值得关注。
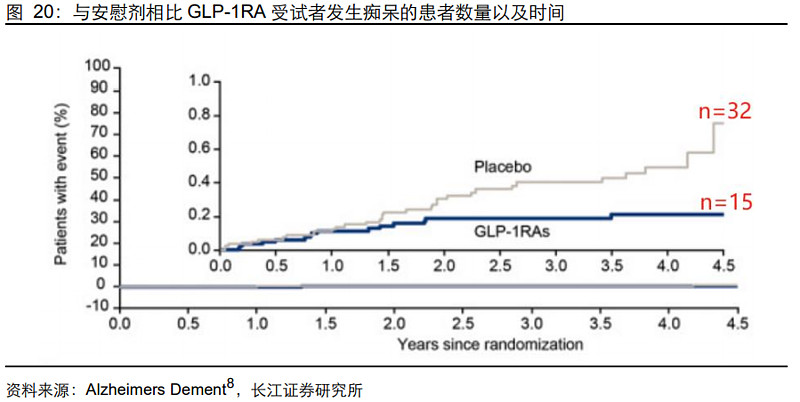
6.国内药物研发情况
国内AD创新药研发同样是久旱待甘霖,NMPA仅在2019年附条件批准了绿叶制药的GV-971这一款创新药,不过至今仍未获得完全批准。另外,国内在创新靶点例如Aβ蛋白、Tau蛋白等领域的新药开发上也明显落后于国际MNC。
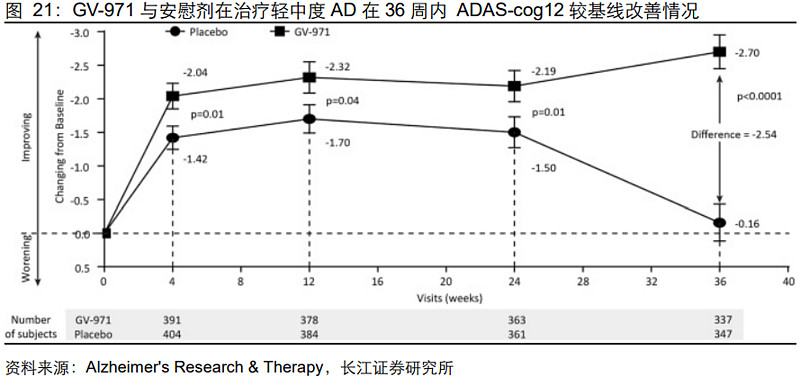
(1)GV-971:首个国产AD新药,国内销售将破亿
甘露特钠(GV-971)由中国海洋大学、中科院上海药物研究所和上海绿谷制药联合研发,是一种由海藻中提取的寡糖类分子。结果显示:与安慰剂组相比GV-971能明显改善AD患者认知功能障碍。安全性方面:与安慰剂组相比不良事件或严重不良事件的发生率无显著统计学差异。
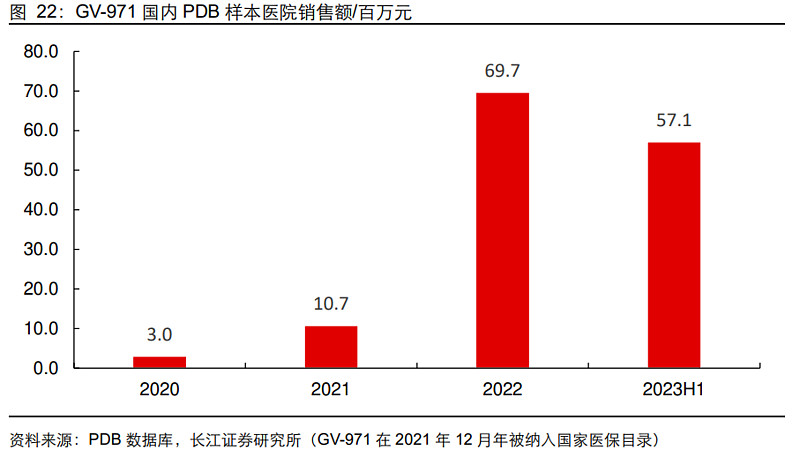
虽有争议,但国内销售可圈可点。因其作用机制尚不明确,加上全球III期临床中断,GV-971自上市以来便饱受争议。抛开学术问题,我们从PDB数据库可以看到:GV-971上市以来国内样本医院销售表现可圈可点,2023年H1样本销售达0.57亿元,预计全年将实现破亿(实际终端销售一般还需放大2-6倍)。
(2)琥珀八氢氨吖啶:老树开新花,优效性尚未可知
琥珀八氢氨吖啶片是由通化金马自主研发的治疗轻中度AD的创新药物,属于传统的胆碱酯酶抑制剂,可以同时抑制乙酰胆碱酯酶和丁酰胆碱酯酶从而发挥双重抑制功能。
琥珀八氢氨吖啶片在2023年9月完成III期临床的盲态数据审核,统计结果表明:与安慰剂组比较,琥珀八氢氨吖啶片对ADAS-cog的改善具有明显的临床意义。虽然琥珀八氢氨吖啶片在III期临床中展现出了相较于安慰剂的疗效明显改善,但与阳性对照药物(多奈哌齐)相比是否达到优效或非劣效还尚未明确。
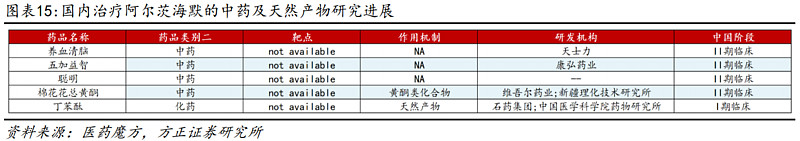
(3)中药:复杂机制或具优势,国内最快到II期
AD发病机制的病理过程十分复杂,涉及多种机制参与,而中药具有多成分、多途径、多靶点的作用特点,对于具有复杂病理机制的AD或许具有独特治疗潜力。目前国内有养血清脑、五加益智以及棉花花总黄酮这几款产品进入到II期临床研究阶段。其中,五加益智颗粒是康弘药业子公司济生堂自主研发的6.1类中药创新药物,目前正在开展“头对头”盐酸多奈哌齐片的IIb期临床试验。

一些天然药物已被证明可以减缓AD的进展和相关症状,比如:木脂素、类黄酮、单宁、多酚、三萜类化合物、甾醇和生物碱,已被证明具有抗炎、抗淀粉样变性、抗胆碱酯酶和抗炎性的属性。国内目前天士力、康弘药业、石药集团等均将中药及天然产物推进到了临床I、II期。
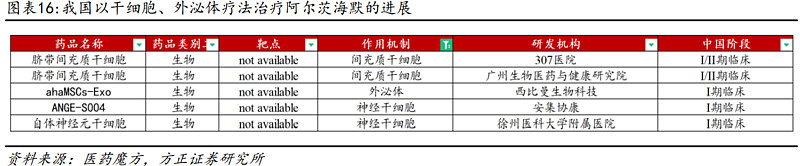
(4)干细胞疗法:能够有效的改善患者病情,未来可期
在寻找阿尔茨海默病的治疗方法的过程中,一个新兴的医学分支带来了新的希望。干细胞疗法已经被用于治疗各种癌症以及血液和免疫系统的疾病。目前我国已有多家机构将干细胞及外泌体疗法推进到了临床I期和II期,临床前试验和临床试验表明:干细胞移植治疗阿尔茨海默症不仅可以调节脑内炎症的大环境,还能促进神经再生和突触连接,能够有效的改善患者病情,干细胞治疗阿尔茨海默症未来可期,能让更多老年痴呆患者病情得到控制和有效改善。
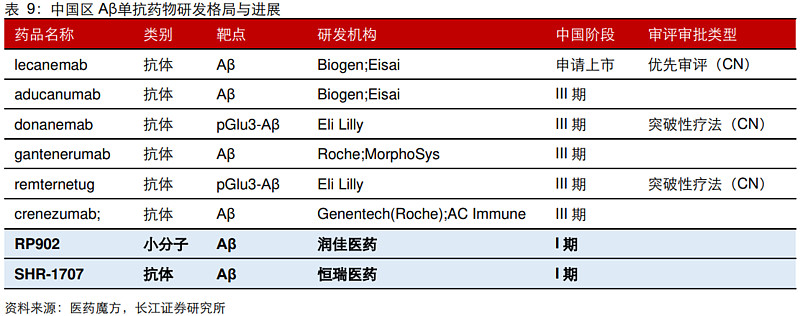
(5)Aβ:国内研发明显滞后,仅两款进入临床
与MNC形成对比,国内针对Aβ单抗的研发鲜有进展。针对创新靶点Aβ,国内厂家中仅润佳医药的小分子RP-902以及恒瑞医药的单抗SHR-1707进入到临床阶段。其中,SHR-1707是由恒瑞医药自主研发的人源化Aβ单抗,2023年3月在国内刚刚完成针对早期AD的Ib期临床试验(NCT05681819)的首例患者入组。
此文章未完,请见:【阿尔茨海默病行业深度:治疗现状、竞争格局、市场空间及相关公司深度梳理(二)】或关注“慧博资讯微信”流畅阅读!