ADC药物
抗体偶联药物(Antibody–Drug Conjugates,ADC)是一类将具有细胞杀伤能力的小分子化疗药物偶联到特异性识别抗原的单克隆抗体(mAbs)上的药物。近年来在抗肿瘤药物的研发领域,ADC药物技术被应用于治疗多种类型的肿瘤疾病。按照目前的发展趋势,ADC药物将占据更大的市场份额。
ADC药物相比单抗药物(Monoclonal Antibody,mAb)有更高的复杂性,在此类药物的生产过程中除涉及单抗药物生产的全部过程外,还包括对抗体的偶联修饰过程。因此对ADC药物的质量表征不仅需要研究抗体本身,还需要进行更多维度的表征如DAR值表征、偶联位点分析等。
虽然距离第一个ADC药物Mylotarg首次上市已经过去了20多年,我们对ADC药物的理解也有了长足的进步,但是开发一款有效的全新ADC药物分子仍然不是一件简单的事情。对于这类药物分子的开发,除了需要进行单抗药物本身的开发外,还要考虑连接子设计和载药的选择,使得此类药物的开发难度更高。
本系列文章基于东曜药业在ADC药物领域多年的分析研究经验,对ADC药物关键质量属性表征和监控方法进行整理和呈现。
DAR值检测方法
药物抗体比(Drug-to-Antibody Ratio,DAR)是ADC药物开发生产过程中一个极为重要的关键质量参数。目前有多种方法可以用于DAR值表征,包括紫外/可见分光光度法(UV/Vis)、疏水相互作用色谱法(HIC-HPLC)、反向色谱法(RP-HPLC)和液相质谱法(LC-MS)。针对不同的ADC药物处于不同开发生产阶段,应选用合适的方法来保证产品质量和开发效率。
基于质谱的DAR值检测
样品经过液相色谱柱的脱盐后导入到QTOF质谱仪器分析,可以产生一系列带不同数量电荷的m/z信号。对质谱图进行去卷积处理,就可以得到一组不含电荷带不同数量载药抗体分子的分子量分布图。根据抗体和载药的理论分子量,可以确定去卷积后计算出分子量峰的载药数量,并依据分子量分布图中各峰的信号强度计算,得到该ADC分子的DAR值和载药分布(Drug Load Distribution,DLD)(图1)。相比于其他方法,基于质谱的检测方法可以快速直接地得到ADC药物的DAR值和DLD信息,极大地加速ADC药物早期开发进程。同时,也可以和HIC-HPLC或RP-HPLC产生的数据进行交叉验证。
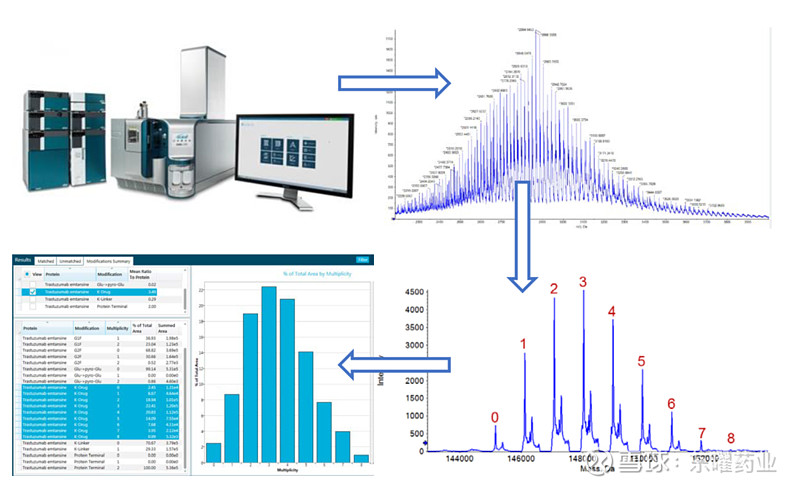
图1 利用高分辨率仪器测定ADC药物的DAR值[1]
ADC药物工艺开发流程
现阶段典型的ADC药物生产流程包括单克隆抗体的制备及换液、抗体还原处理、连接子载药基团与抗体偶联、纯化除杂操作、置换制剂缓冲液等过程(图2)。生产过程中的每个步骤对最终产品的质量都有决定性影响,因此,对这些步骤进行工艺开发和验证是必要的,DAR值则是衡量这些工艺范围是否有效的一个重要依据。针对不同偶联方式的ADC药物,一般需要开发不同的分析方法。
一般而言,小分子具有与抗体不同的最大紫外吸收波长,当多个小分子与抗体偶联后,可通过消光系数分别计算溶液中抗体和小分子的摩尔浓度来计算DAR值,但是这种方法容易受到溶液中游离小分子的干扰。另一方面,小分子的极性一般比抗体分子小,使得抗体分子在偶联不同数量的小分子后,其疏水性也呈现不同分布,因此会使用疏水作用色谱或反向色谱分离不同载药数量的抗体分子,但是通过这种方式获取的谱图,也需要进一步鉴定后才能用于检测。基于质谱的DAR值检测则是依据抗体偶联上不同数量小分子后分子量的变化来进行分析的,这类方法对仪器设备就有更高要求。另外,还存在不同载药分子离子化效率不同的问题。
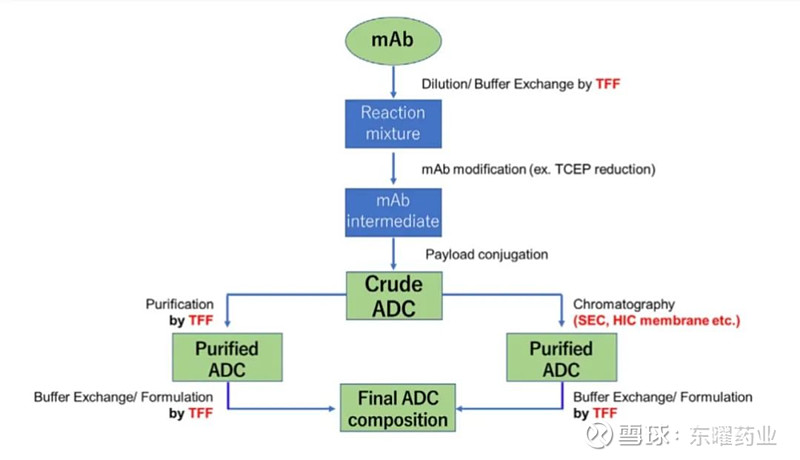
图2 ADC药物的生产过程[2]
以下针对不同偶联方式的MS-DAR检测方法做进一步的讨论。
基于赖氨酸偶联的ADC药物DAR值分析
基于天然氨基酸偶联的ADC药物,其偶联位点局限于赖氨酸和半胱氨酸这2种氨基酸。以Kadcyla为例, Kadcyla是一种通过SMCC连接子将DM1毒素分子连接到曲妥珠单抗序列中赖氨酸残基上的ADC药物(图3)。DM1分子被随机偶联在轻链和重链序列中至少20个赖氨酸位点上,最终产生平均DAR值约为4的混合物。一般地,样品中的单抗分子载药数量在0到8范围内分布(图4)。
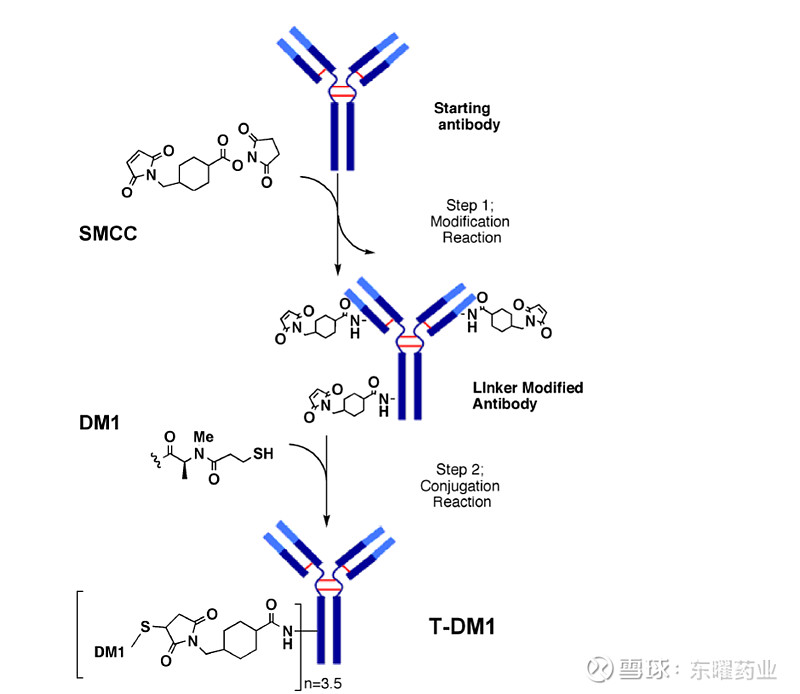
图3 Kadcyla的生产过程[3]
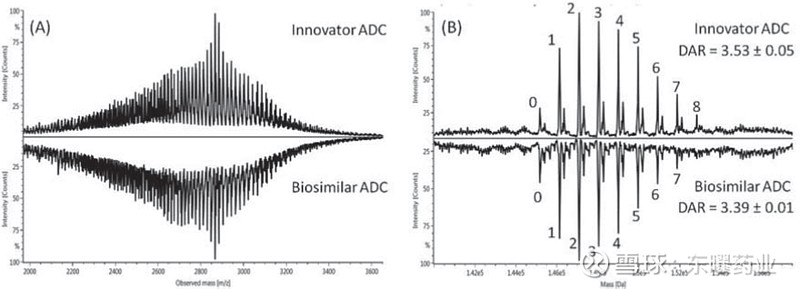
图4 Kadcyla原研药和生物类似药的对比[3]
由于该ADC分子的生产过程是一个两步反应,因此样品混合物中除了有载药数量不同的抗体分子外,还存在一些包含空载连接子的抗体分子。通过对偶联工艺的优化,可以降低ADC样品中空载连接子的比例。但是这类工艺相关杂质的理化性质与主要成分除分子量外没有明显区别, 因此对于此类项目的工艺优化样品,最为快速有效的检测方法便是将样品脱糖处理后进行质谱分析。如图所示(图5),能在一次分析中同时监测样品的DAR值、DLD和空载连接子的占比。
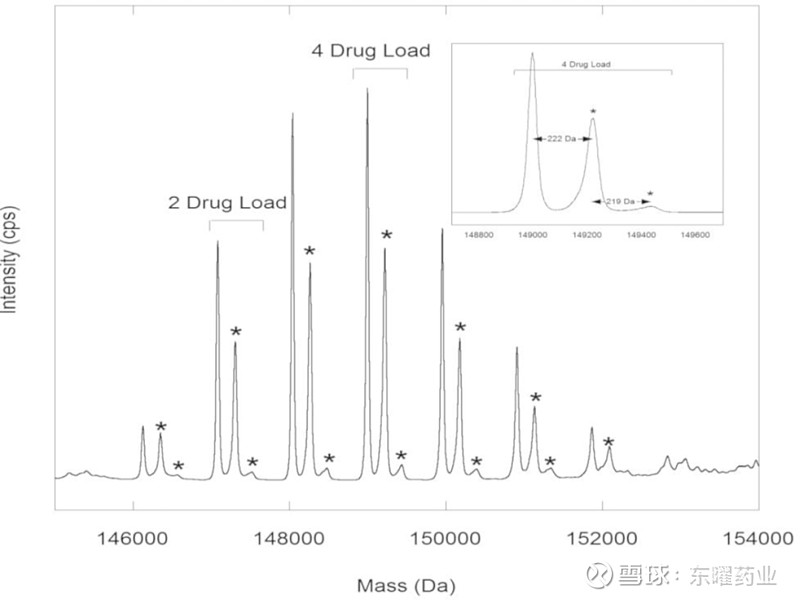
图5 高比例空载连接子样品的分子量分布图[4]
基于半胱氨酸偶联的ADC药物DAR值分析
对于天然的IgG1单克隆抗体,其序列内总共包含32个半胱氨酸,可形成4对链间二硫键和12对链内二硫键。基于半胱氨酸偶联的ADC药物在生产过程中需要选择性打开4对链间二硫键中的部分或全部,随后通过连接子将MMAE,DXd等毒素分子偶联在半胱氨酸的巯基上,由此,便产生了载药数量分别为0、2、4、6、8的分布。由于在生产过程中抗体轻链和重链间,重链和重链间的共价连接键已经被破坏,通过对ADC样品进行脱糖还原处理,再经过液相脱盐,最后ADC药物的轻链、重链分别被洗脱进质谱仪器得到相对应的分子量分布图。轻链和重链理论上分别有1个和3个偶联位点,在轻链分子量分布图中可以观测到L0和L1这2种分布,在重链分子量分布图中可以观测到H0、H1、H2和H3这4种分布(图6)。
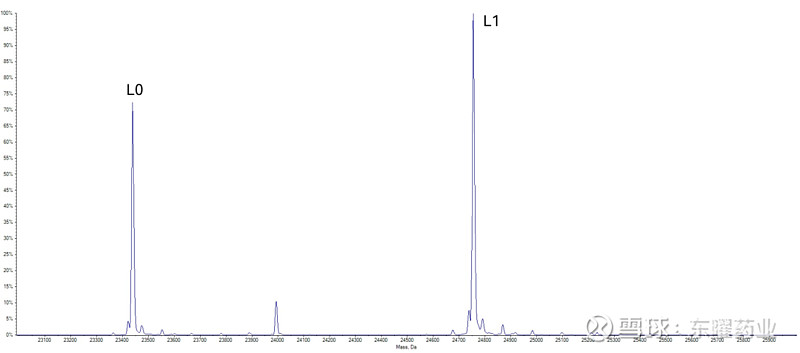
图6a 半胱氨酸偶联ADC分子轻链分子量分布图
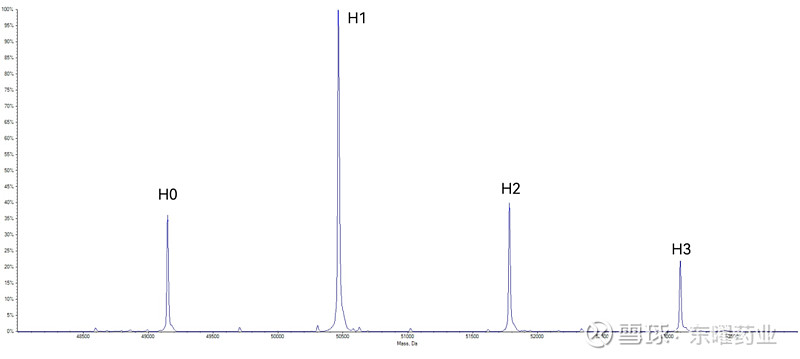
图6b 半胱氨酸偶联ADC分子重链分子量分布图
相比基于赖氨酸的偶联工艺,此类ADC药物的生产过程引入了能够破坏抗体结构稳定性的试剂,最终产品的质量受更多因素的影响,产生了更多和工艺相关的杂质,需要更加细致的分析来表征此类ADC药物。对此类ADC药物进行基于质谱的MS-DAR值检测除了在亚基水平上进行之外,还需要表征其完整水平上的DAR值。完整水平上分子量分布结果和HIC检测方法结果类似,直观地呈现出载药数量为0、2、4、6、8的分布(图7)。
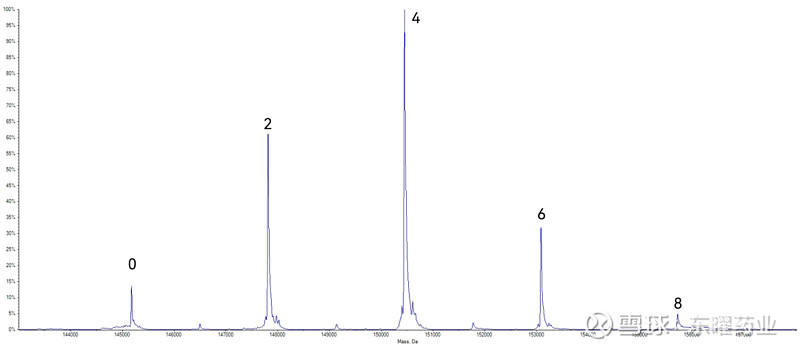
图7 半胱氨酸偶联ADC分子完整分子量分布图
在支持此类项目早期工艺开发过程中,平台化的分析方法只分离轻链分子和重链分子,对不同载药组分别进行液相分离,MS-DAR检测方法可以直接根据鉴定的分子量分布来确定分子的载药分布,对样品中存在的低丰度杂质有更好监测,可以在较短时间内给出可信度较高的结果,加速工艺开发进程。
基于糖定点偶联的ADC药物DAR值分析
天然IgG1单克隆抗体,在其2条重链的Fc区域各有一个固定的N糖基化位点。Synaffix的糖定点偶联技术就是在利用内切糖苷酶将该位点的N糖切下后再使用糖基转移酶将连接子转移到该位点上,最后利用连接子上的叠氮基团与环辛炔反应形成稳定的ADC药物。与上述2类ADC药物相比,此类ADC药物的整体结构没有被破坏,偶联位点为固定的糖基化位点,在质谱分析过程中,可以进行完整水平的分析得到载药数量为0和2的分布(图8)。
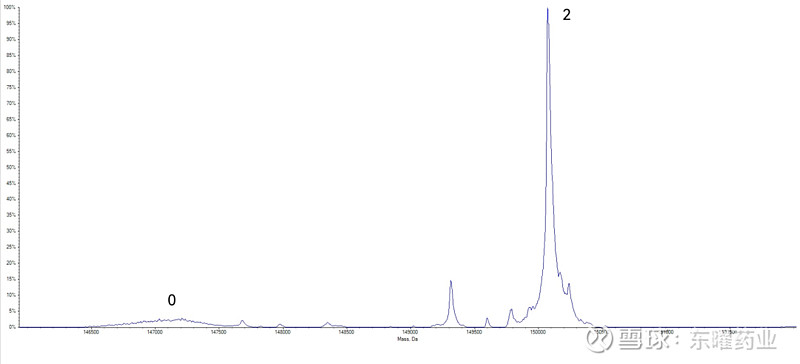
图8 糖定点偶联ADC分子完整分子量分布图
为了降低本底干扰,更准确地对DAR0分子进行研究,可以将抗体还原后进行质谱分析。此时,抗体轻链不载药,抗体重链存在H0和H1的载药分布(图9)。
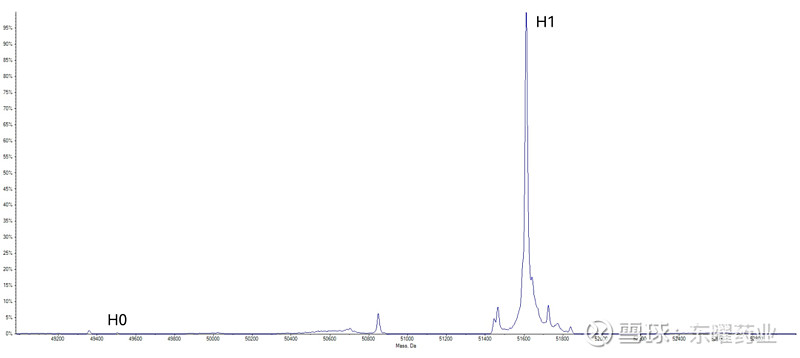
图9 糖定点偶联ADC分子重链分子量分布图
基于糖定点偶联的ADC项目,在生产过程中引入酶催化反应,适宜的催化条件是此类药物生产成功的一个重要因素。在工艺开发过程中选择合适的DAR值检测方法不仅能够提高工艺开发的效率,更能在早期阶段降低开发风险。
小结
综上所述,对不同偶联类型的ADC药物,在DAR值检测方面皆有不同特点需要注意,包括偶联技术、药物载荷数量分布以及对抗体结构稳定性的影响等。因此,在药物开发过程中,根据具体的工艺和需求,选择适合的检测方法是至关重要的,这有助于支持工艺的优化和确保药物质量。
东曜药业已经建立了多个高效的MS-DAR检测分析平台方法, 这些方法具备快速高通量地进行样品检测的能力。通过这些平台方法,可以对样品中的大小分子进行深入表征,从而更全面地了解ADC药物的组成和结构。目前,东曜药业的质谱分析平台已经配备了一台三重四极杆(3Q)仪器、两台高分辨率QTOF仪器以及一台高分辨率QE仪器。这些先进的仪器设备为药物开发过程中的DAR值检测和药物质量评估提供了强有力的支持。在CDMO项目的实施过程中,这些分析平台将为药物生产过程提供准确、高效、可靠的数据,从而加快项目的进展,并确保产品能够更好地实现落地。
参考文献
[1] Wen J, Suya L, Doug S, et al. Intact Analysis of Antibody Drug Conjugates. AB Sciex, 2019.
[2] Matsuda Y . Current approaches for the purification of antibody–drug conjugates. Journal of Separation Science, 2021.
[3] Michael T K, Yan C, Joseph M, et al. Statistical modeling of the drug load distribution on trastuzumab emtansine (Kadcyla), a lysine-linked antibody drug conjugate. Bioconjug Chem, 2014.
[4] Yan C, Michael T K, Laura Z, et al. Structural Characterization of Cross-Linked Species in Trastuzumab Emtansine (Kadcyla). Bioconjug Chem, 2016.

关于东曜药业股份有限公司(股票代码:1875.HK)
东曜药业从事抗体及ADC药物开发10多年,具有丰富的工艺开发与商业化生产经验。
公司于2019年在香港联交所主板上市,2021年全面转型,致力于成为全球药物开发领域专业CDMO合作伙伴,提供生物药开发到生产一站式解决方案。
东曜药业拥有从研发、工艺开发、临床试验、注册报批到商业化生产的全流程经验,建立了完整的ADC技术平台,具备核心偶联工艺和放大的技术优势,以及ADC关键质量属性的自主分析能力,保证产品高质量开发。
在生产方面,东曜药业拥有多条符合GMP标准的集抗体、ADC原液及制剂于一体、国内产能领先的OEB-5级别ADC CDMO商业化生产线,避免了中国与其他国家对于分段生产议题上的法规不确定性风险,抗体产能达万升级以上,并有商业化产品在线生产。
在质量体系方面,东曜药业质量管理体系满足中国/美国/欧盟申报要求,通过国家药品注册生产现场和GMP质量管理体系核查,具有丰富的产品上市注册核查经验,已为客户提供数十个抗体及ADC项目的中美欧工艺开发、临床申报及生产服务。
东曜药业秉持“以品质 助创新 共成长”的服务理念,为产品高质量研发与商业化生产保驾护航,赋能合作伙伴,共创双赢。
往期推荐


业务垂询 bd@totbiopharm.com