对生物靶点具有高选择性的高活性药物成分(High Potency Active Pharmaceutical Ingredient,HPAPI)已广泛用于抗体偶联药物(Antibody-Drug Conjugates,ADC) 领域。如果这些化合物及其衍生物不小心接触到皮肤,被吸入或摄入,都会对人体造成伤害。所以,必须避免生产人员直接暴露于这些药物。另一方面,生物制品需要同时保证其免受来自生产人员和生产环境带来的任何污染。因此需要一个“量身定制”的生产环境确保ADC的稳定生产。
这就需要在整个厂房设计、设备选型、人物流流向、生产管理、人员培训等环节中采取合理有效的预防管理措施,以此来降低操作人员的暴露风险以及防止交叉污染。本期我们将结合东曜药业在近十年ADC药物开发过程中累积的经验,通过上下两篇文章,分享在“ADC原液生产中安全处理高活性物料的考虑因素”。
ICH Q7原料药指南中对高活性药物成分的描述为:低剂量可产生生殖或/和发育影响的化合物,具有高药理活性/毒性和高度潜在致敏性。对于操作高活性药物成分带来的职业风险主要是根据几个指标来确定:日常允许接触量(Acceptance Daily Exposure,ADE),职业暴露等级(Occupational Exposure Band,OEB),以及职业暴露限度(Occupational Exposure Limit,OEL)。每个化合物都有具体的OEL数值,不同的OEL数值对应不同的防护要求,因此OEL更能准确地评估药物生产活动中的暴露风险。但是对于OEL数据不确定的化合物(例如处于临床前新药开发阶段的候选化合物),通常使用OEB等级系统来确定相关控制措施。对于典型的高活性物质OEB等级系统如图1:
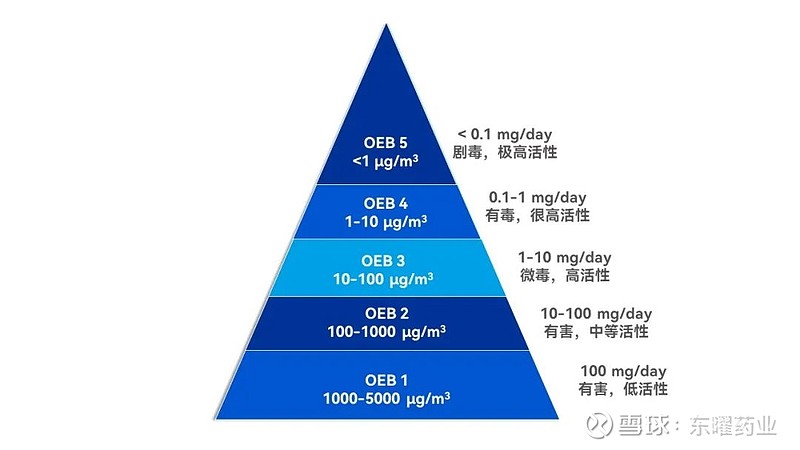
图1 OEB分级
一般来说,OEB等级为2级或者3级的化合物可以通过风险评估,采取分阶段生产并进行清洁确认;对于OEB等级为4级或者5级的同类产品应尽可能使用专用设备设施、一次性设备或者密闭设备进行生产,减少和避免对其他产品的影响。对于毒性未知但确信其具有潜在的高毒性的化合物,建议将它们归为OEB4级或5级。
为了能在高活性物质处理环节中最大限度降低人员暴露和交叉污染风险,需要开展风险分析,确定选择合适的防护设备和规范操作流程。对于安全处理OEB 4-5等级的高活性物质,操作人员需要配备符合防护要求级别的个人防护设备(Personal Protective Equipment,PPE)。最新版欧盟GMP Annex 1(2020实施)针对污染风险控管有严格的规范,要求药厂提供洁净服细菌阻隔效率(Bacterial Filtration Efficiency,BFE) /颗粒阻隔效率 (Particle Filtration Efficiency,PFE)的测试与验证。
人员保护
防护服
对于在ADC原液生产阶段涉及高活性物质的称量、配制、转移等操作工序中,操作人员需穿戴具有高阻隔效率的一次性防护服(图2)进行生产。同时生产区域需要提供应急人员防护措施,以防高活性物料直接暴露于生产环境中,进而对人员产生危害。图3为一种专门为高活性物料操作人员提供保护的动力净化型防毒穿戴设备(Hood Powered Air-Purifying Respirator,HPAPR)。

图2 操作高活性物料时穿戴的一次性防护服


图3 用于高活性物料暴露时的应急穿戴设备
另一方面,处理高活性物质单单依靠一次性防护服等个人防护设备还远远不够,为了防止相关高活性物质的泄露扩散,还需从泄露扩散风险源头控制,使用如隔离器(Isolator)等专业设备,我们将在下一篇继续结合东曜药业的实操经验,阐释ADC原液生产中安全处理高活性物料的其他考虑因素。
左右滑动查看更多




东曜药业已建设符合国际GMP标准的ADC原液中试及商业化生产车间,ADC原液设计年产量达60,000g,并配备OEB-5等级隔离器,结合100L、200L、500L偶联反应釜,最高可达5kg/批的偶联规模。同时,搭配2条一地化ADC制剂生产线,具备注射液和冻干无菌制剂生产能力,产线采用国际进口星德科(原博世包装技术)隔离器灌装联动线(200瓶/分钟),配备OEB-5等级隔离器、40㎡冻干能力,最大限度满足ADC临床和商业化生产需求。

关于东曜药业股份有限公司(股票代码:1875.HK)
东曜药业从事ADC以及抗体药物开发10多年,具有丰富的工艺开发与商业化生产经验。
公司于2019年在香港联交所主板上市,2021年全面转型,致力于成为全球药物开发领域专业CDMO合作伙伴,提供生物药开发到生产一站式解决方案。
东曜药业拥有从研发、工艺开发、临床试验、注册报批到商业化生产的全流程经验,建立了完整的ADC技术平台,具备核心偶联工艺和放大的技术优势,以及ADC关键质量属性的自主分析能力,保证产品高质量开发。
在生产方面,东曜药业拥有多条符合GMP标准的集抗体、ADC原液及制剂于一体、国内产能领先的OEB-5级别ADC CDMO商业化生产线,避免了中国与其他国家对于分段生产议题上的法规不确定性风险,抗体产能达万升级以上,并有商业化产品在线生产。
在质量体系方面,东曜药业质量管理体系满足中国/美国/欧盟申报要求,通过国家药品注册生产现场和GMP质量管理体系核查,具有丰富的产品上市注册核查经验,已为客户提供数十个抗体及ADC项目的中美欧工艺开发、临床申报及生产服务。
东曜药业秉持“以品质 助创新 共成长”的服务理念,为产品高质量研发与商业化生产保驾护航,赋能合作伙伴,共创双赢。
往期推荐


业务垂询 bd@totbiopharm.com